Атеросклероз и связанные с ним заболевания занимают ведущее место среди причин смертности во многих странах мира, а Россия является одним из мировых «лидеров» по уровню данного показателя [1]. В предупреждении кардиальной заболеваемости и смертности важнейшая роль принадлежит профилактике, в частности, стратегии высокого риска — выявления в популяции лиц с повышенным риском развития сердечно-сосудистых заболеваний (ССЗ) [2]. В настоящее время наряду с традиционными моделями расчета суммарного риска развития заболеваний сердца (SCORE, Фрамингемская шкала и др.), которые используются для идентификации таких пациентов, особое место занимает применение инструментальных методов, позволяющих на раннем этапе диагностировать субклинический патологический процесс и прогнозировать риск развития неблагоприятных сердечно-сосудистых исходов. К числу таких методов относится ультразвуковое исследование (УЗИ) сонных артерий (СА) [3].
 УЗИ экстракраниальных сегментов СА позволяет визуализировать ранние, субклинические атеросклеротические изменения в сосудах. Маркерами субклинического атеросклероза служат толщина интимы—медии (ТИМ) и наличие неокклюзирующей атеросклеротической бляшки (АСБ) [4, 5]. Данные о ТИМ и наличии АСБ дополняют информацию, полученную на основании оценки традиционных факторов риска (ФР) развития сердечно-сосудистых осложнений (ССО) и улучшают ее прогностическую ценность [6]. Целесообразность использования показателей субклинического атеросклероза СА показана во многих клинических исследованиях, продемонстрировавших статистически значимую корреляцию ТИМ и АСБ с риском развития инфаркта миокарда (ИМ), инсульта и сердечно-сосудистой смерти [7, 8].
УЗИ экстракраниальных сегментов СА позволяет визуализировать ранние, субклинические атеросклеротические изменения в сосудах. Маркерами субклинического атеросклероза служат толщина интимы—медии (ТИМ) и наличие неокклюзирующей атеросклеротической бляшки (АСБ) [4, 5]. Данные о ТИМ и наличии АСБ дополняют информацию, полученную на основании оценки традиционных факторов риска (ФР) развития сердечно-сосудистых осложнений (ССО) и улучшают ее прогностическую ценность [6]. Целесообразность использования показателей субклинического атеросклероза СА показана во многих клинических исследованиях, продемонстрировавших статистически значимую корреляцию ТИМ и АСБ с риском развития инфаркта миокарда (ИМ), инсульта и сердечно-сосудистой смерти [7, 8].
В настоящее время проведение электрокардиографического стресс-теста с прогностической целью у пациентов в отсутствие симптомов не считается оправданным [3, 9]. При этом принимается во внимание неинформативность такого теста с точки зрения выявления ишемии. Между тем неэлектрокардиографические параметры теста, отрицательного в отношении ишемии (толерантность к физической нагрузке, реакция частоты сердечных сокращений — ЧСС — и артериального давления — АД — на физическую нагрузку), могут нести важную прогностическую информацию. По данным многочисленных клинических исследований, неинвазивная оценка реакции сердечно-сосудистой системы на физическую нагрузку во время отрицательного ишемического стресс-теста дает возможность прогнозировать риск развития клинических исходов атеросклероза. Таким образом, представляется интересным сопоставить результаты двух обсуждаемых исследований у лиц без симптомов заболевания и выявить возможную взаимосвязь между параметрами отрицательного стресс-теста и субклиническим атеросклерозом по данным УЗИ СА, что и явилось целью нашего исследования.
Материал и методы
 Для включения в одномоментное исследование обследовали лиц без клинических проявлений ишемической болезни сердца (ИБС), находившихся на стационарном лечении в Городской Покровской больнице Санкт-Петербурга. Проводили оценку ФР развития ССО, выполняли электрокардиографический тест с физической нагрузкой и УЗИ внечерепных сегментов СА.
Для включения в одномоментное исследование обследовали лиц без клинических проявлений ишемической болезни сердца (ИБС), находившихся на стационарном лечении в Городской Покровской больнице Санкт-Петербурга. Проводили оценку ФР развития ССО, выполняли электрокардиографический тест с физической нагрузкой и УЗИ внечерепных сегментов СА.
Критериями включения в исследование являлись:
1) возраст 35—75 лет для мужчин и 40—75 лет для женщин; 2) наличие одного или более традиционных ФР развития ССО (возраст, артериальная гипертензия — АГ, дислипидемия, курение, отягощенная наследственность).
Критериями исключения из исследования были:
1) документированная ИБС; 2) наличие заболеваний, эквивалентных по степени риска ИБС (сахарный диабет, стенозирующий атеросклероз СА, аневризма брюшной аорты, клинически проявляющийся атеросклероз артерий нижних конечностей); 3) состояния, препятствующие выполнению или интерпретации электрокардио-графического стресс-теста (синдром слабости синусного узла, необходимость приема лекарственных препаратов), препятствующих нормальному приросту ЧСС или влияющих на процессы реполяризации (поражение суставов нижних конечностей), изменения на электрокардиограмме в покое (гипертрофия левого желудочка с вторичными нарушениями реполяризации, депрессия сегмента ST ≥1 мм, полная блокада левой ножки пучка Гиса — БЛНПГ, желудочковая стимуляция, синдром Вольфа—Паркинсона—Уайта); 4) наличие противопоказаний к выполнению нагрузочного теста (неконтролируемая АГ, хроническая сердечная недостаточность III—IV функционального класса по классификации Нью-Йоркской ассоциации сердца, тромбоэмболия легочной артерии, тяжелые пороки клапанов, тахиаритмии, атриовентрикулярная блокада высокой степени, активные воспалительные заболевания, выраженные электролитные нарушения, психические нарушения); 5) наличие показаний к досрочному прекращению стресс-теста (снижение систолического АД — САД ≥10 мм рт.ст. менее исходного уровня, возникновение симптомов ишемии миокарда и диагностически значимых изменений процессов реполяризации, появление признаков гипоперфузии, боли в икроножных мышцах, увеличение АД ≥250/115 мм рт.ст., тахиаритмии и брадиаритмии, появление БЛНПГ) [10].
 Все пациенты дали письменное информированное согласие на участие в исследовании. Исследование одобрено локальным Этическим комитетом.
Все пациенты дали письменное информированное согласие на участие в исследовании. Исследование одобрено локальным Этическим комитетом.
Включенным в исследование пациентам была проведена оценка следующих клинико-анамнестических и лабораторных показателей: возраст, АГ, САД, диастолическое АД (ДАД), пульсовое давление, индекс массы тела (ИМТ), курение, семейный анамнез раннего развития ИБС (внезапная сердечная смерть или ИМ у родственников первой линии: мужчины моложе 55 лет и женщины моложе 65 лет), липидный состав крови, уровень глюкозы в крови натощак. АД оценивали при измерении в положении сидя в утренние часы. Уровень холестерина липо-протеинов низкой плотности (ЛНП) рассчитывали по формуле Фридвальда. Курильщиком считали пациента, который курил на момент обследования или ранее отказался от курения. Для количественной оценки курения рассчитывали индекс курильщика (количество выкуриваемых сигарет в день × длительность курения (годы) / 20). Для каждого обследованного был определен 10-летний суммарный риск развития заболеваний сердца по шкале SCORE для стран с высоким риском развития ССО.
Нагрузочный тест выполнялся на тредмиле (Burdick T600, Megacart, Siemens) по стандартному протоколу Bruce с отменой препаратов (за 2 периода полувыведения), оказывающих антиангинальный эффект или способных препятствовать нормальному приросту ЧСС при нагрузке. Выполнялся симптом-лимитированный тест — до достижения пациентом одышки и/или общей усталости, препятствующей дальнейшему продолжению нагрузки. Период восстановления начинался с фазы «охлаждения» (постепенное снижение наклона и скорости беговой дорожки) в течение 2 мин. По продолжительности нагрузки рассчитывали уровень максимальной работоспособности в метаболических единицах (METs). Оценивали параметры ЧСС: исходная, максимальная достигнутая, максимальный прирост (разница между максимальной достигнутой и исходной ЧСС), максимальная возрастная ЧСС (220 – возраст, годы), резерв ЧСС (разница между максимальной возрастной и исходной ЧСС). Хронотропную недостаточность в ответ на физическую нагрузку определяли с помощью 2 критериев: 1) неспособность достигнуть 85% расчетной максимальной возрастной ЧСС; 2) неспособность достигнуть 80% резерва ЧСС. Восстановление ЧСС оценивали по разнице между ЧСС на пике нагрузки и ЧСС через 1 и 2 мин после прекращения нагрузки (восстановление ЧСС 1 и 2). АД измеряли исходно в покое и на последней минуте каждой ступени. Определяли прирост САД как разницу между максимальным и исходным САД в процентах от исходного. Восстановление АД оценивали по соотношению показателей САД на 3-й минуте восстановительного периода с САД на 1-й минуте (восстановление САД 3/1). Рассчитывали максимальное двойное произведение (САДмакс×ЧССмакс).
Выраженность атеросклеротических изменений в СА оценивали по данным УЗИ (ультразвуковой сканер Sonoline g60s, Siemens, датчик 7,5 МГц). ТИМ измеряли в продольной плоскости в латеральной проекции по задней стенке сосуда в 3 внечерепных сегментах СА (дистальный отдел общей СА — ОСА, бифуркация, проксимальная часть внутренней СА — ВСА, билатерально). Учитывали среднюю величину 3 измерений ТИМ в ОСА и максимальные значения ТИМ в бифуркации и ВСА.

ТИМ >75-го процентиля не использовали в качестве маркера наличия атеросклероза СА в связи с отсутствием референсных значений ТИМ для российской популяции.
АСБ в СА определяли как локальное утолщение стенки сосуда более чем на 50% по сравнению с окружающими участками или локальное утолщение стенки более чем 1,5 мм с его протрузией в просвет артерии. При наличии АСБ рассчитывали ее площадь в продольной плоскости и в проекции с наилучшей визуализацией бляшки.
 Статистическую обработку данных выполняли с применением пакета статистических программ SAS. Количественные переменные представлены в виде среднего значения и его стандартного отклонения (M±SD), качественные переменные — в виде абсолютного и относительного числа наблюдений. Для сравнения групп использовали критерий t Стьюдента (для количественных переменных) и χ²-тест (для качественных переменных). Оценку зависимости между количественными показателями проводили с помощью пошагового многофакторного регрессионного анализа. Результаты анализа представлены в виде коэффициента регрессии с 95% доверительным интервалом (ДИ). Оценку влияния количественных показателей на качественные осуществляли с помощью многофакторного логистического регрессионного анализа. Выбор параметров для включения в модель производили с помощью однофакторного анализа. Результаты логистического регрессионного анализа представлены в виде отношения шансов (ОШ) с 95% ДИ. Для нахождения точек разделения показателей использовали интегральную площадь под характеристической кривой (ППК). Были рассчитаны чувствительность, специфичность пороговых значений и прогностическая ценность положительного и отрицательного результата теста. Различия считали статистически значимыми при p<0,05.
Статистическую обработку данных выполняли с применением пакета статистических программ SAS. Количественные переменные представлены в виде среднего значения и его стандартного отклонения (M±SD), качественные переменные — в виде абсолютного и относительного числа наблюдений. Для сравнения групп использовали критерий t Стьюдента (для количественных переменных) и χ²-тест (для качественных переменных). Оценку зависимости между количественными показателями проводили с помощью пошагового многофакторного регрессионного анализа. Результаты анализа представлены в виде коэффициента регрессии с 95% доверительным интервалом (ДИ). Оценку влияния количественных показателей на качественные осуществляли с помощью многофакторного логистического регрессионного анализа. Выбор параметров для включения в модель производили с помощью однофакторного анализа. Результаты логистического регрессионного анализа представлены в виде отношения шансов (ОШ) с 95% ДИ. Для нахождения точек разделения показателей использовали интегральную площадь под характеристической кривой (ППК). Были рассчитаны чувствительность, специфичность пороговых значений и прогностическая ценность положительного и отрицательного результата теста. Различия считали статистически значимыми при p<0,05.
Результаты
В исследование были включены 204 пациента (100 женщин и 104 мужчины), средний возраст составил 54,16±8,07 года (от 35 до 73 лет). Основные характеристики группы пациентов представлены в табл. 1
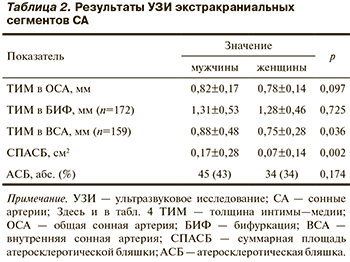
ТИМ в ОСА была измерена у всех пациентов. Ввиду анатомических особенностей измерить ТИМ в бифуркации удалось у 172 (84%) обследованных, в ВСА — у 159 (78%). Наибольшая ТИМ наблюдалась в бифуркации ОСА и составила 1,31±0,53 мм у мужчин и 1,28±0,46 мм у женщин. Средняя ТИМ в ОСА достигала 0,82±0,17 мм у мужчин и 0,78±0,14 мм у женщин, в ВСА — 0,88±0,48 и 0,75±0,28 мм соответственно. АСБ обнаружена у 79 (39%) больных (43% мужчин и 34% женщин). Средняя суммарная площадь АСБ (СПАСБ) составила 0,17±0,28 см² у мужчин и 0,07±0,14 см² у женщин. Были выявлены достоверные различия по ТИМ в ВСА и по СПАСБ между мужчинами и женщинами. Результаты УЗИ внечерепных сегментов СА представлены в табл. 2.
Всем пациентам, включенным в исследование, выполнен электрокардиографический тест с физической нагрузкой. Результаты обследования представлены в табл. 3.

Показатели стресс-теста и ТИМ СА. Для оценки зависимости ТИМ и СПАСБ от параметров стресс-теста выполнен многофакторный регрессионный анализ с пошаговым отбором наиболее значимых показателей. По результатам анализа (табл. 4) резерв ЧСС являлся предиктором ТИМ во всех сегментах СА и СПАСБ. Уменьшение резерва ЧСС ассоциировалось с большими величинами ТИМ и СПАСБ.
На показатели ТИМ в ОСА также влияли прирост ЧСС, максимальное САД и двойное произведение. Предикторами ТИМ, а также СПАСБ в бифуркации были исходные ЧСС и САД, восстановление ЧСС 2, максимальное САД и прирост САД. ТИМ ВСА была взаимосвязана с САД в покое, приростом САД и физической работоспособностью.
Показатели стресс-теста и АСБ СА. Для оценки взаимосвязи параметров стресс-теста с наличием АСБ в СА был выполнен логистический регрессионный анализ.
С наличием АСБ статистически значимо были связаны следующие показатели: максимальная ЧСС (ОШ 0,97 при 95% ДИ от 0,95 до 0,99; р=0,02), восстановление ЧСС 2 (ОШ 0,96 при 95% ДИ от 0,93 до 0,99; р=0,003) и прирост САД (ОШ 1,05 при 95% ДИ от 1,02 до 1,07; р=0,0004).
С помощью расчета интегральной ППК определены пороговые значения восстановления ЧСС 2 и прироста САД, обеспечивающие наилучшее разделение пациентов по наличию АСБ в СА. Для восстановления ЧСС 2 таковым оказалось значение ≤42 уд/мин (ППК=0,575; p=0,02), для прироста САД — показатель >42% (ППК=0,614; p=0,002).
Данные по прогностической способности этих показателей в отношении наличия АСБ представлены в табл. 5 и на рисункею
Обсуждение
Показатели отрицательного ишемического теста и риск развития субклинического атеросклероза
Физическая работоспособность. Среди других показателей нагрузочного теста физическая работоспособность является наиболее сильным независимым предиктором сердечно-сосудистой и общей смертности [9, 11]. Имеются данные о взаимосвязи физической работоспособности с субклиническим атеросклерозом СА. C.D. Lee и соавт. по результатам обследования 9871 здорового мужчины показали, что атеросклероз СА (увеличение ТИМ >1,2 мм и/или наличие АСБ, суживающей просвет на ≥25%) чаще встречается в группе пациентов с низкой толерантностью к физической нагрузке [12]. В нашем исследовании физическая работоспособность являлась предиктором ТИМ ВСА. Уменьшение толерантности к физической нагрузке на 1 METs коррелировало с увеличением ТИМ на 0,07 мм.
Реакция ЧСС на физическую нагрузку. Хронотропная недостаточность и замедленное восстановление ЧСС после нагрузки зависят от множества взаимодействующих факторов (возраст, физическая активность, нейрогуморальная регуляция, применение лекарственных препаратов и др.). Известна корреляция этих показателей с традиционными ФР развития ССО: курение [13], повышенные САД, ДАД, уровень ЛНП и триглицеридов, ИМТ [14]. Хотя показатели реакции ЧСС на физическую нагрузку не являются диагностически значимыми в отношении ишемии миокарда, они могут иметь значение в стратификации риска развития ССО [15, 16]. По данным C.R. Cole и соавт. [17], риск смерти увеличивался при неспособности снизить ЧСС на >12 уд/мин в течение 1-й минуты восстановления.
K. Shetler и соавт. по данным обследования 2193 мужчин показали, что предиктором смерти является неспособность уменьшить ЧСС на ≥22 уд/мин через 2 мин после прекращения нагрузки [18].
Следует отметить, что для восстановления ЧСС четко определенных нормативов не существует. Дело в том, что восстановление ЧСС во многом зависит от протокола нагрузочного теста — наличие фазы «охлаждения», положение пациента в периоде восстановления, время определения ЧСС. Этим можно объяснить различия в пороговых показателях параметра в указанных исследованиях.
Механизмом нарушения реакции ЧСС на физическую нагрузку, вероятно, является вегетативный дисбаланс, который обусловлен снижением чувствительности каротидных барорецепторов за счет атеросклеротических изменений.
В исследовании S.Y. Jae и соавт. [19] выявлена взаимосвязь между хронотропной недостаточностью и атеросклерозом СА (увеличение ТИМ >1,2 мм и/или наличие АСБ, суживающей просвет сосуда на ≥25%) у 8567 здоровых мужчин среднего возраста. Выявленная взаимосвязь оставалась значимой после учета возраста и других согласованных ФР. В другой работе S.Y. Jae и соавт. также изучена взаимосвязь восстановления ЧСС на 2-й минуте восстановительного периода с атеросклерозом СА у 12 712 мужчин. Значения восстановления ЧСС распределили по 4 квартилям. У лиц в нижнем квартиле (<44 уд/мин) атеросклероз СА встречался в 1,5 раза чаще, чем у лиц в верхнем квартиле (>61 уд/мин) [20].
В нашем исследовании наиболее значимыми параметрами в прогнозировании субклинического атеросклероза СА оказались прирост и резерв ЧСС, восстановление ЧСС 2. Уменьшение резерва ЧСС на 1 уд/мин коррелировало с увеличением ТИМ на 0,007 мм в ОСА, 0,015 мм в бифуркации и 0,006 мм в ВСА. При этом суммарная площадь АСБ увеличивалась на 0,005 см². Замедление прироста ЧСС на 1 уд/мин ассоциировалось с увеличением ТИМ на 0,008 мм в ОСА.
Выявлена слабая, но статистически значимая корреляция между восстановлением ЧСС 2 ≤42 уд/мин и наличием АСБ в СА. Чувствительность и специфичность показателя, прогностическая ценность его положительного и отрицательного результата составили 82 и 33%, 44 и 75% соответственно.
Реакция АД на физическую нагрузку. Чрезмерный подъем САД во время нагрузки у лиц с нормальным АД является предиктором развития АГ и ССЗ [21]. По результатам исследования J.A. Laukkanen и соавт. [22], подъем САД ≥230 мм рт.ст. на фоне физической нагрузки у 1731 здорового мужчины среднего возраста ассоциировался с 2,47-кратным увеличением риска развития ИМ. Одной из возможных причин патологической реакции АД у пациентов без клинических симптомов заболевания является ригидность периферических сосудов за счет субклинического атеросклеротического процесса. S.Y. Jae и соавт. продемонстрировали корреляцию подъема САД с атеро-склерозом СА (увеличение ТИМ >1,2 мм и/или наличие АСБ, суживающей просвет сосуда на ≥25%) у 9073 здоровых мужчин. В группе лиц с увеличением уровня САД ≥210 мм рт.ст. во время нагрузки атеросклероз встречался в 2,02 раза чаще [23].
По результатам нашего исследования, прирост САД являлся предиктором ТИМ в бифуркации, ВСА и СПАСБ. Прирост САД на 1% коррелировал с увеличением ТИМ на 0,055 мм в бифуркации и 0,008 мм в ВСА. При этом суммарная площадь АСБ увеличивалась на 0,026 см².
Прирост САД >42% во время нагрузки прогнозировал наличие АСБ в СА с чувствительностью 62% и специфичностью 61%. Прогностическая ценность положительного и отрицательного результата показателя составила 50 и 72% соответственно.
Замедленное восстановление или парадоксальный прирост САД после прекращения нагрузки являются признаком дисфункции левого желудочка и предиктором ССО [21]. S.A. McHam и соавт. изучена взаимосвязь замедленного восстановления САД (соотношение САД на 3-й минуте с САД на 1-й минуте >1) с выраженностью атеросклероза коронарных артерий у 493 пациентов. Взаимосвязь оказалась статистически значимой даже после учета возможных вмешивающих факторов [24]. В нашем исследовании парадоксального подъема САД не зафиксировано. Среднее значение восстановления САД 3/1 составило 0,87. В регрессионных моделях статистически значимых взаимосвязей скорости восстановления САД с ТИМ СА и наличия АСБ не выявлено.
Заключение
Электрокардиографический тест с физической нагрузкой используется для подтверждения диагноза ишемической болезни сердца при клиническом подозрении на это заболевание и не рекомендован в целях скринингового обследования больных. Тем не менее отрицательный в отношении ишемии нагрузочный тест содержит важную прогностическую информацию, которая, как правило, не интерпретируется должным образом.
Прогностическая способность отрицательного электрокардиографического стресс-теста основана на анализе недиагностических в отношении ишемии миокарда параметров, таких как физическая работоспособность, реакция частоты сердечных сокращений и артериального давления на физическую нагрузку. Значению данных показателей в прогнозировании риска развития сердечно-сосудистых осложнений и общей смертности в последние годы уделяется все большее внимание. Известны также результаты исследований, продемонстрировавших корреляцию параметров отрицательного ишемического стресс-теста с атеросклерозом сонных и коронарных артерий. В нашем исследовании продемонстрирована зависимость маркеров выраженности субклинического атеросклероза сонных артерий от показателей стресс-теста у пациентов без симптомов заболевания. Наиболее важными предикторами субклинического атеросклероза были толерантность к физической нагрузке, прирост и резерв частоты сердечных сокращений, восстановление частоты сердечных сокращений 2 и прирост систолического артериального давления. На основании полученных сведений можно сделать вывод, что данные о физической работоспособности и гемодинамические показатели отрицательного стресс-теста могут представлять ценную в клиническом отношении информацию, дополняющую анализ традиционных факторов риска развития сердечно-сосудистых осложнений. Факторами, которые ограничивают использование информации, получаемой в отрицательном ишемическом тесте, являются отсутствие стандартизации и рандомизированных контролируемых исследований, изучавших эффективность параметров стресс-теста, недиагностических в отношении ишемии миокарда, в улучшении прогнозирования сердечно-сосудистых заболеваний и модификации алгоритмов первичной профилактики.



