Инфекционный эндокардит (ИЭ) до настоящего времени остается довольно часто встречающимся угрожающим жизни заболеванием в структуре приобретенных пороков сердца. Ежегодная заболеваемость составляет от 3 до 10 случаев на 100 тыс. населения. Заболевание имеет полиэтиологичную природу и может быть вызвано различными микроорганизмами: не только грамположительной и грамотрицательной флорой, но дрожжевыми и плесневыми грибами, риккетсиями и хламидиями [1—7].
Впервые протезирование аортального клапана (АК) в 1963 г. и митрального клапана (МК) в 1964 г. у больных ИЭ клапанов сердца выполнил A. Wallace. В СССР первыми выполнили успешные операции по поводу ИЭ клапанов сердца Г.М. Соловьев и Г.И. Цукерман.
После первых успешных операций у больных ИЭ клапанов сердца начался новый этап в истории лечения данного заболевания. Этот этап может быть охарактеризован как этап внедрения хирургических методов лечения ИЭ. Он значительно расширил диапазон лечебных мероприятий и позволил врачам не только спасать жизнь, но и восстанавливать трудоспособность больных, прежде считавшихся обреченными.
Целью настоящего исследования явилась оценка результатов хирургического лечения ИЭ различной локализации.
Материал и методы
За период с 1978 по 2013 г. наблюдали 438 пациентов с ИЭ в возрасте от 12 до 74 лет (средний возраст 49,0±9,3 года, мужчин — 69,1%, женщин — 30,9%). Сердечная недостаточность (СН) IV функционального класса (ФК) по классификации Нью-Йоркской ассоциации сердца (NYHA) имелась у 302 (68,9%) пациентов, III ФК — у 101 (23%), II ФК — у 35 (8,1%).

ИЭ возник на фоне исходного ревматического поражения клапанного аппарата сердца у 184 пациентов, из них инфекционное поражение протезированных клапанов – у 37 (42%), врожденные аномалии клапанного аппарата (системные дегенеративные заболевания соединительной ткани, двустворчатый АК) — у 167 (38,1%), без предшествующей патологии — 87 (19,9%).
Активная фаза инфекционного процесса отмечена у 211 (48,1%), ремиссия — у 227 (51,9 %) больных. Внутрисердечное абсцедирование диагностировано у 26 (5,9%) больных.
Положительная гемокультура до операции получена у 66% пациентов (наиболее часто возбудителями ИЭ были различные типы стафилококков — 72%). У 34% пациентов имелась культуро-негативная форма ИЭ.
Непосредственные причины, приведшие к возникновению ИЭ, выявлены только у 58% пациентов. При этом главными причинами в общей структуре были инфекционные заболевания верхних дыхательных путей (26%) и одонтогенный ИЭ (21%).
Обследование больных, поступавших в клинику с подозрением на ИЭ, проводилось по стандартному плану, включавшему клинический, лабораторный и инструментальный методы исследования и, по возможности, исключавшему инвазивные дооперационные исследования.

Показаниями к хирургическому лечению служили прогрессирующая СН (3—4-й стадии по классификации А.Н. Бакулева и Е.А. Дамир [1, 2]), возможность первичного или повторного возникновения эмболического синдрома, перианулярное абсцедирование, отсутствие эффекта от антибиотикотерапии [1, 2].
В активной фазе ИЭ хирургическое вмешательство выполнено 53% пациентов, в стадии ремиссии — 47%.
Изолированное поражение АК отмечено у 202 (46,1%) пациентов, МК — у 149 (34%), трикуспидального клапана (ТК) — у 15 (3,4%), АК и ТК — у 4 (0,9%). Наиболее тяжелую группу составили пациенты с комбинированным поражением двух клапанов — МК и АК — 65 (14,8%) пациентов, а также МК, АК и ТК — 3 (0,7%) пациента.
 Целью хирургического вмешательства было не только восстановление нормальной гемодинамики, но и надежная санация очага внутрисердечной инфекции. Локализация инфекционного процесса и объем операции представлены в табл. 1.
Целью хирургического вмешательства было не только восстановление нормальной гемодинамики, но и надежная санация очага внутрисердечной инфекции. Локализация инфекционного процесса и объем операции представлены в табл. 1.
Статистическую обработку данных исследования проводили с помощью пакета программ Biostat, актуарные кривые отдаленных результатов рассчитывали по методу Anderson. Для сравнения количественных показателей в группах и определения различий между ними использовали критерий Стьюдента. Данные считали достоверными при р<0,05. Для вычисления различий между группами по частоте выявления различных признаков использовали критерий χ2 и точный критерий Фишера с построением четырехпольных таблиц.
Результаты
Общая летальность составила 9,1%. В группе пациентов, оперированных в активной стадии ИЭ, летальность составила 11,2%, в стадии ремиссии — 6,7%. В зависимости от локализации инфекционного процесса летальность составила при поражении АК — 7,9%, МК — 10,1%, МК и АК — 10,7%, ТК — 6,7%.
Отдаленные результаты хирургического лечения больных с клапанным ИЭ прослежены у 332 пациентов, что составляет 75% от числа всех выписанных больных. Сроки наблюдения составили от 1 мес до 25 лет (в среднем 8,9±4,7 года).
Актуарная выживаемость к концу 1-го года составила 83,7%, через 5 лет после операции — 78,6%, через 10 лет — 66,2% (рис. 1).
Ранний рецидив ИЭ (в сроки до 6 мес после операции) выявлен у 37 (11,1%) больных, поздний — у 54 (16,2%).
По поводу раннего рецидива повторно оперированы 30 пациентов, 7 лечились консервативно. Летальность среди повторно оперированных пациентов составила 10% (3 пациента). Из 54 больных с поздним рецидивом ИЭ повторно оперированы 43, летальность составила 6,9% (3 пациента). Консервативную терапию получали 11 пациентов, из которых умерли 4.
Число наблюдений рецидива ИЭ, на наш взгляд, довольно отчетливо характеризует радикальность хирургического вмешательства, адекватность последующего консервативного комплексного лечения.
Наблюдается отчетливое различие по соотношению показаний к повторному хирургическому лечению в зависимости от срока рецидива ИЭ, что отражено в табл. 2.
Среди больных, перенесших рецидив ИЭ, большинство были с имплантированными при первичной операции механическими дисковыми и шаровыми протезами — 36 (49,3%) и 22 (30,1%) соответственно. В группе пациентов с имплантированными двустворчатыми механическими протезами рецидив ИЭ отмечен у 8 (10,9%), а в группе с биологическими протезами и аллографтами — у 6 (8,2%).
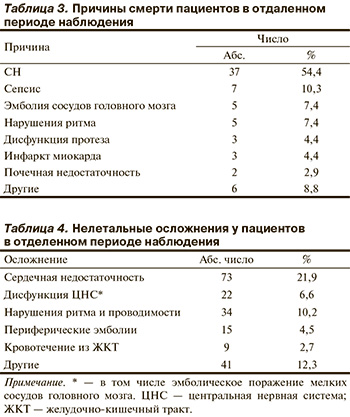
Основные причины смерти перенесших хирургическое лечение ИЭ пациентов в отдаленном периоде наблюдения представлены в табл. 3.
Как представлено в табл. 3, нарастающая СН служит основной причиной летального исхода в отдаленном периоде наблюдения. Причиной СН может быть не только ревматическое поражение миокарда с постепенным снижением его насосной функции, но и токсическое поражение сердечной мышцы (токсический миокардит) при ИЭ.
В группе пациентов, у которых наблюдались нелетальные осложнения, также преобладает СН, обусловливающая необходимость проведения комплексной кардиальной терапии (сердечные гликозиды, диуретики, ингибиторы ангиотензинпревращающего фермента и т.д., табл. 4).
Как отмечалось ранее, СН развивается в основном у больных ревматизмом и обусловливает необходимость постоянной кардиальной терапии. Неврологические нарушения, как правило, имели преходящий характер в виде парезов, снижения чувствительности правой или левой половины тела и на фоне медикаментозной терапии разрешались. Нарушения ритма сердца проявлялись в виде пароксизмов мерцания/трепетания предсердий, перешедших в постоянную форму у 24 (7,2%) пациентов. Эмболические осложнения развивались на фоне нерегулярного или неадекватного приема антикоагулянтов непрямого действия. Желудочно-кишечное кровотечение отмечено у 9 больных на фоне язвенной болезни желудка или двенадцатиперстной кишки, эрозивного гастрита.
Из прочих осложнений следует отметить носовые кровотечения, возникающие нередко, особенно при передозировке антикоагулянтов непрямого действия. Чаще всего с такими кровотечениями удается справиться амбулаторно при помощи передней тампонады носового хода с уменьшением дозы антикоагулянта.
Выявлена зависимость выживаемости пациентов в отдаленные сроки после операции от локализации и выраженности поражения сердца инфекционно-воспалительным процессом.

Согласно приведенным на рис. 2 данным, наименьшая выживаемость отмечалась в группе пациентов с инфекционным поражением МК и АК: через 5 лет после операции — 66,3%, через 10 лет — 52,7%. Это, несомненно, обусловлено наличием двух протезов клапанов и, соответственно, исходной тяжестью состояния пациентов, бóльшим риском рецидива ИЭ и большей вероятностью развития характерных для механических протезов осложнений (дисфункция протеза, тромбоз, тромбоэмболический синдром и т.д.).
Наилучшими оказались результаты в группах с изолированным поражением инфекционным процессом МК или АК.
Так, при поражении МК 5-летняя выживаемость больных составила 85,3%, 10-летняя — 77,1%. При поражении АК через 5 и 10 лет после операции выживаемость составила 86 и 83,4% соответственно. При ИЭ ТК выживаемость составила через 5 лет 74,3%, через 10 лет — 69,4%.
Следует отметить, что имеются совершенно отчетливые различия между отдаленными результатами хирургического лечения пациентов с первичным и вторичным ИЭ.
Как свидетельствует сравнительное изучение функциональных результатов хирургического лечения ИЭ, наилучшими они оказались при вмешательствах по поводу первичной его формы (рис. 3). Все пациенты этой группы в различные сроки после вмешательства переходили в более высокий ФК и в отдаленном периоде наблюдения, как правило, не имели признаков декомпенсации кровообращения.
Через 1 год после операции выживаемость составила 87,2%, через 5 лет — 81,3%, через 10 — 76,6%. В группе пациентов с первичным ИЭ через 1 год после операции выживаемость составила 94,5%, через 5 лет — 87%, через 10 лет — 85,5%. В группе пациентов с вторичным ИЭ выживаемость через 1 год, 5 и 10 лет наблюдения составила 86,3%, 77,4 и 70,6% соответственно.

Зависимость рецидива ИЭ от активности инфекционного процесса на момент хирургического лечения показана на рис. 4.
Вероятность рецидива ИЭ у пациентов, оперированных в период ремиссии инфекционного процесса, в течение 1-го года после операции составляет 7%. При этом частота рецидива ИЭ в группе больных, оперированных в активной стадии ИЭ, в течение 1-го года после вмешательства, составила 17,2%. В течение 5-летнего наблюдения в группе пациентов, оперированных в стадии ремиссии, рецидив ИЭ отсутствовал у 77,2%, а в группе пациентов, оперированных в активной стадии ИЭ, — у 71,4%.
Количество рецидивов у больных, оперированных в активной стадии инфекционного процесса и в стадии ремиссии, через 5 лет после операции уменьшается и различия между этими двумя группами становятся недостоверными (р>0,05).
Обсуждение
При изучении отдаленных результатов, прежде всего, исходили из оценки степени выраженности симптомов, связанных с собственно ИЭ, восстановления кровообращения и трудоспособности пациентов. Отсутствие рецидива ИЭ довольно отчетливо характеризует радикальность хирургического вмешательства, надежность санации очагов внутрисердечной инфекции, а также преемственность последующего консервативного комплексного ведения пациента и адекватность профилактики рецидива ИЭ.
По данным T.E. David и соавт. (2007), отсутствие рецидива ИЭ в течение 15 лет наблюдения после операции составило 86%, а повторных операций — 70% [8]. S.P. Kaiser и соавт. (2007) сообщают о необходимости повторных вмешательств у 17% пациентов с ИЭ в отдаленном периоде наблюдения. В нашем исследовании отсутствие рецидива ИЭ в течение 10 лет наблюдения составляет 71%, а выживаемость — 66% [9].
По данным литературы, общая отдаленная выживаемость пациентов с клапанным ИЭ в сроки 10 и 15 лет после операции составляет 56—59% и 42—44% соответственно [5, 8, 10]. Отдаленная выживаемость больных с протезным ИЭ в течение 5 лет после повторной операции составляет 82% [11], в течение 10 лет — 25% [8].
Некоторые исследователи ИЭ утверждают, что выполненные клапаносберегающие вмешательства обеспечивают высокую выживаемость и отсутствие рецидива ИЭ. Так, R. Zegdi и соавт. (2005) сообщают, что 10-летняя выживаемость и отсутствие повторной операции у пациентов, перенесших реконструкцию МК, составили 80 и 91% соответственно, причем у 92% у больных не было значимой митральной регургитации [12]. Выживаемость при реконструкции АК в течение 5 лет наблюдения составила 88%, а отсутствие повторной операции — 87%, в то время как отсутствие аортальной регургитации — лишь 66% [13]. В настоящее время прослеживается отчетливая тенденция к выполнению, по возможности, клапаносберегающих вмешательств при ИЭ, однако мы располагаем лишь единичными наблюдениями подобной реконструкции клапанного аппарата, поскольку почти все пациенты поступали в стационар с признаками выраженной и необратимой деструкции клапанного аппарата сердца.

После наших вмешательств трудоспособность восстановлена у 40,4% пациентов [14]. Это связано со своевременно выполненным первичным вмешательством, преемственностью последующего ведения больного: кардиохирургическое отделение, курс санаторной реабилитации, консультативно-поликлиническое наблюдение. Таким образом, пациенты, прошедшие курс реабилитационных мероприятий, находящиеся на диспансерном наблюдении, готовы к продолжению трудовой деятельности при минимальной медикаментозной поддержке и соблюдении подобранного уровня физической активности.
Некоторые авторы [12, 15] подчеркивают высокий ФК (по NYHA) пациентов в отдаленном периоде наблюдения в случае выполнения реконструкции клапанного аппарата сердца при его поражении инфекционным процессом. Так, по данным R. Zegdi и соавт. (2005), через 10 лет после операции у 96% пациентов имеются I и II ФК [12].
Показаниями к повторному хирургическому лечению ИЭ служат [1, 2, 4, 14, 16] дисфункция протеза, неконтролируемая инфекция, угроза развития эмболии (или повторной эмболии), внутрисердечное абсцедирование.
Следует отметить, что в зависимости от срока рецидива ИЭ изменяются показания к повторному вмешательству. Так, в нашем исследовании наиболее частым показанием к повторному вмешательству при позднем рецидиве ИЭ была прогрессирующая СН, обусловленная поражением протеза клапана и его последующей дисфункцией. При этом в группе пациентов с ранним рецидивом ИЭ наиболее частым показанием к повторной операции являлась неэффективная антибактериальная терапия, что было связано с высоковирулентным характером микрофлоры или ее устойчивостью к широкому спектру антибактериальных препаратов. Смешанные показания (2 и более) в наблюдениях с ранним и поздним рецидивами ИЭ по частоте находятся на втором месте. Наиболее редкими показаниями к повторному хирургическому лечению в случае рецидива ИЭ являются внутрисердечное абсцедирование и эмболический синдром, причем последний не встречался при раннем рецидиве ИЭ, что может быть обусловлено наиболее ранним повторным хирургическим вмешательством до развития этого грозного осложнения.
По данным И.И. Шевелева (2013), наиболее частыми показаниями к хирургическому лечению ИЭ являются СН (57,6%), некупирующийся септический процесс (30,6%), тромбоэмболический синдром (18,8%), острое разрушение клапанов сердца (5,9%) [2]. C. Rostagno и соавт. (2011) считают, что основными показаниями к хирургическому лечению ИЭ были острая регургитация на клапанном аппарате (48% оперированных пациентов), большие (более 10 мм) вегетации с эмболическим синдромом (24%), неэффективность антибактериальной терапии (8,7%) и различные сочетания этих показаний [17].
Многие исследователи ИЭ не находят статистически значимой зависимости частоты рецидива от типа имплантированного протеза [2, 4, 14, 16], что соответствует и нашим наблюдениям.
По данным литературы, наиболее частыми причинами послеоперационных осложнений и летальных исходов в отдаленном периоде наблюдения являются нарастающая СН и рецидивы инфекции [1, 2, 10, 17, 18–21].
В нашем исследовании нарастающая СН также послужила причиной летального исхода у 54% пациентов, а у 22% пациентов СН обусловила необходимость постоянной комплексной кардиальной терапии.
В настоящее время следует признать, что к числу наиболее недооцененных аспектов относится оценка миокардиальной функции при ИЭ. В структуре летальных и нелетальных осложнений она занимает основное место, что свидетельствует о недооценке исходного состояния миокарда. По данным литературы, становится очевидным, что до настоящего времени не установлены четкие причины миокардиальной недостаточности при ИЭ.
Важной особенностью ИЭ является вовлечение миокарда в патологический процесс. При макроскопическом изучении препаратов находят некротическое поражение миокарда разной величины и протяженности в 3—9% случаев, фиброзные изменения — в 4—64% случаев, папиллярные некрозы — в 58%. В сосудах миокарда обнаруживают эндо- и периваскулиты, дистрофию эндотелиальных клеток капилляров. В крупных коронарных артериях нередко находят эмболы, формирующие микотические аневризмы при грибковой инфекции [19].
В свете этих находок неудивительным является обнаружение у отдельной группы пациентов зон гипо- и нормокинезии при выраженных степенях регургитации, вариации фракции изгнания от 50 до 56% (т.е. не чрезмерных, характерных для выраженной перегрузки объемом левого желудочка сердца) [14, 18].
В отдаленном периоде наблюдения прослеживается зависимость результатов от локализации инфекционного процесса. По данным A.M. Sheikh и соавт. (2009), отдаленная выживаемость больных, оперированных по поводу активного ИЭ МК, через 5, 7 и 10 лет наблюдения составляет 73, 68 и 58% соответственно, 5-летняя выживаемость после вмешательства по поводу ИЭ АК составляет 88% при его реконструкции и 65% при его протезировании [10].
При реконструктивном вмешательстве на МК 10-летняя выживаемость также остается высокой — около 80% [12, 15].
Зарубежные исследователи ИЭ, как правило, не выделяют первичный или вторичный характер инфекционного поражения клапанного аппарата сердца, а подразделяют ИЭ на нативный и протезный. Однако отечественные авторы проводят четкую дифференциацию между этими формами ИЭ [1, 2, 14, 18, 20, 21].
Наиболее быстрая компенсация кровообращения и хорошие общие отделенные результаты достигнуты у пациентов, оперированных по поводу первичного ИЭ. Уже в течение 1-го месяца после операции у больных этой группы отмечалось значительное улучшение самочувствия с явной регрессией остаточных явлений различных осложнений ИЭ. Как показывает дальнейший анализ отдаленных результатов хирургического лечения первичного ИЭ, через 1 год после вмешательства они были одинаково хорошими у всех больных, независимо от вида возбудителя, формы клинического течения, вида пораженного клапана и стадии заболевания.
У больных, оперированных по поводу ИЭ на ревматически измененных клапанах, отдаленные результаты оказались хуже, что связано с периодически развивающейся активностью ревматического процесса, а также наличием у большинства из них довольно выраженных дистрофических изменений миокарда и других внутренних органов, обусловленных длительным существованием до операции порока сердца и хронической недостаточностью кровообращения.
Заключение
Таким образом, современные методы комплексного лечения инфекционного эндокардита и меры профилактики его рецидива позволяют бороться не только за сохранение жизни больного, но и за восстановление его физической активности. Восстановление трудоспособности оперированных больных свидетельствует об эффективности хирургического лечения инфекционного эндокардита, а реабилитация и диспансерное наблюдение значительно повышают эту эффективность, улучшая качество жизни пациентов в отдаленном периоде наблюдения.



