К числу основных факторов риска (ФР) развития коронарного атеросклероза относится анамнез ранней (проявившейся в возрасте ≤55 лет у мужчин или ≤65 лет у женщин) ишемической болезни сердца (ИБС) у родственников I степени родства (родители, родные братья и сестры) [1]. Этот ФР во многих случаях позволяет выделять из общей выборки группу, в которой следует искать модифицируемые ФР с целью их коррекции [1, 2]. Одним из таких факторов, точнее риск-состояний, является сахарный диабет (СД) 2-го типа [1—3], его распространенность растет с возрастом у лиц обоих полов, достигая максимума (10—20%) после 60 лет [4]. Поэтому объектом первичной профилактики СД 2-го типа (и, вероятно, ИБС) должны быть, прежде всего, лица более молодого возраста c повышенным риском его возникновения, в частности, имеющие предиабет — ПреСД: нарушение гликемии натощак (НГН) и/или нарушение толерантности к глюкозе (НТГ) [4]. Целью этой работы был поиск собственных и родительских предикторов ПреСД у детей (младшей и старшей возрастных групп) лиц с ранней ИБС.
Материалы и методы
В рамках программы изучения ФР развития коронарного атеросклероза в семьях лиц с ранней ИБС мы обследовали членов 303 семей: пробандовI (n=285; 69,4% мужчин; 79,2% после инфаркта миокарда) с ранней ИБС, их супруговII (n=216; 17,6% мужчин, у 4,23% выявлена явная ИБС) и родных детей пробандов (n=395; 55,2% лиц мужского пола без явной ИБС) в возрасте 32—67, 28—67 и 5—38 лет соответственно.
Анализ проводили отдельно в 2 группах детей: 5—17 лет (n=149, 92 из 149 мальчиков), 18—38 лет (n=246, 126 из 246 мужчин) и в 3 наборах предикторов: собственном (n=399), пробанда-родителя (n=285) и супруга-родителя (n=216).
Детей младшей возрастной группы, пробанд-родитель которых имел ПреСД, было 40, СД — 20; супруг-родитель — 20 и 2 соответственно. Детей 18—38 лет, пробанд-родитель которых имел ПреСД, было 80, СД — 44; супруг-родитель — 32 и 7 соответственно.
Кроме того, для сравнения долей лиц с ПреСД среди детей пробандов и в выборках общей популяции (по некоторым данным литературы) были сформированы 2 группы детей пробандов: в возрасте 12—19 лет (n=128; 62,5% мальчики) и 20—38 лет (n=217; 51% мужчины).
Дети (4 из 399) родителей с СД в анализ не включались.
Определяемые параметры и критерии их оценки. Регистрировали следующие характеристики: массу тела при рождении, длительность грудного кормления, употребление алкоголя, статус курения табака, рост, индекс массы тела (ИМТ), окружность талии (ОТ), частоту сердечных сокращений (ЧСС), систолическое и диастолическое артериальное давление (САД и ДАД), уровни общего холестерина (ХС), ХС липопротеинов высокой (ЛВП), низкой (ЛНП) плотности, триглицеридов (ТГ) в крови, гликемию сыворотки натощак и после пероральной нагрузки глюкозой. Регистрировали также наличие предгипертонии/артериальной гипертонии (ПреАГ/АГ) [5—6] и метаболического синдрома (МС) у лиц в возрасте 10—15 лет [7] и ≥16 лет [8] с учетом возраста, пола и приема лекарственных препаратов. Кроме того, у родителей учитывали уровень образования и использование пероральных контрацептивов.
Сведения о массе тела при рождении, длительности грудного кормления, курении, употреблении алкоголя, уровне образования и использовании пероральных контрацептивов получали при персональном опросе.
В группе детей 5—17 лет сведения о кормлении материнским молоком отсутствовали у 12 из 149 человек.
Признаком НГН считали уровень глюкозы в сыворотке крови натощак 5,55—6,99 ммоль/л (100—125 мг/дл) [9]. Толерантность к глюкозе оценивали с помощью перорального теста на толерантность к глюкозе (ПТТГ), выполнявшегося в соответствии с рекомендациями ВОЗ [10], исследование проводилось только у пробандов и их родных детей. Признаком НТГ считали уровень глюкозы в сыворотке крови 7,8—11,0 ммоль/л (140—199 мг/дл) спустя 2 ч после ПТТГ [9]. Критерии СД были следующими: 1) базальный ≥7,0 ммоль/л (126 мг/дл) и/или поспрандиальный ≥11,1 ммоль/л (200 мг/дл) уровень глюкозы в сыворотке крови спустя 2 ч после ПТТГ [9]; 2) диагноз СД по данным выписного эпикриза; 3) указания на лечение СД. Диагноз СД устанавливали при наличии 1 критерия, если базальный и/или постпрандиальный уровень глюкозы в сыворотке крови соответствовал отрезной точке СД) [9], в остальных случаях — при наличии двух (диагноз + лечение СД).
Остальные методы обследования изложены нами ранее [11—16].
Статистический анализ. До оценки связей между ПреСД и другими характеристиками в целях уменьшения вариабельности и подавления влияния возможных экстремальных значений (выбросов) проведено симметризованное цензурирование непрерывных переменных. У детей пробандов НГН и НТГ объединены и обозначены как ПреСД, дети с СД из этого анализа исключены. Предикторы ПреСД отбирали с поправкой на пол, возраст и прием лекарственных препаратов (дополнительно для ЧСС на прием β-адреноблокаторов, для ТГ, ХС ЛВП и ХС ЛНП на медикаментозное лечение дислипидемий) отдельно в 2 выборках детей: 5—17 лет (n=149) и 18—38 лет (n=246) и в 3 наборах предикторов: собственном (n=395), пробанда-родителя (n=285) и супруга-родителя (n=216). Вначале выполнен бинарный логистический однофакторный регрессионный анализ. Затем полученный в ходе однофакторной регрессии набор предикторов (при р<0,1) был включен в пошаговую регрессионную модель (включения и исключения) для идентификации независимых предикторов ПреСД.
Результаты
Дети (пробандов) в возрасте 5—17 лет. Базальный уровень глюкозы в сыворотке крови находился в диапазоне от 3,60 до 6,60 ммоль/л (4,89±0,60 ммоль/л; медиана 4,93 ммоль/л).
У 22 (14,8% [16 из 22 мужского пола]) найден ПреСД (НГН; 20 из 149 и/или (НТГ; 2 из 117). Доля детей с ПреСД возрасте 12—19 лет составила 12,5% (16 из 128).
При однофакторном анализе (p<0,1) ПреСД с собственным и родительским возрастом или полом не связан.
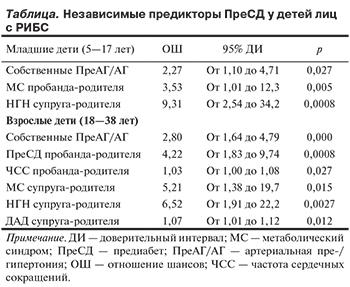
Характеристики, ассоциированные (p<0,1) с ПреСД в однофакторном анализе (ИМТ, ОТ, ДАД, ПреАГ/АГ этих детей; более низкое употребление алкоголя и МС пробанда; НГН супруга), включены (кроме ДАД детей) в пошаговую процедуру. Факторами, независимо связанными с ПреСД, оказались ПреАГ/АГ этих детей (отношение шансов — ОШ 2,27 при 95% доверительном интервале — ДИ от 1,10 до 4,71; р=0,027), МС пробанда-родителя (ОШ 3,53 при 95% ДИ от 1,01 до 12,3; р=0,005) и НГН супруга-родителя (ОШ 9,31 при 95% ДИ от 2,54 до 34,2; р=0,0008) (см. таблицу).
Дети (пробандов) в возрасте 18—38 лет. Уровень глюкозы в сыворотке крови натощак был в диапазоне от 3,60 до 6,97 ммоль/л (4,90±0,61ммоль/л; медиана 4,82 ммоль/л). ПреСД выявлен у 33 человек (14,1%; 22 из 33 мужчины). Доля лиц с ПреСД в возрасте 20—38 лет составила 15,2% (33 из 217).
 При однофакторном анализе ПреСД статистически значимо ассоциирован с собственным возрастом (ОШ 1,15 при 95% ДИ от 1,06 до 1,24; р=0,001) и мужским полом (ОШ 2,72 при 95% ДИ от 1,24 до 5,97; р=0,013).
При однофакторном анализе ПреСД статистически значимо ассоциирован с собственным возрастом (ОШ 1,15 при 95% ДИ от 1,06 до 1,24; р=0,001) и мужским полом (ОШ 2,72 при 95% ДИ от 1,24 до 5,97; р=0,013).
Другими характеристиками, ассоциированными (р<0,1) с ПреСД в однофакторном анализе, оказались собственные ОТ, САД, ДАД, ТГ, ПреАГ/АГ; ПреСД и ЧСС пробанда; ОТ, САД, ДАД, НГН и базальный уровень глюкозы в сыворотке крови супруга.
Набор собственных, а затем характеристик пробанда включен в пошаговую процедуру, с ПреСД, независимо ассоциировались только ПреАГ/АГ этих детей (ОШ 2,80 при 95% ДИ от 1,64 до 4,79; р=0,0002]); ПреСД (ОШ 4,22 при 95% ДИ от 1,83 до 9,74; р=0,0008) и более высокая ЧСС (ОШ 1,03 при 95% ДИ от 1,00 до 1,08; р=0,027) пробанда-родителя.
Затем в пошаговую процедуру включены ИМТ и МС супруга, ПреСД независимо ассоциировался только с МС (ОШ 5,21 при 95% ДИ от 1,38 до 19,7; р=0,015) супруга. При замене в этой процедуре МС на его компоненты — ОТ, САД, ДАД, НГН — предикторами ПреСД оказались НГН (ОШ 6,52 при 95% ДИ от 1,91 до 22,2; р=0,0027) и более высокие показатели ДАД (ОШ 1,07 при 95% ДИ от 1,01 до 1,12; р=0,012) супруга-родителя.
Таким образом, факторами, независимо ассоциированными с ПреСД, оказались ПреАГ/АГ этих детей; ПреСД и более высокая ЧСС пробанда-родителя; а также МС (НГН и более высокие уровни ДАД) супруга-родителя (см. таблицу).
Обсуждение
Согласно недавним документам Ассоциации диабета США (ADA), а также Европейского общества кардиологов (ESC) и Ассоциации по исследованию диабета (EASD), распространенность СД (в 90—95% случаев — СД 2-го типа) продолжает расти [9, 17]. В клинических рекомендациях Российской ассоциации эндокринологов (РАЭ) (2015), высокие темпы роста заболеваемости СД отмечаются и в России [18]. По данным, полученным в США, растет распространенность СД среди детей и подростков [19].
Продолжающийся рост заболеваемости СД 2-го типа повышает актуальность его первичной профилактики. Как зарубежные [9, 17], так и отечественные [18] эксперты признают существование лиц с повышенным риском возникновения СД 2-го типа. По мнению экспертов ESC/EASD, это лица: 1) с анамнезом СД во время беременности; 2) с инсулинорезистентностью с эугликемией; 3) с НГН; 4) с НТГ [17]. В документе РАЭ этот перечень шире, и, в частности, включает сердечно-сосудистое заболевание (ССЗ) [18].
Нарушения метаболизма глюкозы — НГН и/или НТГ — часто называют предиабетом (ПреСД) и рассматривают как переходное состояние от нормогликемии к СД 2-го типа [17]. Причем ПреСД признается ФР развития как СД, так и ССЗ [9].
В докладе Международного общества по диабету у детей и подростков (ISPAD) [20] представлены те же диагностические критерии СД и НТГ, что и у взрослых [9, 10, 17]. Для диагностики СД эксперты ISPAD допускают использование гликированного гемоглобина (HbA1c), ссылаясь на специальный доклад ВОЗ [21]. Однако отрезные точки уровня HbA1c для диагностики НГН эксперты ISPAD не приводят [20]. В докладе ADA также отсутствуют отрезные точки уровня HbA1c для диагностики НГН [9]. Определение НГН по уровню базальной гликемии у экспертов ISPAD [20] и ADA [9] общее (5,55—7,0 ммоль/л), что несколько отличается от критериев НГН других известных обществ (6,1—7,0 ммоль/л) [10, 17].
По мнению экспертов ADA, диагностику (скрининговое обследование) ПреСД/СД 2-го типа в отсутствие симптомов нужно проводить лишь при наличии избыточной массы тела и дополнительных ФР развития ПреСД/СД 2-го типа (ИМТ ≥25 кг/м2 + ≥1 ФР у взрослых; ИМТ ≥85-го скорректированного по возрасту и полу процентиля + ≥2 ФР у лиц ≤18 лет [9]. В документе РАЭ указано, что это скрининговое обследование должно проводиться у любого взрослого с ИМТ ≥25 кг/м2 и ≥1 ФР или у лиц старше 45 лет (даже с нормальным ИМТ и без ФР) [18].
Хотя скрининговое обследование лиц без симптомов представляется целесообразным, строго спланированные клинические исследования, доказывающие его эффективность, отсутствуют [9]. Эффективность первичной профилактики СД 2-го типа главным образом продемонстрирована при НТГ, а не при изолированной НГН, выявленной с помощью измерения базальной гликемии или HbA1c [22].
Было проведено скрининговое ПреСД и СД пробандов, их супругов и детей, используя оценку гликемии натощак и после ПТТГ, а не оценку уровня HbA1c. Согласно данным исследования NHANES, отрезная точка уровня HbA1c ≥6,5% выявляет на 30% меньше лиц с СД, чем отрезная точка гликемии натощак ≥7,0 ммоль/л [23].
У детей 5–17 лет мы применили рекомендованные экспертами ADA/ISPAD отрезные точки гипергликемии (натощак и после ПТТГ), доля имеющих ПреСД составила 14,7%. Нам не удалось найти отечественных исследований, в которых бы использовались те же отрезные точки у детей и подростков. Поэтому для сравнения применены данные NHANES (США) [24]. В выборке общей популяции (2689 человек в возрасте 12—19 лет) распространенность ПреСД составила 16,1% (НГН — 13,1%; НТГ — 3,4%) [24]. В нашей группе детей лиц с РИБС того же возраста (n=128) доля ПреСД составила 12,5%. Таким образом, частота обнаружения ПреСД у детей лиц с РИБС была меньше распространенности ПреСД среди детей и подростков того же возраста в выборке общей популяции США.
Согласно данным NHANES, распространенность ПреСД была в 2,4 раза выше среди мальчиков, чем среди девочек; в 2,6 раза выше у подростков с повышенным ИМТ, чем с нормальным; в 2,7 раза выше у лиц с ≥2 ФР развития ССЗ и метаболических нарушений, чем без таковых; в 4 раза выше у лиц с гиперинсулинемией, чем без нее. Однако ни повышенный ИМТ, ни число ФР развития ССЗ и метаболических нарушений не были статистически значимо ассоциированы с ПреСД после поправки на гиперинсулинемию, которая оказалась независимо ассоциированной с ПреСД [24]. Наши результаты в целом соответствуют этим данным. Большинство (16 из 22) лиц с ПреСД составили мальчики. ПреСД ассоциировался с собственными компонентами МС, в основе которого, согласно общепринятым представлениям, лежит пониженная чувствительность тканей к инсулину.
ПреСД у детей в возрасте 5—17 лет независимо и сильно ассоциировался с НГН супруга-родителя, которое повышало вероятность обнаружения ПреСД более чем в 9 раз.
Полученный результат соответствует данным литературы. Хотя для СД 2-го типа не найдено специфического гена [25], агрегация СД 2-го типа у кровных родственников [26], высокое сходство показателей заболеваемости СД 2-го типа у близнецов указывают, что в этиологии СД 2-го типа имеется выраженный генетический компонент. В частности, опубликованы данные проспективного генетического исследования с участием 1766 близнецов, в котором в течение 6 лет изучались показатели устойчивости гликемии (базальной и после ПТТГ) и появления ПреСД, начиная с возраста 6—20 лет. Лица, у которых уровень глюкозы в крови находился в верхнем терциле, имели тенденцию к более высокому риску развития ПреСД, чем лица, у которых уровень глюкозы в крови находился в нижнем терциле. Генетические факторы объясняли 43 и 41% вариации базальной гликемии и 72 и 47% НТГ для лиц мужского и женского пола соответственно; факторы окружающей среды вносили существенный вклад в показатели постпрандиальной (спустя 2 ч после ПТТГ) гликемии и НТГ. ПреСД чаще развивался у лиц мужского пола. Показатели базальной гликемии в большей степени определялись генетическими факторами, постпрандиальной — факторами окружающей среды [27].
Данные о том, что у ребенка будет выше вероятность развития СД 2-го типа с больной СД матерью, а не отцом, носят противоречивый характер. В одних работах показано преимущество передачи заболевания от матери [28, 29], в других нет [26, 30].
Другим независимым предиктором ПреСД был МС пробанда, который повышал вероятность обнаружения ПреСД в 3,5 раза. Однако ни один из компонентов МС пробанда самостоятельно не был ассоциирован (p<0,1) с ПреСД детей. С практической точки зрения это в очередной раз подчеркивает важность диагностики именно МС, не ограничиваясь только констатацией наличия его компонентов.
Собственным независимым предиктором ПреСД (как и у взрослых детей) у детей 5—17 лет оказались только ПреАГ/АГ, что соответствует представлениям о кластеризации компонентов МС [7, 8].
У лиц в возрасте ≥18 лет мы использовали отрезные точки гипергликемии, рекомендованные ADA. При этом у взрослых (18–38 лет) детей лиц с ранней ИБС доля имеющих ПреСД составила 14,1%. В возрастной группе 20—38 лет, выделенной для сравнения с данными исследований, проведенных в США, доля ПреСД составила 15,2% (33 из 217). Обе эти цифры оказались меньше распространенности ПреСД/СД в выборке общей популяции США в возрасте 20—39 лет (17,9%), оцененной с использованием ПТТГ и критериев ADA [32]. Отчасти это соотношение, как и сходное соотношение в младшей возрастной группе, можно рассматривать как свидетельство отсутствия ассоциации родительской РИБС с увеличением риска возникновения ПреСД у детей разного возраста. Однако не исключено, что это лишь отражение большей распространенности ПреСД в США.
ПреСД у детей 18—38 лет был ассоциирован с собственным возрастом (риск повышался на 15% после каждого года жизни) и мужским полом (ОШ для мужчин по сравнению с женщинами 2,72). Это соответствует данным литературы. В упомянутом исследовании NHANES распространенность ПреСД в возрасте 12—19, 20—39, 40—59, 60—74 и ≥75 лет составила 16, 17,9, 34,6, 36,8 и 46,7%; у лиц мужского пола в возрасте ≥12 и ≥20 лет — 34 и 36%, женского — 21,6 и 23,4% соответственно [24].
Родительским фактором, независимо связанным с ПреСД взрослых детей, был МС супруга-родителя пробанда (обычно матери), который более чем в 5 раз повышал шансы взрослых детей иметь ПреСД. Дальнейший анализ показал, что эта ассоциация обусловлена НГН и более высокими уровнями диастолического АД этого супруга.
Семейная агрегация также выявлена и с другим родителем: наличие ПреСД у пробанда повышало вероятность обнаружения ПреСД у этих детей более чем в 4 раза. Полученные факты, свидетельствующие о родительской (прежде всего материнской) передаче ПреСД уже в раннем возрасте, участие в передаче ПреСД обоих родителей, безусловно, заслуживают внимания. В этом контексте интересны данные Фрамингемского исследования, в котором изучались ассоциации ПреСД и СД 2-го типа с родительским СД 2-го типа в выборке общей популяции (2527 человек в возрасте 26—82 лет из 1303 ядерных семей). По сравнению с лицами, родитель которых не имел СД, ОШ детей иметь СД 2-го типа или ПреСД с СД матери составило 3,4 (при 95% ДИ от 2,3 до 4,9) и 2,7 (при 95% ДИ от 2,0 до 3,7) соответственно; с СД отца — 3,5 (при 95% ДИ от 2,3 до 5,2) и 1,7 (при 95% ДИ от 1,2 до 2,4), соответственно; с СД матери и отца — 6,1 (при 95% ДИ от 2,9 до 13,0) и 5,2 (при 95% ДИ от 2,6 до 10,5) соответственно. Хотя материнский и отцовский риск развития СД значительно не различался, лица с СД матери (по сравнению с СД отца) имели слабый, но статистически значимый риск иметь ПреСД, который составил 1,6 (при 95% ДИ от 1,1 до 2,4). Лица, у матери которых СД проявился в возрасте <50 лет, имели наиболее высокий риск развития СД — 9,7 (при 95% ДИ от 4,3 до 22,0) и ПреСД — 9,0 (при 95% ДИ от 4,2 до 19,7) [33].
Наконец, ПреСД детей в возрасте 18—38 лет независимо и слабо ассоциировался с ЧСС пробанда. Из данных литературы известно, что МС ассоциируется с увеличением собственной ЧСС покоя, что, по-видимому, обусловлено инсулин-опосредованной активацией симпатической части вегетативной нервной системы [33, 34].
Заключение
Доля лиц с предиабетом среди младших и взрослых детей лиц с ранней ишемической болезнью сердца не превышала распространенность этого состояния в выборках общей популяции того же возраста. Однако надо учитывать, что для сравнения использованы данные о выборке общей популяции, полученные в США, где, как известно, распространенность нарушений углеводного обмена очень велика.
Предиабет у детей обеих возрастных групп независимо ассоциировался с предгипертонией/артериальной гипертонией. Это указывает на необходимость более тщательного контроля гликемии у лиц со стойко повышенным артериальным давлением.
Другими независимыми предикторами предиабета оказались только родительские характеристики, прежде всего, метаболический синдром. Связь предиабета с метаболическим синдромом обоих родителей подчеркивает необходимость обследования супруга-родителя (обычно матери) и вовлечения в профилактические мероприятия всей семьи пробанда. Дальнейший анализ показал, что предиабет в младшей возрастной группе был ассоциирован с метаболическим синдромом пробанда-родителя, но не его компонентами; тогда как в старшей — как с метаболическим синдромом, так и нарушением гликемии натощак и более высокими уровнями диастолического артериального давления супруга-родителя. С одной стороны, это подчеркивает важность диагностики у лиц, страдающих ранней ишемической болезнью сердца, именно метаболического синдрома, а не только констатации наличия его компонентов. С другой стороны, это указывает на необходимость более тщательного слежения за уровнем гликемии у детей в семьях пациентов с ранней ишемической болезнью сердца, у которых выявлен метаболический синдром. Наконец, ассоциация предиабета с метаболическим синдромом супруга-родителя подчеркивает необходимость обследования этого родителя (большинство — матери), и вовлечения в профилактические мероприятия всей семьи пробанда.
В основе независимых ассоциаций предиабета с родительскими метаболическими характеристиками лежала семейная агрегация. В младшей возрастной группе эта агрегация проявилась только с одним родителем (большинство матери), в старшей — с обоими. Полученные данные позволяют предположить, что в ранний патогенез сахарного диабета 2-го типа вовлечены как генетические факторы, так и факторы окружающей среды. Очевидное доминирование передачи супруга-родителя только в младшей возрастной группе, возможно, обусловлено тем, что в раннем возрасте ребенок больше проводит времени с матерью, а не с отцом. Это является дополнительным аргументом, что объектом обследования и профилактического воздействия должны быть все члены семьи пробанда.



