В последнее время появилось немало статей, в которых обсуждается вопрос о том, как наличие атеросклеротического поражения в одном кровеносном сосуде отражает распространение атеросклероза в другие сосудистые бассейны [1—8]. Это очень важно для выявления риска развития инфаркта миокарда (ИМ), так как прогнозировать развитие ИМ с помощью неинвазивных методов очень сложно. В то же время исследовать внутреннюю сонную артерию (ВСА) неинвазивными методами не представляет большой сложности, особенно с помощью ультразвукового исследования (УЗИ). Состояние таких больных можно легко мониторировать, поэтому ряд авторов проводят исследования по изучению того, как атеросклеротические поражения в бассейне сонной артерии сочетаются с заболеваемостью ИМ, и ищут факторы, по которым можно прогнозировать заболеваемость ИМ при наличии атеросклеротической бляшки (АСБ) в ВСА. часто обследуются больные с ишемической болезнью сердца [2—4]. Кроме того, исследуется гипотеза, можно ли прогнозировать заболеваемость ИМ при наличии АСБ в ВСА, установленной только с помощью УЗИ [9, 10]. Некоторые авторы считают, что только нестабильная АСБ может демонстрировать распространение атеросклеротических изменений на другие сосуды [7—11]. Научные исследования, проведенные другими авторами, отмечают связь между ИМ и структурой АСБ [11]. Все исследователи отмечают, что необходим поиск факторов, на основе которых можно прогнозировать распространение атеросклероза в коронарные артерии (КА) и заболеваемость ИМ при наличии АСБ в ВСА.
Цель настоящего исследования — обнаружить связь между АСБ ВСА и ИМ, а также выявить факторы, которые определяют распространение атеросклероза в КА.
Материал и методы
Обследованы 655 больных, которым выполнена эндартерэктомия ВСА; из них 148 в прошлом перенесли ИМ. Оценивали следующие факторы риска: возраст, пол, артериальная гипертензия (АГ), сахарный диабет, гиперхолестеринемия, повышенный уровень фибриногена, мерцательная аритмия. Оценивали также степень стеноза ВСА, степень сужения противоположной ВСА, степень стеноза позвоночных артерий. Степень сужения установлена по данным дуплексного сканирования и уточнена методом ангиографии. УЗИ кровеносных сосудов проведено в Республиканской Вильнюсской клинической больнице и в Клинической больнице г. Вильнюса.
В двухмерном режиме с помощью линейного датчика 7,5 MГц осмотрены общая сонная артерия, ее бифуркация, внутренняя и наружная сонные артерии, просвет позвоночных артерий и их протяженность в костном канале. Оценивали АСБ в сонных артериях и их ультразвуковые характеристики в соответствии с классификацией Gray—Weal и Geroulakos [12]: I тип: эхонегативные бляшки с наличием или без эхогенных образований; II тип: преобладает эхонегативная структура, эхогенные структуры составляют <50%; III тип: преобладает эхогенная структура, эхонегативные структуры составляют <50%; IV тип: эхогенная бляшка; V тип: бляшка не поддается классификации из-за акустической тени. Если граница атеросклеротических изменений в ультразвуковом отражении была ровной и однородной, то поверхность АСБ расценивали как гомогенную. Если граница была прерывающаяся, с изъязвлением >2 мм, то поверхность бляшки определяли как гетерогенную. Степень стеноза измеряли импульсно-волновым допплером в режиме окрашивания кровотока. С помощью установленной методики измеряли скорость кровотока в месте стеноза; выявлена следующая степень стеноза: 50—69% при систолической скорости (V sist.) 125—230 см/с, 70—89% при V sist. 230—325 см/с, критическая (≥90%), при V sist. >325 см/с [13]. УЗИ проведено у всех 665 больных.
Субстратное ангиографическое исследование (АИ) проводили с помощью аппарата Siemens Axiom Artis в Республиканской Вильнюсской клинической больнице. Исследования выполняли у больных, у которых во время УЗИ был выявлен гемодинамически значимый стеноз ВСА, в случаях, если больному было намечено хирургическое лечение, при согласии больного на АИ и в отсутствие противопоказаний (аллергия, почечная недостаточность, беременность, нарушение свертываемости крови, отсутствие контакта с больным из-за нарушения сознания). Степень стеноза артерии оценивали с учетом критериев NASCET: (1 – N/D) · 100%, где N — самое узкое место суженного просвета, D — просвет ВСА над bulbus caroticus [14]. Сужение ВСА расценивали как критическое при стенозе ≥90%, высокой степени — 70—89%, средней — 50—69%. АИ рассматривают как «золотой стандарт» при определении степени стеноза сонной и позвоночной артерий. АИ имеет особое значение при определении степени стеноза позвоночной артерии, так как у некоторых больных из-за анатомической структуры шеи (толстая, короткая шея) результаты УЗИ могут быть недостоверными. АИ проведено у 595 (89,5% больных), включенных в исследование.
 У 213 больных во время операции проводили оценку АСБ макроскопически, т. е. оценивали степень стеноза, гетерогенность бляшки, изъязвление бляшки, наличие тромба, внутрибляшечную геморрагию (ВБГ). Выявлены следующие признаки гомогенной бляшки: бляшка является однородной, если у нее отсутствуют трещины и язвы, а поверхность гладкая. Признаки гетерогенной бляшки иные: она неоднородная, с неровной поверхностью, с трещинами и язвами. Больных расценивали как имеющих симптомы, если они перенесли инсульт или транзиторную ишемическую атаку в бассейне оперированной артерии не ранее чем за 6 мес до операции.
У 213 больных во время операции проводили оценку АСБ макроскопически, т. е. оценивали степень стеноза, гетерогенность бляшки, изъязвление бляшки, наличие тромба, внутрибляшечную геморрагию (ВБГ). Выявлены следующие признаки гомогенной бляшки: бляшка является однородной, если у нее отсутствуют трещины и язвы, а поверхность гладкая. Признаки гетерогенной бляшки иные: она неоднородная, с неровной поверхностью, с трещинами и язвами. Больных расценивали как имеющих симптомы, если они перенесли инсульт или транзиторную ишемическую атаку в бассейне оперированной артерии не ранее чем за 6 мес до операции.
Качественные данные сравнивали с помощью критерия χ2 или точного критерия Фишера. Для сравнения количественных значений переменных использовался критерий Стьюдента. Факторы риска, которые могут прогнозировать ИМ, были установлены при помощи логистического регрессионного анализа. Вычисляли отношение шансов (OШ) и 95% доверительные интервалы (ДИ). Различия считали статистически значимыми при p<0,05.
Результаты
Больным, у которых стеноз ВСА был более 50%, выполнена эндартерэктомия. Средний возраст оперированных больных составил 65,6±0,3 года. Всего оперированы 520 (78,2%) мужчин и 145 (21,8%) женщин. У 48,7% больных имелся гемодинамически значимый стеноз другой брахиоцефальной артерии (БЦА). У многих больных имелся мультифокальный атеросклероз (МФА): 22,3% в прошлом перенесли острый ИМ, 43,6% — ИБС, у 11,1% были поражены периферические артерии, у 30,9% имелась симптоматика в другом бассейне (не в БЦА).
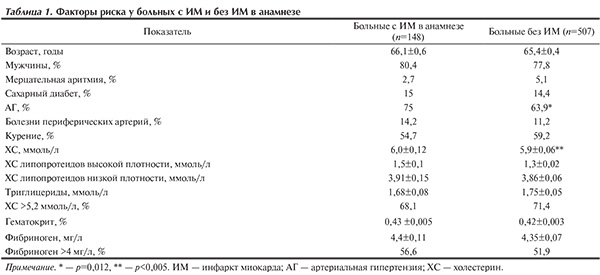
Больные с ИМ в анамнезе страдали артериальной гипертензией (АГ) чаще, чем больные без ИМ (75 и 63,9% соответственно; p<0,05). Другие факторы риска васкулярного характера статистически значимо не различались (табл. 1). В группе больных, которые перенесли ИМ, средний уровень холестерина липопротеидов высокой плотности (1,5±0,1 ммоль/л) был выше, чем в группе больных без ИМ (1,3±0,02 ммоль/л; p<0,05), но больные в 1-й группе в 4,2 раза чаще употребляли статины.
Клинически проявляющийся стеноз оперированной ВСА имелся у 61,5% больных, перенесших ИМ, и у 57,4% больных без ИМ (p>0,05). В табл. 2 представлены данные о различиях по степени сужения ВСА и типе бляшки у оперированных больных с ИМ и без ИМ. У больных, перенесших ИМ, и без ИМ, степень стеноза не различалась, хотя сужение ВСА >70% статистически незначимо встречалось чаще у больных, перенесших ИМ (88,5% против 87,2%; p>0,05). Однако гетерогенные АСБ, т. е. нестабильная бляшка ВСА, у больных с ИМ в анамнезе выявлялись чаще, чем у больных без ИМ (82 и 75,1% соответственно; p<0,05).
В табл. 3 представлены данные о распространении атеросклеротического процесса в других магистральных экстракраниальных артериях шеи у больных сравниваемых группах. Больные с ИМ в анамнезе чаще, чем больные без ИМ, имели гемодинамически значимое сужение другой артерии шеи (58,1 и 46% соответственно; p<0,01), у них чаще выявлялся стеноз позвоночной артерии шеи более 50% (25,7 и 15,8% соответственно; p<0,01). Примечательно, что больные, у которых был установлен гемодинамически значимый стеноз нескольких магистральных артерий шеи, не только чаще имели ИМ в анамнезе (27 и 18,5% соответственно; p<0,01), но и чаще, чем больные, которые имели только стеноз ВСА, страдали атеросклерозом периферических артерий (15,2 и 8,8% соответственно; p=0,012). У больных с распространением атеросклероза более чем в одной магистральной артерии, снабжающей головной мозг, и сужением их диаметра более чем на 50%, в сравнении с больными, которые имели только лишь стеноз ВСА, гемодинамически значимый стеноз был найден и в других сосудах, таких как КА и/или периферические артерии (38,6 и 24,4% соответственно; p<0,001). Отметим, что гетерогенная АСБ клинически проявлялась у 89,8%, а гомогенная — у 88,5% больных (p>0,05).
 Число больных, которые с нераспространенным атеросклерозом и гомогенной бляшкой в ВСА перенесли ИМ, составило только 8,2%. В то же время среди больных с гетерoгенной бляшкой в ВСА и распространенным атеросклерозом в БЦА или в периферических артериях чиcлo перенесших ИМ составило 27,2% (p<0,005).
Число больных, которые с нераспространенным атеросклерозом и гомогенной бляшкой в ВСА перенесли ИМ, составило только 8,2%. В то же время среди больных с гетерoгенной бляшкой в ВСА и распространенным атеросклерозом в БЦА или в периферических артериях чиcлo перенесших ИМ составило 27,2% (p<0,005).
С помощью логистического регрессионного анализа (табл. 4) выявляли факторы риска развития ИМ у больных с гемодинамически значимым стенозом ВСА. Как представлено в табл. 4, статистически значимое влияние на возникновение и развитие ИМ имели гетерогенность АСБ (OШ 2,3 при 95% ДИ от 1,02 до 5,17; p=0,04) и распространение атеросклеротического процесса в более чем одной магистральной артерии шеи c гемодинамически значимым стенозoм (OШ 1,81 при 95% ДИ от 1,0 до 3,26; p=0,049).
У 213 больных во время операции проводили оценку АСБ макроскопически. В табл. 5 представлены характеристика АСБ, ее макроскопические различия у больных с ИМ в анамнезе и без ИМ. ВБГ установлена у 43,2% больных, перенесших ИМ, в сравнении с 17,6% больных без ИМ (p=0,001).
Обсуждение
У больных с МФА, гемодинамически значимо сужающим сосуды, факторы риска, кроме АГ, статистически значимо не отличались от тех же факторов риска у больных, у которых АСБ, сужающая артерию >50%, была только в ВСА. Атеросклероз — это мультифокальный процесс. АСБ в ВСА увеличивает риск повреждения КА, что подтверждают и данные литературы [1—7]. Как видно из наших данных, почти у 50% больных, имеющих гемодинамически значимый стеноз в ВСА, был выявлен атеросклероз периферических артерий и/или имелись признаки повреждения КА (стенокардия или ИМ), а ИМ в анамнезе был у 22,3% больных. Эти данные сопоставимы с данными авторов, которые исследовали больных с патологией БЦА. КА были повреждены у 18% больных с патологией БЦА [3]. Почти у 50% больных, имеющих стеноз ВСА, был гемодинамически значимый стеноз другой БЦА. По нашим данным, распространение атеросклероза в другие БЦА — это определенный показатель, отражающий распространение атеросклероза и в другие бассейны, в том числе в КА. Этот риск увеличивается в 1,8 раза по сравнению с таковым у больных с гемодинамически значимо поврежденной атеросклерозом только одной ВСА. Таким образом, распространение атеросклероза не только в другом бассейне, но и в нескольких БЦА увеличивает шансы того, что атеросклероз охватывает и КА, т.е. увеличивает риск развития ИМ.
Нами изучено, увеличивает ли характер повреждения ВСА шансы развития ИМ. Установлено, что при увеличении степени стеноза риск возникновения ИМ не возрастает. Однако в результате проведенного исследования с участием 665 больных стало очевидно, что шансы развития ИМ, т.е. шансы повреждения КА, наивысшие при наличии гетерогенной (нестабильной) АСБ в ВСА. Как известно, нестабильная бляшка может разорваться и тромбироваться, поэтому в сосудах, в которых обнаружена нестабильная АСБ, может появиться соответственная симптоматика (инсульт, ИМ и т.д.). Важно также знать, может ли нестабильная АСБ одного бассейна отражать патологию и другого бассейна, т.е. представляет ли нестабильность АСБ системный процесс. Наши результаты частично совпадают с данными других авторов, которые исследовали АСБ в ВСА с помощью УЗИ и магнитно-резонансной томографии и сравнивали их с коронарной симптоматикой [7—11]. Эти авторы также пришли к выводу, что нестабильная АСБ в большей степени, чем такая же стабильная АСБ в ВСА, увеличивает риск развития ИМ, т.е. увеличивает риск появления нестабильной бляшки в КА. Подчеркнем и то, что АСБ в КА имеет тенденцию к тромбозу чаще, чем такая же АСБ в ВСА [15]. Поэтому нестабильная АСБ в КА скорее становится причиной ИМ, чем такая же нестабильная АСБ в ВСА — причиной инсульта. Это частично объясняет тот факт, что число клинически проявляющихся ВСА в группах с гомогенной и гетерогенной бляшками в ВСА статистически значимо не различалось. В то же время число ИМ значительно различалось в группах с гомогенной и гетерогенной бляшками в ВСА. Это, скорее всего, отражает то, что нестабильность АСБ в КА коррелирует с нестабильностью АСБ в ВСА.
 ВБГ — один из факторов нестабильности АСБ, и она более характерна для ВСА, а не для КА [15]. Наши данные совпадают с данными других авторов, которые заметили, что именно ВБГ в ВСА теснее всего коррелирует с патологией КА [11]. Следует отметить, что это связано с увеличением частоты развития АГ в этой группе, что в свою очередь может являться важным фактором риска нестабильности бляшки и распространения ее в КА. Поэтому, проводя лечение больных, важно не только применять статины, но и осуществлять коррекцию артериального давления, так как оно может служить причиной ВБГ и тем самым как увеличивать нестабильность бляшки, так и повышать риск атеросклероза.
ВБГ — один из факторов нестабильности АСБ, и она более характерна для ВСА, а не для КА [15]. Наши данные совпадают с данными других авторов, которые заметили, что именно ВБГ в ВСА теснее всего коррелирует с патологией КА [11]. Следует отметить, что это связано с увеличением частоты развития АГ в этой группе, что в свою очередь может являться важным фактором риска нестабильности бляшки и распространения ее в КА. Поэтому, проводя лечение больных, важно не только применять статины, но и осуществлять коррекцию артериального давления, так как оно может служить причиной ВБГ и тем самым как увеличивать нестабильность бляшки, так и повышать риск атеросклероза.
Таким образом, больным, у которых диагностирован атеросклероз в нескольких БЦА и гетерогенная АСБ в ВСА, особенно ВБГ, необходимо особое внимание и лечение, чтобы предотвратить развитие ИМ.
Заключение
Нестабильность атеросклеротической бляшки (особенно внутрибляшечная геморрагия) внутренней сонной артерии и распространение стеноза >50% в более чем одной брахиоцефальной артерии шеи являются независимыми факторами риска, наличия коронарного атеросклероза и развитие инфаркта миокарда.



