Дегенеративный стеноз аортального клапана (АК) — самый распространенный приобретенный порок сердца [1], встречающийся у 3% лиц старше 75 лет [2]. Консервативное лечение больных с клинической симптоматикой заболевания сопровождается высокой смертностью, достигающей 50% в течение 1 года наблюдения, тогда как у лиц с бессимптомным аортальным стенозом тяжелой степени выживаемость в течение 2 лет составляет 20—50%. Хирургическое протезирование АК — единственный метод лечения, позволяющий добиться как уменьшения симптомов, так и увеличения продолжительности жизни [3]. При успешном исходе операции отдаленный прогноз сопоставим с таковым в общей популяции, особенно среди пожилых лиц. Однако 1/3 больных, нуждающихся в хирургическом лечении, не получают его ввиду высокого операционного риска [1]. С 2002 г. появилась альтернатива классической операции протезирования — эндоваскулярная имплантация искусственного клапана. В первом рандомизированном исследовании PARTNER с участием 700 больных, признанных неоперабельными, выживаемость в течение 1-го года после транскатетерного протезирования аортального клапана (ТПАК) была сопоставима с таковой после хирургического протезирования [4] и существенно выше, чем при медикаментозном лечении [5]. Мы представляем больного с декомпенсированным стенозом АК, крайне высоким операционным риском и рецидивом хронического В-клеточного лимфолейкоза (В-ХЛЛ), требующим проведения химиотерапии лишь после компенсации сердечной патологии.
Больной П., 70 лет, поступил в стационар в феврале 2014 г. с жалобами на выраженную слабость, одышку и боли в грудной клетке при незначительных физических нагрузках и в покое. В течение длительного времени страдает артериальной гипертензией с подъемами артериального давления (АД) до 160/90 мм рт.ст. С 2010 г. появились типичные приступы стенокардии напряжения и покоя, одышка при ходьбе до 100 м. В декабре 2012 г. впервые в жизни возник обморок во время физической активности, который повторялся впоследствии 4 раза. При эхокардиографии (ЭхоКГ) был выявлен дегенеративный стеноз АК.
В июле 2013 г. больной перенес передний инфаркт миокарда без подъема сегмента ST. Заболевание протекало без осложнений, проводилось медикаментозное лечение ацетилсалициловой кислотой (АСК), клопидогрелом, β-адреноблокаторами, статинами.
В октябре 2013 г. в связи со стенокардией напряжения IV функционального класса был впервые госпитализирован в РКНПК. Состояние стабильное, средней тяжести, рост 182 см, масса тела 108 кг, грубый систолический шум над всей поверхностью сердца, частота сердечных сокращений (ЧСС) 72 уд/мин, ритм правильный, АД 130/80 мм рт.ст., частота дыхательных движений (ЧДД) 18 в минуту, в легких хрипы отсутствовали.
По данным ЭхоКГ выявлены признаки сочетанного аортального порока: максимальная скорость трансаортального потока 5,0 м/с, средний систолический градиент между левым желудочком (ЛЖ) и аортой 64 мм рт.ст., площадь отверстия АК по уравнению непрерывности 0,5 см2, аортальная недостаточность II степени. Отмечены расширение ЛЖ до 6,0 см со снижением фракции выброса (ФВ) до 38%, гипертрофия миокарда ЛЖ с утолщением стенок до 1,3—1,5 см, увеличение обоих предсердий, начальная легочная гипертензия (систолическое давление в легочной артерии 33 мм рт.ст.).
При коронарографии выявлены стеноз до 40% в средней трети передней нисходящей артерии, в диагональной артерии — до 60%. На фоне стандартной терапии были достигнуты субкомпенсация недостаточности кровообращения и стабилизация параметров гемодинамики (при выписке ЧСС 65/мин, АД 100/70 мм рт.ст.). По результатам обследования консилиум с участием кардиохирургов определил показания к изолированному протезированию АК. Однако, принимая во внимание выраженный гиперлейкоцитоз 130×109/л, больной был выписан для коррекции заболевания крови.
Диагноз В-ХЛЛ, стадия А по Binet был установлен в 1996 г. Показания к началу лечения возникли в 2007 г., пациенту было проведено 6 курсов химиотерапии (препаратами флударабин, митоксантрон, циклофосфамид, ритуксимаб) с неподтвержденной полной ремиссией в 2008 г. Рецидив В-ХЛЛ зарегистрирован в 2012 г., в ноябре 2013 г.возникла необходимость специфической терапии. Учитывая тяжелое общее состояние больного, обусловленное декомпенсацией аортального порока и рецидивом хронического лимфолейкоза, в качестве паллиативной циторедуктивной терапии и подготовки к хирургическому лечению проводилась терапия ритуксимабом и дексаметазоном в течение 3 дней, ежемесячные внутривенные введения иммуноглобулина в дозе 20 г. На фоне лечения отмечены снижение опухолевого лейкоцитоза до 13×109/л и уменьшение размеров периферических лимфатических узлов.
Больной регулярно принимал бисопролол 2,5 мг, АСК 100 мг, аторвастатин 10 мг, диуретики (торасемид и спиронолактон). Однако с момента выписки из РКНПК в октябре 2013 г. стали прогрессировать явления недостаточности кровообращения в обоих кругах кровообращения в виде нарастания слабости, одышки, приступов удушья в ночные часы, отеков ног, постепенного снижения переносимости физических нагрузок, массы тела.
При поступлении состояние больного расценивалось как тяжелое. При осмотре положение ортопноэ, кожные покровы теплые, слабо развитый подкожно-жировой слой (кахексия), масса тела 98 кг.
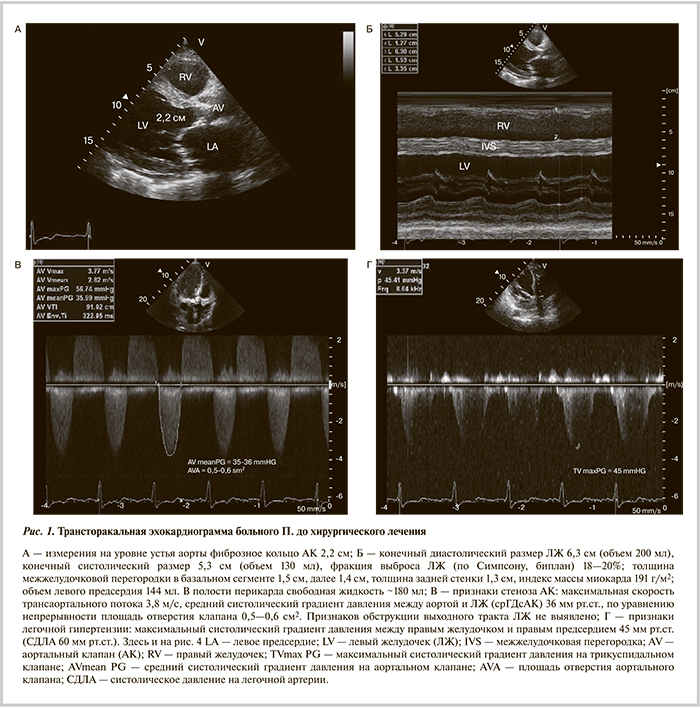
ЧДД 30 в минуту, дыхание жесткое, хрипы отсутствовали. Ритм сердечных сокращений правильный с частотой 78 уд/мин, АД 80/60 мм рт.ст. В точке аускультации АК выслушивался слабый систолический шум. Отмечались набухшие вены шеи, пульсация периферических артерий симметричная, ослабленная. Живот увеличен за счет асцита, умеренно болезненный при пальпации в правом подреберье, печень увеличена, отеки стоп и голеней. На электрокардиограмме (ЭКГ) покоя: синусовый ритм, атриовентрикулярная блокада I степени (PQ 220 мс), блокада передней ветви левой ножки пучка Гиса (QRS 110 мс), признаки гипертрофии ЛЖ. При рентгенографии легких выявлено усиление легочного рисунка за счет сосудистого и интерстициального компонентов, расширение верхнедолевых сосудов; венозный застой I—II степени; малоструктурные и расширенные корни; небольшой двусторонний плевральный выпот (гидроторакс); кардиомегалия (кардиоторакальный индекс 65%). По данным ЭхоКГ (рис. 1): критический декомпенсированный стеноз АК с кальцинозом III—IV степени и недостаточностью II степени; выраженная гипертрофия миокарда ЛЖ; увеличение размеров всех полостей сердца, преимущественно левых отделов; на фоне диффузного снижения сократимости акинезия средневерхушечных отделов переднеперегородочной стенки; нарушение диастолической функции миокарда ЛЖ по рестриктивному типу; легочная гипертензия II степени; гидроперикард; признаки повышения центрального венозного давления и малого сердечного выброса.
При суточном мониторировании ЭКГ клинически значимых нарушений ритма и проводимости сердца не зарегистрировано, средняя ЧСС 87 уд/мин. При ультразвуковом исследовании внутренних органов выявлено увеличение печени с признаками венозного застоя; умеренный выпот в плевральной и брюшной полостях, в перикарде; в парааортальной области конгломераты гипо- и изоэхогенных округлых образований (лимфатические узлы). При мультиспиральной компьютерной томографии определялся кальциноз АК с переходом на митрально-аортальный контакт; диаметр фиброзного кольца АК 2,9×2,2 см; расстояние от устья левой коронарной артерии до фиброзного кольца 1,1 см, расстояние от устья правой коронарной артерии 1,5 см; диаметр аорты на уровне синусов Вальсальвы 3,4×3,5×3,6 см; двусторонний гидроторакс; гидроперикард; внутригрудная, подмышечная, брюшная, паховая лимфаденопатия; признаки легочной гипертензии. В анализах крови гемоглобин 10—12 г/дл при нормальном уровне сывороточного железа (15 мкмоль/л), гематокрит 30%, лейкоциты в диапазоне (12—25)×109/л, лимфоидная формула, скорость оседания эритроцитов 10 мм/ч, тромбоциты 228×109/л, клиренс креатинина >60 мл/мин (формула Кокрофта—Голта), гипербилирубинемия до 37 мкмоль/л. Были начаты интенсивная диуретическая терапия, курс альбумина в связи с гипоальбуминемией (34 г/л), коррекция электролитов, продолжена терапия АСК и бисопрололом. На фоне медикаментозного лечения исчезли отеки ног, уменьшилась выраженность одышки, за 14 дней масса тела снизился на 10 кг. Однако сохранялись гипотония, синусовая тахикардия (90—95 уд/мин), тахипноэ, рентгенологические признаки легочно-артериальной гипертензии и венозного застоя легких до II степени, высокий уровень мозгового натрийуретического пептида (BNP) до 3300 пг/мл. При ЭхоКГ обращало на себя внимание значимое ухудшение гемодинамических параметров по сравнению с октябрем 2013 г. в виде снижения глобальной сократимости (ФВ ЛЖ с 38 до 20%) и уменьшения среднего градиента давления между полостью ЛЖ и аортой с 64 до 35 мм рт.ст. при площади отверстия 0,5—0,6 см2. По рекомендации гематолога, в предоперационном периоде проводилось лечение иммуноглобулином человека, в качестве антибиотика был выбран цефалоспорин третьего поколения. Непосредственно перед операцией в анализе крови лейкоциты 26×109/л, гемоглобин 12 г/дл, гематокрит 38%, тромбоциты 228×109/л.
Транскатетерная трансфеморальная имплантация биопротеза Edwards SAPIEN XT 29 мм (рис. 2, см. цветную вклейку) в позицию АК выполнена 11.03.14 г. При контрольной ангиографии коронарные артерии проходимы, нормальное функционирование протеза (рис. 3, см. цветную вклейку).
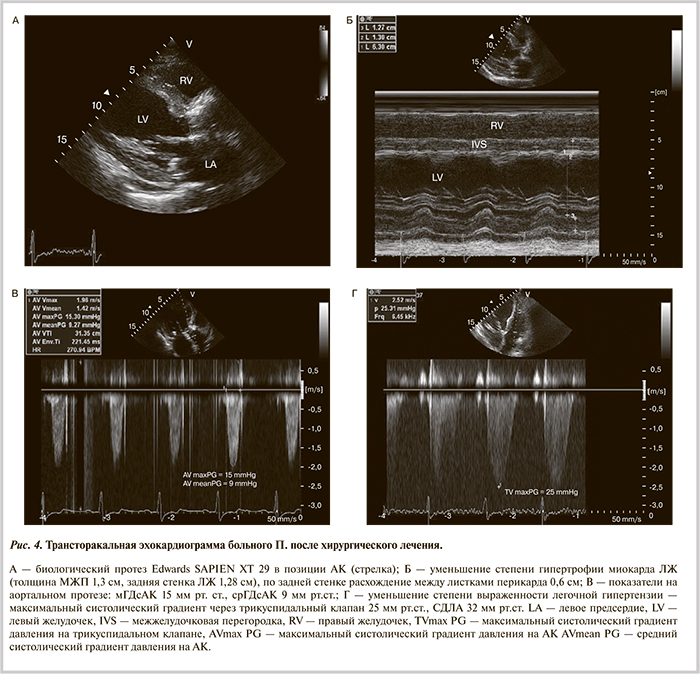
После хирургического вмешательства отмечено улучшение состояния больного: снижение ЧСС до 68—72 уд/мин, увеличение АД до 110—120/60 мм рт.ст., отсутствие одышки в покое и снижение давления в легочной артерии до 42/24 мм рт.ст. Успешное проведение малотравматичной операции без использования аппарата искусственного кровообращения позволило активизировать больного в течение 3 сут после операции. При повторном суточном мониторировании ЭКГ клинически значимых нарушений ритма и проводимости сердца не зарегистрировано. При ЭхоКГ на 3-и сутки после ТПАК (рис. 4) дисфункции аортального протеза не наблюдалось, уменьшились признаки легочной гипертензии и количество жидкости в полости перикарда.
От терапии варфарином решено было воздержаться, к проводимому лечению АСК, β-адреноблокаторами, малыми дозами ингибиторов ангиотензинпревращающего фермента, петлевыми диуретиками, антагонистами минералокортикоидных рецепторов, аторвастатином был добавлен клопидогрел. Наблюдались дальнейшая стабилизация состояния и параметров гемодинамики, уменьшение явлений недостаточности кровообращения со снижением уровня BNP до 440 пг/мл.
Больной был выписан на 11-е сутки после операции с диагнозом: приобретенный сочетанный аортальный порок: декомпенсированный критический аортальный стеноз, умеренная недостаточность АК. Трансфеморальное протезирование АК биопротезом Edwards SAPIEN XT №29 11.03.14. Ишемическая болезнь сердца: постинфарктный атеросклероз (2013), атеросклероз коронарных артерий. Атеросклероз аорты, сонных артерий. Хроническая сердечная недостаточность IIА стадии,III функционального класса. Вторичная легочная гипертензия. В-ХЛЛ, рецидив, стадия С (Binet).
Через 1 мес после операции состояние и показатели гемодинамики больного на фоне терапии были стабильными, больной отметил увеличение переносимости физических нагрузок.
Мы представили случай успешной эндоваскулярной коррекции декомпенсированного критического стеноза АК у мужчины 70 лет с В-ХЛЛ. Возможность лечения В-ХЛЛ с помощью химиотерапии изначально была ограничена наличием патологии сердца. В то же время наличие лимфолейкоза и выраженность сердечной недостаточности обусловливали высокий риск, ассоциированный с хирургической коррекцией клапана. В отсутствие лечения прогноз у данного больного оценивался как крайне неблагоприятный. Риск смерти был рассчитан как 5,7% по шкале EuroSCORE.
Согласно рекомендациям по лечению больных с клапанными пороками сердца (версия 2014 г.) [6], тяжесть аортального стеноза у нашего больного соответствовала стадии D2 — клинически проявляющийся критический стеноз с низким потоком и низким градиентом. В данном случае методом выбора в лечении являлась операция ТПАК с уровнем доказательности IС. У больных с выраженным бессимптомным стенозом АК без систолической дисфункции ЛЖ или соответствующих гемодинамических и клинических отклонений при нагрузочном тесте сроки проведения хирургического вмешательства остаются предметом дискуссий. Отсутствуют исследования, демонстрирующие пользу от хирургического лечения даже в случаях критического поражения клапана. Баллонная вальвулопластика может рассматриваться как «мост» до хирургического или эндоваскулярного протезирования у больных с гемодинамической нестабильностью, в частности при ургентной некардиохирургической операции (класс IIb, уровень C) [7]. Развитие недостаточности кровообращения, стенокардии, синкопэ или пресинкопэ являются определяющими при направлении больного со стенозом АК на операцию. Решение о выборе метода протезирования принимается на основании значимости сопутствующих заболеваний, степени кальциноза клапана, выраженности коронарного атеросклероза и необходимости реваскуляризации миокарда.
Согласно современному алгоритму ведения больных с выраженным аортальным стенозом, абсолютными показаниями к транскатетерному протезированию являются наличие противопоказаний к открытой операции или сопряженного с ней высокого риска при учете, что ожидаемая продолжительность жизни больного составляет более 1 года [7]. Важно подчеркнуть, что эндоваскулярное вмешательство на клапане должно проводиться лишь в лечебных учреждениях с возможностью перехода к открытой операции. С технических позиций операция ТПАК может быть выполнена практически у любого пациента с аортальным стенозом. Абсолютные противопоказания к проведению ТПАК классифицируют на: 1) анатомические – слишком большой или маленький размер фиброзного кольца (<18 мм или >29 мм), наличие тромба в полости ЛЖ, активный инфекционный эндокардит, высокий риск закрытия устья коронарной артерии (асимметричный кальциноз клапана, небольшое расстояние от коронарных устьев до кольца, малый размер синусов Вальсальвы), наличие бляшек с флотирующим тромбом в восходящей аорте или ее дуге, особенности периферического доступа (размер сосудов, их кальциноз и извитость); 2) клинические – ожидаемая продолжительность жизни менее 1 года, тяжелые сопутствующие заболевания, наличие комбинированной клапанной патологии, которая может быть скорректирована при помощи хирургической операции. К относительным противопоказаниям относятся двустворчатый АК, потребность в реваскуляризации миокарда, нестабильная гемодинамика, ФВ ЛЖ<20%, для трансапикального доступа — болезнь легких тяжелой степени, невозможность доступа к верхушке ЛЖ.
При высоком операционном риске (оценка по шкале EuroSCORE≥20% или STS>10%) врачебный консилиум нередко принимает решение в пользу эндоваскулярного лечения с возможностью проведения открытой операции [8]. При невысоком операционном риске (EuroSCORE<20% или STS<10%) наличие таких факторов, как старческий возраст, «фарфоровая аорта», отсутствие стенозирующего поражения коронарного русла, облучение средостения в анамнезе, цирроз печени, делают больного также более вероятным кандидатом для ТПАК. Ввиду отсутствия адекватной шкалы оценки риска у больных с показаниями к протезированию АК используется индивидуальный подход [9].



