Процесс дестабилизации атеросклеротической бляшки (АСБ) можно отнести к классической воспалительной реакции, в которой непосредственное участие принимают факторы иммунной системы: эндотелиальные клетки, макрофаги, Т-лимфоциты, нейтрофилы и гладкие мышечные клетки (ГМК) [1].
В последнее время большое внимание уделяется изучению врожденного иммунитета, напрямую связанного с воспалением, у больных ишемической болезнью сердца (ИБС) и острым коронарным синдромом (ОКС). Более 40 лет изучается роль активации комплемента в развитии реперфузионного повреждения миокарда у больных ОКС. В 1970 г. J. Hill и Р. Ward опубликовали данные исследования, в котором продемонстрировано, что при развитии экспериментального инфаркта миокарда (ИМ) ингибирование комплемента приводило к уменьшению хемотаксиса и аккумуляции нейтрофилов в зоне повреждения [2]. Комплемент является одним из участников воспалительной реакции. Его мембранно-атакующие комплексы обнаружены в инфарцированном миокарде животных и человека в остром периоде ИМ.
Маннозо-связывающий лектин (MBL – mannose-binding lectin) — важный фактор врожденного иммунитета, участвующий в защите от бактерий, вирусов, грибов. Он запускает лектиновый путь активации комплемента, играет ключевую роль в фагоцитозе и опсонизации чужеродных организмов. Дефицит MBL считается одним из наиболее часто встречаемых иммунодефицитных состояний. У детей низкий уровень MBL ассоциируется с рецидивирующими инфекциями [3—5]. Дефицит MBL может играть важную роль патогенезе аутоиммунных и онкологических заболеваний [6, 7].
В последние годы активно изучается влияние MBL на развитие ОКС. В нескольких экспериментальных работах показано, что блокада лектинового пути активации комплемента с помощью антител к MBL приводит к уменьшению зоны реперфузионного повреждения миокарда [8—10]. В клинических исследованиях получены противоречивые данные о влиянии концентрации MBL на риск развития ИБС и ИМ, а также на прогноз после ОКС. В ряде работ показано протективное влияние MBL, по другим источникам получен обратный результат [11—13].
 Имеются неоднозначные данные о прогностической значимости как высокого уровня MBL [14—16], так и дефицита этого белка у больных ИМ [17, 18]. В некоторых работах уровень MBL не влиял на развитие ИБС и ИМ [19]. Эти данные свидетельствуют о неоднозначной роли MBL, который может в разных клинических ситуациях либо улучшать прогноз у больных, либо, наоборот, способствовать развитию осложнений. Если при инфекционно-воспалительных процессах имеется достаточно четкое понимание роли MBL, то участие MBL в патогенезе сердечно-сосудистых заболеваний, атеросклероза, ИМ в настоящее время остается недостаточно изученным.
Имеются неоднозначные данные о прогностической значимости как высокого уровня MBL [14—16], так и дефицита этого белка у больных ИМ [17, 18]. В некоторых работах уровень MBL не влиял на развитие ИБС и ИМ [19]. Эти данные свидетельствуют о неоднозначной роли MBL, который может в разных клинических ситуациях либо улучшать прогноз у больных, либо, наоборот, способствовать развитию осложнений. Если при инфекционно-воспалительных процессах имеется достаточно четкое понимание роли MBL, то участие MBL в патогенезе сердечно-сосудистых заболеваний, атеросклероза, ИМ в настоящее время остается недостаточно изученным.
Материал и методы
В исследование были включены 77 больных ОКС в возрасте 30—70 лет независимо от пола. Всем больным ОКС с подъемом сегмента ST (ОКСпST) проведены тромболитическая терапия (ТЛТ) или чрескожное коронарное вмешательство (ЧКВ). ТЛТ проводилась пациентам либо в стационаре, либо на этапе скорой медицинской помощи. Эндоваскулярную реваскуляризацию выполняли как самостоятельный метод реперфузионного лечения (первичное ЧКВ) или после ТЛТ. В дальнейшем больные получали стандартную медикаментозную терапию, включающую ацетилсалициловую кислоту, клопидогрел, β-адреноблокаторы, статины, ингибиторы ангиотензинпревращающего фермента АПФ, а также, по показаниям, мочегонные и другие препараты. При выявлении клинических и инструментальных признаков ишемии пациентам была рекомендована коронарография, а в дальнейшем эндоваскулярное лечение. Больным ОКС без подъема сегмента ST (ОКСбпST) назначали стандартную лекарственную терапию, основу которой составляли антитромботические, антиангинальные препараты и статины. Помимо консервативного лечения ряду больных ОКСбпST проведено экстренное или плановое ЧКВ.
Критерии исключения из исследования: злокачественные новообразования и другие тяжелые сопутствующие заболевания, самостоятельно влияющие на прогноз; вторичная нестабильная стенокардия, в частности обусловленная анемией, тиреотоксикозом, тахиаритмиями. Повышение уровня аспартатаминотрансферазы >75 ед/л, аланинаминотрансферазы >200 мкмоль/л или печеночная недостаточность. Острые инфекционные и воспалительные заболевания; заболевания, требующие постоянного приема нестероидных противовоспалительных препаратов, блокаторов циклооксигеназы-2, глюкокортикоидов (ревматоидный артрит и другие заболевания соединительной ткани, тяжелое течение бронхиальной астмы); хроническая сердечная недостаточность (СН).
Диагностические критерии ОКС: диагностику ОКС проводили в соответствии с критериями Европейского общества кардиологов [20]. У всех больных при поступлении произведен забор крови для последующего определения MBL. Сыворотку замораживали и хранили при температуре -70 °С. Уровень MBL определяли с помощью стандартного коммерческого набора HBT Human MBL (lectin assay) ELISA. В основе метода лежит специфическая реакция антиген-антитело. Выявление образовавшегося комплекса проводят с использованием фермента в качестве метки для регистрации сигнала.
Наблюдение за больными ОКС продолжалось в среднем 571 день, минимум 1 день, максимум 940 дней от наступления ОКС. Первичной конечной точкой была сердечно-сосудистая смертность (ССС) и нефатальный ИМ. Вторичная конечная точка — ССС, повторный ИМ, реваскуляризация, повторная госпитализация c целью лечения нестабильной стенокардии или недостаточности кровообращения.
Статистический анализ данных проводили с помощью программ для статистического анализа Statistica 6.0 и Medcalc. При нормальном распределении показателя для первичного сравнения данных между группами использовали однофакторный дисперсионный анализ. Если не подтверждалась нормальность распределения, то применяли порядковые критерии Манна—Уитни для межгруппового сравнения и W-критерий Вилкоксона для оценки динамических наблюдений. Уровень достоверности был принят р<0,05. Корреляционный анализ проводили по методу Спирмена (ранговая корреляция).
Для определения прогностической значимости изучаемых маркеров воспаления выполняли логистический регрессионный анализ, применяли регрессионную модель пропорционального риска Кокса, а также анализ выживания по Каплану—Мейеру. При вычислении относительного риска (ОР) для каждого показателя выбирали референсное значение ОР, принимавшееся за 1,0. Строили 95% доверительные интервалы (ДИ) для средних и отношений шансов (ОШ). ОШ с 95% ДИ в однофакторном анализе рассчитывали в модели логистической регрессии с поправкой на возраст. Данные представлены в виде М±m (медиана±стандартная ошибка среднего). С помощью ROC-анализа были определены значения уровня MBL (и соответствующие значения чувствительности и специфичности), разделяющие выборку на 2 группы: с благоприятным и неблагоприятным исходом для каждой исследуемой конечной точки. Для моделирования выживаемости и определения прогностически значимых показателей (клинических, иммунологических) использовали регрессионную модель пропорционального риска Кокса.
Клиническая характеристика. Среди больных ОКС было 79% (61) мужчин и 21% (16) женщин. Средний возраст больных составил 58,6 года (от 29 до 83 лет). Сопутствующая артериальная гипертония выявлена у 68% больных, сахарный диабет — у 22%, гиперхолестеринемия — у 75%. У 21% (16) больных в анамнезе имелась ИБС (от 1 года до 15 лет), у 13% — ИМ, 2,6% (2) больных перенесли ранее операцию коронарного шунтирования, 9,1% (7) пациентам проводилось ЧКВ.
 Среди больных ОКС у 76% (59) диагностирован ОКСпST, у 24% (18) пациентов — ОКСбпST: 8% (6) – с нестабильной стенокардией, 16% (12) – с ИМ без подъема ST. У 50,6% (39) больных выявлен ИМ передней локализации. В 1-е сутки у 16,8% (13) больных имелись признаки СН. По тяжести проявлений СН больные распределились следующим образом: Killip I — 7,8% больных, Killip II — 3,9%, Killip III — 3,9%, Killip IV — 1,3%. У 2,6% (2) лечение симптомов недостаточности кровообращения сопровождалось искусственной вентиляцией легких. После выписки в среднем в течение 2 лет больные наблюдались на базе отделения неотложной кардиологии. Прогноз определен по количеству неблагоприятных исходов: смерть от кардиальных причин, развитие нефатального ИМ, повторной реваскуляризации и госпитализации с целью проведения ЧКВ или в связи с декомпенсацией кровообращения.
Среди больных ОКС у 76% (59) диагностирован ОКСпST, у 24% (18) пациентов — ОКСбпST: 8% (6) – с нестабильной стенокардией, 16% (12) – с ИМ без подъема ST. У 50,6% (39) больных выявлен ИМ передней локализации. В 1-е сутки у 16,8% (13) больных имелись признаки СН. По тяжести проявлений СН больные распределились следующим образом: Killip I — 7,8% больных, Killip II — 3,9%, Killip III — 3,9%, Killip IV — 1,3%. У 2,6% (2) лечение симптомов недостаточности кровообращения сопровождалось искусственной вентиляцией легких. После выписки в среднем в течение 2 лет больные наблюдались на базе отделения неотложной кардиологии. Прогноз определен по количеству неблагоприятных исходов: смерть от кардиальных причин, развитие нефатального ИМ, повторной реваскуляризации и госпитализации с целью проведения ЧКВ или в связи с декомпенсацией кровообращения.
За время наблюдения 6 (7,8%) пациентов скончались от сердечно-сосудистых причин, из них 1 (1,3%) умер в 1-е сутки госпитализации. У 6 (7,8%) больных за время наблюдения развился нефатальный ИМ. Повторная реваскуляризация за время наблюдения проведена 13 (16,8%) больным. Повторно госпитализированы в связи с развитием нестабильной стенокардии или СН 6,5% больных .
Результаты
В течение 2 лет у 12 (15,5%) больных развились неблагоприятные исходы (ИМ+ССС) — первичная конечная точка. Уровень MBL у больных с неблагоприятным исходом оказался достоверно выше, чем у пациентов с благоприятным исходом (2319±367 нг/дл против 813±151 нг/дл; p=0,02). Определялась прямая достоверная, однако слабая корреляция между уровнем MBL и прогнозом (r=0,268; p<0,05).
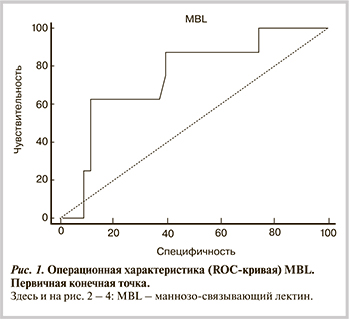
Значение, разделяющее уровень MBL для первичной конечной точки, составило 2273 нг/мл (чувствительность 62,5%, специфичность 87,5%). Площадь под ROC-кривой 0,734±0,106 (95% ДИ от 0,601 до 0,855). Уровень MBL >2273 нг/мл определял развитие неблагоприятного исхода (рис. 1).
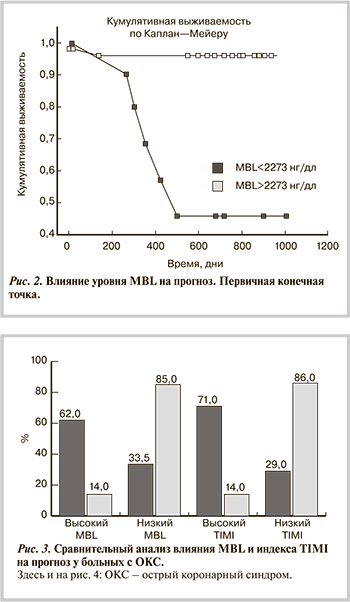
Высокий уровень MBL (>2273 нг/дл) достоверно (с использованием теста Кокса—Монтеля; p=0,0008) прогнозировал развитие неблагоприятных исходов у больных ОКС. При регрессионном анализе выживаемости ОР 19 (при 95% ДИ от 4,9 до 74,5; р=0,005), ОШ 22,8 (рис. 2).
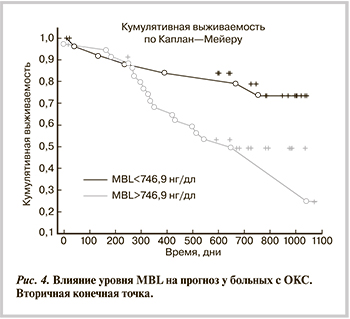
Мы сопоставили прогностическую способность MBL и индекса TIMI у больных ОКС. Индекс TIMI — один из общепринятых интегральных показателей для прогнозирования неблагоприятных исходов у больных ОКС. Рассчитывается по формуле ЧСС·(возраст/10)2/САД [21], где ЧСС — частота сердечных сокращений, САД — систолическое артериальное давление. Индекс TIMI >30 обусловливает высокий риск развития госпитальной смертности (>10%). Индекс TIMI был достоверно выше у больных с неблагоприятными исходами (27,5±6,9 и 19,6±1,3; р=0,02). При ROC-анализе значение, разделяющее индексы TIMI для первичной конечной точки, составило 27,2 (чувствительность 60%, специфичность 90%), площадь под кривой 0,726±0,070 при 95% ДИ от 0,596 до 0,833. Высокий индекс TIMI (>27,2) достоверно прогнозировал неблагоприятные исходы у больных ОКС (рис. 3).
Корреляции между уровнем MBL и индексом TIMI не выявлено, что позволяет рассматривать оба фактора как независимые друг от друга предикторы прогноза. В нашей выборке у 62% больных с уровнем MBL >2273 нг/мл и только у 14% с уровнем MBL<2273 нг/мл развились неблагоприятные исходы. У 71% больных с высоким индексом TIMI были осложнения. Таким образом, прогностическая способность MBL сопоставима с таковой индекса TIMI.
В течение 2 лет у 8 (13,6%) больных ОКСпST развились неблагоприятные исходы (ИМ+ССС) — первичная конечная точка. Уровень MBL у больных с неблагоприятным исходом оказался значительно выше, чем у пациентов с благоприятным исходом, однако различия были недостоверными. У больных ОКСпST с благоприятным и неблагоприятным исходом высокая концентрация MBL (>2273 нг/дл) достоверно прогнозировала неблагоприятные исходы (с использованием теста Кокса—Монтеля; p<0,01) с ОР 10,5.
В течение 2 лет у 3 (16,7%) больных ОКСбпST развились неблагоприятные исходы (ИМ+ССС) — первичная конечная точка. Уровень MBL у больных с неблагоприятным исходом оказался значительно выше, чем у пациентов с благоприятным исходом, однако различия были недостоверными (2291 и 693 нг/дл соответственно). В связи с небольшим числом наблюдений достоверно оценить влияние уровня MBL на прогноз у больных ОКСбпST не представляется возможным.
Неблагоприятные исходы (ИМ+ССС+госпитали-зация+реваскуляризация) развились в течение 2 лет у 30 (38,9%) больных ОКС. Уровень MBL у больных с неблагоприятным исходом оказался достоверно выше, чем у пациентов с благоприятным исходом (1177 и 690 нг/дл соответственно; p=0,04). Определялась прямая достоверная, однако слабая корреляция между уровнем MBL и прогнозом (r=0,255; p=0,04).
Значение, разделяющее уровень MBL для вторичной конечной точки, составило 746,9 нг/дл (чувствительность 76%, специфичность 53%). Площадь под кривой составила 0,646±0,076 (при 95% ДИ от 0,516 до 0,761). Высокий уровень MBL (>746,9 нг/дл) достоверно прогнозировал развитие неблагоприятных исходов с ОР 2,54 (при 95% ДИ от 1,046 до 6,172), р=0,03, ОШ 3,67 (рис. 4).
Среди больных ОКСпST вторичная конечная точка была зафиксирована у 28 (48%) пациентов. Уровень MBL достоверно не различался у больных ОКСпST с благоприятными и неблагоприятными исходами (1045±370 нг/дл против 746,9±153 нг/дл). Достоверного влияния уровня MBL на последующее развитие неблагоприятных исходов у больных ОКСпST не выявлено.
В течение 2 лет у 10 (55,5%) больных ОКСбпST развились неблагоприятные исходы (ИМ+ССС+реваскуляризация+повторная госпитализация). Уровень MBL у больных с неблагоприятными исходами оказался значительно выше, чем у пациентов с неосложненным течением, однако различия недостоверны (1352±353 нг/мл против 356±647 нг/мл; р>0,05). В связи с небольшим числом наблюдений достоверно оценить влияние уровня MBL на прогноз у больных ОКСбпST не представляется возможным.
От кардиальных причин (ССС) в течение 2 лет умерли 6 (7,8%) больных. Уровень MBL у больных, впоследствии умерших, был достоверно выше, чем у выживших (2338±257 нг/мл против 787±152 нг/мл; p=0,02). Определялась прямая достоверная умеренная корреляция между уровнем MBL и ССС (r=0,3; p=0,01).
Значение, разделяющее уровень MBL для конечной точки ССС, составило 976,5 нг/мл (чувствительность 100%, специфичность 60,3%). Площадь под кривой 0,802±0,111 (при 95% ДИ от 0,683 до 0,891). В связи с небольшим числом наблюдений достоверно оценить влияние уровня MBL на ССС у больных ОКС не представляется возможным. Однако можно отметить, что у всех 6 пациентов, умерших за период наблюдения, уровень MBL оказался выше 976,5 нг/мл.
Обсуждение
До настоящего времени нет четких данных о нормальном уровне MBL в крови. По разным источникам, он находится в пределах от 10 до 5000 нг/дл. В связи с этим мы использовали для анализа разные пороговые значения, вычисленные с помощью ROC-анализа для каждой конечной точки: 2238 нг/дл для первичной конечной точки, 746,5 нг/дл для вторичной конечной точки и 946,5 нг/дл для ССС. Вычисленные нами прогностические пороговые значения оказались сопоставимы с данными других исследований. Так, M. Trendelenburg и соавт. [22] использовали пороговое значение 1000 нг/дл.
 У многих авторов пороговые значения были значительно меньше (100 нг/дл в исследовании S. Saevarsdottir и соавт. [16]) или больше (800 мкг/л в исследовании S. Haahr-Pedersen и соавт. [23]). Такие различия можно в некоторой степени объяснить разными лабораторными наборами, использованными исследователями для определения уровня MBL Исследования прогностической значимости MBL у больных ОКС малочисленны. В литературе мы нашли несколько работ, в которых изучалась прогностическая ценность MBL. В основном в этих работах изучалось влияние MBL на реперфузионное повреждение миокарда. Наши данные оказались сходными с результатами этих работ. Так, М. Trendelenburg и соавт. при обследовании 890 больных острым ИМпST, которым проводилось первичное ЧКВ, показали значительное повышение летальности у больных с высоким уровнем MBL (>100 нг/мл) при сравнении с больными с низким уровнем MBL (<100 нг/мл) — 5,1 и 0,79% соответственно (р=0,02). По комбинированной конечной точке (смертность, кардиогенный шок, сердечная недостаточность — СН) различий в обеих группах выявлено не было. Авторы показали, что низкий уровень MBL связан со снижением частоты фатальных аритмий, не влияя на развитие СН.
У многих авторов пороговые значения были значительно меньше (100 нг/дл в исследовании S. Saevarsdottir и соавт. [16]) или больше (800 мкг/л в исследовании S. Haahr-Pedersen и соавт. [23]). Такие различия можно в некоторой степени объяснить разными лабораторными наборами, использованными исследователями для определения уровня MBL Исследования прогностической значимости MBL у больных ОКС малочисленны. В литературе мы нашли несколько работ, в которых изучалась прогностическая ценность MBL. В основном в этих работах изучалось влияние MBL на реперфузионное повреждение миокарда. Наши данные оказались сходными с результатами этих работ. Так, М. Trendelenburg и соавт. при обследовании 890 больных острым ИМпST, которым проводилось первичное ЧКВ, показали значительное повышение летальности у больных с высоким уровнем MBL (>100 нг/мл) при сравнении с больными с низким уровнем MBL (<100 нг/мл) — 5,1 и 0,79% соответственно (р=0,02). По комбинированной конечной точке (смертность, кардиогенный шок, сердечная недостаточность — СН) различий в обеих группах выявлено не было. Авторы показали, что низкий уровень MBL связан со снижением частоты фатальных аритмий, не влияя на развитие СН.
Происхождение данного феномена связывается со снижением реперфузионного повреждения миокарда, запускаемого с помощью MBL путем активации комплемента [22]. В небольшом исследовании у 74 больных ИМпST, которым проводили первичное ЧКВ, высокий уровень MBL оказался предиктором систолической дисфункции. Авторы предполагают, что высокая концентрация MBL приводит к выраженной активации комплемента и увеличению реперфузионного повреждения миокарда [23].Эти данные подтверждаются результатами исследований на животных. J. Jordan и соавт. показали, что при блокаде лектинового пути активации комплемента с помощью моноклональных антител к MBL зона реперфузионного повреждения миокарда вследствие экспериментального ИМ у мышей уменьшается [8]. Уменьшение зоны реперфузионного повреждения миокарда наступало за счет снижения нейтрофильной инфильтрации и снижения экспрессии провоспалительных генов [24]. М. Walsh и соавт. выявили, что у мышей со сниженным MBL зона реперфузионного повреждения миокарда ниже, чем у мышей с нормальным уровнем MBL. Авторы предположили, что активация комплемента именно по лектиновому пути является ключевым фактором в патогенезе реперфузионного повреждения миокарда. L. La Bonte и соавт. показали, что при терапии моноклональными антителами к MBL у мышей с экспериментальным ИМ на фоне сахарного диабета размер ИМ, уровень С3 комплемента и аккумуляция нейтрофилов оказалась значительно ниже, чем у мышей без этой терапии [25].
В нашем исследовании у всех больных ОКС высокий уровень MBL достоверно прогнозировал развитие неблагоприятных исходов по всем конечным точкам. У всех умерших больных уровень MBL был выше разделяющего значения (976 нг/мл). В нашем исследовании уровень MBL прогнозировал развитие неблагоприятных исходов по вторичной (комбинированной) конечной точке. Подобных данных в имеющейся литературе не найдено.
В нашей работе всем больным ОКСпST проведена реперфузионная терапия (ТЛТ или ЧКВ). У больных ОКСпST независимо от варианта реперфузионной терапии уровень MBL был достоверно выше при неблагоприятных исходах (смерть+ИМ). Высокий уровень MBL прогнозировал развитие неблагоприятных исходов в этой подгруппе больных, что может быть объяснено участием MBL в реперфузионном повреждении миокарда. Уровень MBL достоверно не прогнозировал достижения вторичной конечной точки у больных ОКСпST.
Обсуждается несколько механизмов возможного участия MBL в атерогенезе и тромбообразовании. Во-первых, MBL, запуская лектиновый путь активации комплемента, является одним из триггеров воспалительной реакции. Его мембранно-атакующие комплексы обнаружены в поврежденных кардиомиоцитах при ИМ. Есть данные, что активация комплемента повышает риск развития сердечно-сосудистых осложнений у больных распространенным атеросклерозом. Отложение комплемента iC3b в нестабильных бляшках приводит к увеличению риска развития ОКС, по-видимому, за счет усиления воспалительной реакции и увеличения риска тромбообразования. Кроме того, оксидантный стресс, играющий ключевую роль в патогенезе ОКС, активирует комплемент через лектиновый путь в культуре клеток.
В нашей работе уровень MBL обладал приблизительно той же прогностической силой, что и одна из основных шкал для стратификации риска у больных ОКС — индекс TIMI, что является дополнительным свидетельством прогностической силы MBL. Достаточно длительный период наблюдения в нашей работе (2 года) позволяет с определенной основательностью говорить о MBL как о новом прогностическом маркере у больных ОКС.
Вместе с тем положительный результат пилотного исследования, которым является представленная работа, предполагает проведение крупных исследований с длительным периодом наблюдения. Кроме того, полученные результаты могут служить основанием для изучения ингибиторов MBL как средств, улучшающих прогноз у больных ОКС.
Заключение
Повышение концентрации маннозо-связывающего лектина в сыворотке крови больных острым коронарным синдромом является неблагоприятным прогностическим фактором. Для определения долгосрочного прогноза у больных острым коронарным синдромом в дополнение к известным факторам риска рекомендуется определение уровня маннозо-связывающего лектина в первые сутки от начала заболевания.



