Наличие кальция в коронарных артериях является характерным признаком атеросклероза. Процессы атеросклероза и кальциноза артерий взаимосвязаны и протекают синхронно [1]. В качестве стандартизированного метода количественной оценки коронарного кальция применяется кальциевый индекс (КИ), рассчитываемый по методу Агатсона [2]. На современном этапе КИ определяется, как правило, при выполнении мультиспиральной компьютерной томографии (МСКТ). Выявление и количественная оценка коронарной кальцификации имеют важное значение для определения субклинического атеросклероза и прогноза у бессимптомных лиц, что, по-видимому, может улучшить диагностику сердечно-сосудистых заболеваний (ССЗ), которые остаются основной причиной смерти в России [3]. Кроме того, в последнее время возрастает интерес к определению КИ не только у бессимптомных лиц, но и у пациентов с подозрением на ишемическую болезнь сердца (ИБС), а также у пациентов с некардиальной патологией.
В данном обзоре представлены результаты современных исследований прогностической значимости КИ и его роли в выборе профилактических программ у бессимптомных лиц, а также клинического значения КИ при обследовании больных с вероятной ИБС. Кроме того, представлены данные о взаимосвязи КИ с раком, деменцией и некоторыми другими хроническими неинфекционными заболеваниями.
КАЛЬЦИЕВЫЙ ИНДЕКС И СЕРДЕЧНО-СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ: ЗНАЧЕНИЕ ДЛЯ БЕССИМПТОМНЫХ ЛИЦ И ДОЛГОСРОЧНЫЙ ПРОГНОЗ
В современной практике сканирование кальция в коронарных артериях служит важным методом прогнозирования ССЗ в первую очередь у бессимптомных лиц [4]. В последние годы было выполнено несколько крупномасштабных исследований (CARDIA, The Walter Reed Cohort Study, MESA, The CAC Consortium), на основании которых проведена оценка долгосрочного прогноза КИ с периодом наблюдения более 10 лет у бессимптомных пациентов [5–9].
Mitchell J.D. et al., изучив когорту пациентов из 23 637 людей без известных ССЗ со средним периодом наблюдения 11,4 года, установили, что оценка КИ значительно улучшала точность прогнозирования отдаленных исходов ИБС, инсульта и общей смертности у лиц с низким сердечно-сосудистым риском. Отмечено, что среди лиц без каких-либо традиционных факторов риска (ФР) наличие кальция в коронарных артериях (КИ >0) было достоверно и независимо связано со значительно повышенной вероятностью основных неблагоприятных сердечно-сосудистых событий. Кроме того, авторы указывают, что КИ тесно ассоциирован с риском коронарной реваскуляризации в течение 90 дней после сканирования кальция [5]. Несколько ранее в исследовании CARDIA сообщалось, что у людей молодого возраста (средний возраст 40 лет) с любым КИ >0 угроза развития сердечно-сосудистых осложнений (ССО) увеличивалась в 3 раза при средней продолжительности наблюдения в 12,5 лет [6].
При анализе многоцентровой когорты The CAC Consortium, включающей 66 636 участников без ИБС, за время наблюдения в среднем 12,5 лет были получены следующие результаты: участники с показателем КИ ≥400 имели значительно повышенный риск смертности от ИБС и ССЗ по сравнению с пациентами с КИ=0. Лица без ФР, но с КИ ≥400 имели значительно более высокие показатели смертности по сравнению с участниками, имевшими 3 и более ФР, но без коронарного кальциноза (КИ=0). При более высоких значениях КИ большая доля от общего числа смертей приходилась на сердечно-сосудистые причины. Отсутствие коронарного кальциноза выявило лиц с низким риском событий в течение 12 лет наблюдения, при этом большинство смертей не было связано с ССЗ [7].
В исследовании MESA с участием 6814 пациентов без клинических проявлений ИБС и длительностью наблюдения 11,1 лет проводилась оценка взаимосвязи КИ и сердечно-сосудистых событий. Частота кардиоваскулярных осложнений в группах при КИ=0 варьировала от 1,3 до 5% и существенно возрастала у пациентов с КИ ≥100; в частности, при КИ >300 частота событий была примерно в 10 раз выше и составляла 13,1–25,6% независимо от возраста, пола или этнической принадлежности [8].
Valenti V. et al. продемонстрировали, что у лиц, относящихся к группе высокого риска по клиническим шкалам, отсутствие коронарного кальция обеспечивает лучшую выживаемость, чем у лиц с низким и средним риском, но с КИ >0. Уровень КИ=0 у людей с низким и средним риском свидетельствует о крайне низкой вероятности смерти от ССЗ в течение 15 лет [9].
Для расчета 10-летней вероятности развития ИБС у пациентов, не имеющих симптомов, наиболее часто используются традиционные шкалы (например, Framingham Risk Score, Systematic Coronary Risk Evaluation), основанные на определении установленных факторов сердечно-сосудистого риска (пол, возраст, артериальная гипертензия, дислипидемия, сахарный диабет и курение). Выявление коронарного кальциноза в сочетании с традиционными шкалами позволяет значительно точнее определить индивидуальный прогноз развития ИБС [10].
КАЛЬЦИЕВЫЙ ИНДЕКС И ТАКТИКА ВЕДЕНИЯ БЕССИМПТОМНЫХ ЛИЦ
Получены данные, что у бессимптомных лиц выявление повышенного КИ может служить руководством к началу первичной профилактики, включая прием статинов. Отсутствие коронарного кальция может быть основанием для того, чтобы отложить медикаментозное лечение [11], тогда как высокий КИ может служить аргументом в пользу более агрессивной терапии.
Пациенты с КИ=0 и отсутствием таких ФР, как курение, сахарный диабет (СД), семейный анамнез ранних ССЗ, имеют низкий риск сердечно-сосудистых осложнений; отказ от назначения статинов обеспечивает более индивидуализированный подход к ведению таких пациентов, позволяет избежать лишних финансовых затрат и возможных побочных эффектов, связанных с приемом этой группы препаратов [12]. Это положение подтверждается рядом крупных исследований, демонстрирующих, что КИ позволяет выявить пациентов как с наибольшей, так и наименьшей пользой от терапии статинами [13–15], в том числе и среди больных пожилого возраста [16].
Отмечено, что КИ имеет значение не только для начала гиполипидемической терапии, но и может играть важную роль в выборе целевых уровней холестерина. Martin S.S. et al. отмечают, что бессимптомные пациенты с КИ ≥100 независимо от показателей липидного обмена имеют частоту сердечно-сосудистых осложнений, близкую к больным с наличием ССЗ, которым проводится вторичная профилактика. Из этого, по мнению авторов, следует, что у таких пациентов при назначении статинов для первичной профилактики предпочтителен более низкий целевой уровень холестерина липопротеинов низкой плотности (ХС ЛПНП), а именно <1,8 ммоль/л [15]. Аналогичные выводы были сделаны в исследовании Blaha M.J. для пациентов с очень высоким индексом КИ (>300), у которых при наличии выраженного субклинического атеросклероза еще не диагностированы ССЗ: интенсивность гиполипидемической терапии и целевые уровни холестерина у них не должны существенно отличаться от терапии, проводимой в группе больных с наличием ССЗ [17].
Определение кальция в коронарных артериях с целью решения вопроса о назначении статинов нашло отражение и в современных международных клинических рекомендациях. В американских рекомендациях (AHA/ACC) по первичной профилактике ССЗ целесообразность оценки КИ отмечена для пациентов с пограничным и промежуточным 10-летним риском ССЗ, когда в ходе клинической оценки вопрос о приеме статинов остается неясным [18]. Европейское кардиологическое общество (ECS) рекомендует определять КИ для принятия решения о старте медикаментозной гиполипидемической терапии у пациентов низкого и умеренного риска, у которых не удается достичь целевых значений ХС ЛПНП с помощью немедикаментозных воздействий [19].
В ряде исследований отмечена роль коронарного кальция в определении целевых показателей артериального давления (АД) с учетом сердечно-сосудистого риска. В работе Parcha V. et al. показана связь между КИ, риском возникновения кардиоваскулярных осложнений и показателями АД. Пациенты с КИ >0 имели повышенный риск сердечно-сосудистых осложнений даже при оптимальном уровне АД (<120/80 мм рт.ст.), и с увеличением показателей АД этот риск нарастал. При КИ=0 вероятность развития ССЗ была существенно ниже как при оптимальном АД, так и при более высоких его показателях (120–139/80–89 мм рт.ст.). В работе подчеркнуто, что выявление коронарного кальциноза (КИ >0) является эффективным инструментом для определения лиц с высоким риском возникновения ИБС, инсульта и сердечной недостаточности, и эти лица могут получить выгоду от антигипертензивной фармакотерапии даже в отсутствии повышенных цифр АД (>140/90 мм рт.ст., а именно при показателях 120–139/80–89 мм рт.ст.) [20].
Подходы к персонализации целевых уровней АД у больных с промежуточным риском развития ССЗ и систолическим АД 120–159 мм рт.ст. продемонстрированы в исследовании McEvoy J.W. et al. Выявление КИ >100 среди пациентов данной группы помогает выявить лиц, которые получат пользу от антигипертензивной терапии с целевым САД <120 мм рт.ст., тогда как при КИ=0 сохраняются традиционные целевые показатели систолического АД <140 мм рт. ст. Это позволяет избежать ненужной интенсификации лекарственной терапии [21].
ЗНАЧЕНИЕ ЭКСТРЕМАЛЬНО ВЫСОКОГО КАЛЬЦИЕВОГО ИНДЕКСА
На современном этапе лиц с КИ >400, как правило, рассматривают как группу наивысшего риска ССЗ без дальнейшей дифференциации выше этого порога. Однако в последнее время появляются исследования, демонстрирующие необходимость выделения в отдельную группу пациентов с обширной кальцификацией коронарных сосудов и экстремально высоким значением КИ, а именно ≥1000.
Проведен детальный анализ бессимптомных пациентов с КИ ≥1000 (n=2869) на основании данных многоцентровой когорты The CAC Consortium. Сообщается, что экстремальные значения КИ (≥1000) связаны со значительно повышенным риском ССЗ, ИБС, рака и общей смертности, причем угроза смерти от ССЗ у таких лиц почти в 2 раза выше по сравнению с пациентами, имеющими КИ от 400 до 999. Более того, большинство больных с КИ ≥1000 имели более рассредоточенный характер кальцификации в коронарных артериях: отложения кальция у многих наблюдались в 3–4 сосудах, имелась большая общая площадь поражения и плотность кальцификации, а также отмечалось более диффузное распределение внекоронарного кальциноза при сравнении с пациентами с КИ=400–999 [22]. Аналогичные данные были получены в исследовании MESA: у бессимптомных лиц с КИ ≥1000 также был уставнолен значительно высокий риск сердечно-сосудистых осложнений и общей смертности [23].
Результаты проведенных исследований позволяют предположить, что бессимптомные лица с экстремально высоким КИ (≥1000) представляют собой особую группу лиц с существенно более высоким риском неблагоприятных сердечно-сосудистых событий, соизмеримым с пациентами, уже имеющими ССЗ, которым проводится вторичная профилактика ИБС. Рассматривается возможность выделения пациентов с КИ ≥1000 в отдельную группу риска в будущих клинических рекомендациях, поскольку этим больным может быть полезна более агрессивная профилактическая терапия [22, 23].
Таким образом, на сегодняшний день существует большая доказательная база по высокой прогностической значимости КИ у бессимптомных лиц независимо от наличия традиционных факторов сердечно-сосудистого риска. КИ помогает определить индивидуальный прогноз, что, в свою очередь, дает возможность персонализировать профилактические мероприятия, включая применение лекарственной терапии.
РОЛЬ КАЛЬЦИЕВОГО ИНДЕКСА У ПАЦИЕНТОВ С ПОДОЗРЕНИЕМ НА ИШЕМИЧЕСКУЮ БОЛЕЗНЬ СЕРДЦА
У больных с симптомами ИБС значение КИ оценивается неоднозначно, в отличие от бессимптомных лиц, однако в ряде исследований показано, что определение коронарного кальция может иметь определенную пользу и в данной группе пациентов. Нулевой показатель КИ имеет благоприятный прогноз не только для бессимптомных пациентов, но и больных с симптомами ИБС [24–27].
Большой интерес представляет использование КИ как показателя, определяющего тактику дальнейшего неинвазивного тестирования больных с подозрением на ИБC [28, 29]. На современном этапе при обследовании пациентов с предполагаемой ИБС делается акцент на визуализирующих диагностических методах. В ряде исследований совместно выполнялись оценка КИ и стрессовая визуализация перфузии миокарда [24, 30, 31]. В исследовании Engbers E.M. et al. было показано, что выявление и коронарного кальциноза (КИ >0), и ишемии миокарда по данным однофотонной эмиссионной компьютерной томографии (ОФЭКТ) у больных с подозрением на ИБС тесно связано с прогнозом серьезных неблагоприятных сердечно-сосудистых событий, а сочетание результатов перфузии миокарда c оценкой КИ дает дополнительную информацию о степени поражения коронарных артерий. Также было продемонстрировано, что у пациентов с симптомами ИБС оценка КИ служит предиктором кардиоваскулярных осложнений независимо от результатов ОФЭКТ. Такая закономерность наблюдалась как при отсутствии коронарной кальцификации (при КИ=0 частота отдаленных неблагоприятных событий была низкой независимо от наличия дефектов перфузии), так и при повышенных значениях КИ, ассоциированных с высоким сердечно-сосудистым риском. Кроме того, авторы отметили, что уровень КИ – более сильный предиктор выявляемых изменений перфузии миокарда, чем такие традиционные ФР, как возраст, сахарный диабет и артериальная гипертензия (АГ). По мнению авторов работы, у пациентов с сомнительными или небольшими дефектами перфузии миокарда, но высоким КИ может быть рассмотрена ранняя инвазивная стратегия в связи с повышенным риском кардиоваскулярных осложнений [24].
Аналогичные результаты были получены в более раннем исследовании на небольшой группе пациентов с сохраненной перфузией по ОФЭКТ, но наличием экстремально высокого КИ (>1000). Дополнительное обследование позволило выявить ИБС у данной группы пациентов [30].
В более позднем исследовании на основе анализа данных около 15 000 пациентов с подозрением на ИБС его авторы (Engbers E.M. et al.) рекомендуют использовать уровень коронарного кальция в качестве показателя, определяющего последующее диагностическое обследование: при КИ=0 дополнительная визуализация не требуется; при КИ 1–599 предлагается рассмотреть проведение МСКТ-коронарография из-за ее высокой отрицательной прогностической ценности для этих пациентов; при КИ 600–999 предпочтительно выполнение визуализирующий перфузионных методик; при обширной коронарной кальцификации (КИ>1000) предлагается рассмотреть выполнение селективной коронарографии [31].
Совместная оценка коронарного кальция и результатов обследования современным визуализирующим методом позитронно-эмиссионной томографии (ПЭТ) со стресс-тестированием у 5528 пациентов с клиническими проявлениями, но без ранее диагностированной ИБС проводилась в работе Le V.T. et al. Эта высокочувствительная, но дорогостоящая методика обычно используется для обнаружения тяжелой распространенной ишемии миокарда с последующим направлением на реваскуляризацию. Было показано, что в группе пациентов без кальция в коронарных артериях (n=3018), по сравнению с группой с КИ >0 (n=2510), реже выявлялась выраженная ишемия миокарда >10% (1,7 и 6,1% соответственно), обструктивное поражение сосудов (0,5 против 6,5%; p <0,0001), а также реже проводилась коронарная ангиография (3,4 против 10,2%; p <0,0001) и возникала необходимость в проведении реваскуляризации (0,4 против 5,8%, p <0,0001). Отдаленные сердечно-сосудистые осложнения (период наблюдения – 4 года) также встречались существенно реже в группе с КИ=0 (2,4 против 6,9%). Авторы подчеркивают большой потенциал КИ как инструмента скрининга у пациентов с симптомами ИБС для выявления лиц, кому не потребуется дальнейшее выполнение диагностического обследования, включая дорогостоящие методы. Необходимо выполнение крупных проспективных исследований, уточняющих роль КИ в обследовании больных с вероятной ИБС [32].
В то же время в ряде работ было показано, что, несмотря на низкую частоту кардиоваскулярных осложнений в будущем, КИ=0 не имеет достаточной отрицательной прогностической ценности для стратификации риска пациентов с подозрением на ИБС, если используется в качестве единственного маркера. Несмотря на отсутствие коронарного кальциноза, от 1,4 до 7% пациентов с симптомами имеют обструктивное поражение коронарных артерий [25, 26, 33].
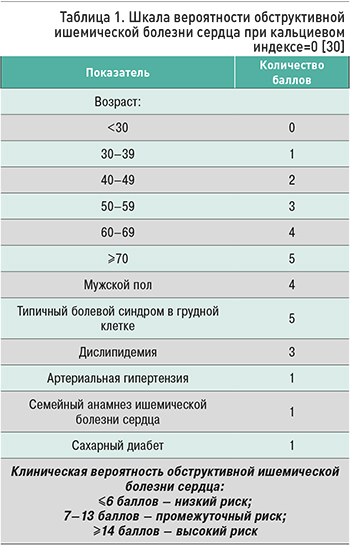 Alshahrani A.M. et al. в 2019 г. провели ретроспективный анализ 4290 пациентов с подозрением на ИБС, имеющих КИ=0. У всех больных были оценены факторы сердечно-сосудистого риска (возраст, пол, наличие типичного болевого синдрома в грудной клетке, дислипидемия, АГ, семейный анамнез ССЗ, СД) и выполнена МСКТ коронарных артерий. При обнаружении коронарного стеноза не менее 50% диагностировали обструктивную форму ИБС. На основании результатов исследования была разработана специальная шкала для определения вероятности обструктивной ИБС и необходимости в дополнительном обследовании у пациентов с подозрением на ИБС и отсутствием коронарной кальцификации (табл. 1). В зависимости от суммы баллов по предлагаемой шкале были выделены 3 группы: низкого риска (≤6 баллов), промежуточного риска (7–13 баллов) и высокого риска (≥14 баллов). При низком риске наличие обструктивной ИБС можно исключить с высокой степенью уверенности (отрицательная прогностическая ценность 99%). При высоком риске вероятность обструктивного поражения коронарных артерий была высокой (специфичность показателя 98%). В зависимости от количества баллов авторы предлагают алгоритм дальнейшего обследования больных с КИ=0: если баллов ≤6, то нет необходимости выполнять дальнейшее обследование; если ≥7, то проведение обследования рекомендуется (МСКТ-коронарография или другое тестирование), так как нельзя исключить обструктивную ИБС. Авторы отмечают, что пациенты с подозрением на ИБС с КИ=0 представляют неоднородную группу с различной степенью выраженности коронарной патологии, и это диктует разные подходы к их дальнейшему обследованию. Разработанная шкала помогает выявлять больных с различным риском, однако ее необходимо валидизировать в проспективных исследованиях [34].
Alshahrani A.M. et al. в 2019 г. провели ретроспективный анализ 4290 пациентов с подозрением на ИБС, имеющих КИ=0. У всех больных были оценены факторы сердечно-сосудистого риска (возраст, пол, наличие типичного болевого синдрома в грудной клетке, дислипидемия, АГ, семейный анамнез ССЗ, СД) и выполнена МСКТ коронарных артерий. При обнаружении коронарного стеноза не менее 50% диагностировали обструктивную форму ИБС. На основании результатов исследования была разработана специальная шкала для определения вероятности обструктивной ИБС и необходимости в дополнительном обследовании у пациентов с подозрением на ИБС и отсутствием коронарной кальцификации (табл. 1). В зависимости от суммы баллов по предлагаемой шкале были выделены 3 группы: низкого риска (≤6 баллов), промежуточного риска (7–13 баллов) и высокого риска (≥14 баллов). При низком риске наличие обструктивной ИБС можно исключить с высокой степенью уверенности (отрицательная прогностическая ценность 99%). При высоком риске вероятность обструктивного поражения коронарных артерий была высокой (специфичность показателя 98%). В зависимости от количества баллов авторы предлагают алгоритм дальнейшего обследования больных с КИ=0: если баллов ≤6, то нет необходимости выполнять дальнейшее обследование; если ≥7, то проведение обследования рекомендуется (МСКТ-коронарография или другое тестирование), так как нельзя исключить обструктивную ИБС. Авторы отмечают, что пациенты с подозрением на ИБС с КИ=0 представляют неоднородную группу с различной степенью выраженности коронарной патологии, и это диктует разные подходы к их дальнейшему обследованию. Разработанная шкала помогает выявлять больных с различным риском, однако ее необходимо валидизировать в проспективных исследованиях [34].
Прогностическая значимость КИ у стабильных пациентов с вероятной ИБС проанализирована в недавно опубликованном метаанализе, в который вошел 34 041 пациент из 19 наблюдательных исследований. Было определено, что повышенные уровни КИ у пациентов с клиническими проявлениями ИБС достоверно и независимо связаны с высоким риском неблагоприятных сердечно-сосудистых событий. С увеличением КИ отмечено возрастание угрозы событий, причем выявленная закономерность сохранялась после коррекции с учетом клинических ФР, включая возраст, мужской пол, АГ, СД, дислипидемию и курение. Отсутствие коронарного кальция было связано с низким риском будущих кардиоваскулярных осложнений у пациентов с подозрением на ИБС [35].
С учетом вышеизложенного следует отметить, что для пациентов с вероятной ИБС оценка КИ может быть важным дополнительным инструментом при выборе тактики обследования. Отсутствие кальция в коронарных артериях даже при наличии симптомов у большинства пациентов ассоциировано с низким риском сердечно-сосудистых осложнений.
КАЛЬЦИЕВЫЙ ИНДЕКС И НЕКАРДИАЛЬНАЯ ПАТОЛОГИЯ
Исследования по изучению прогностической значимости коронарного кальциноза для некардиальной патологии немногочисленны. Анализ этой взаимосвязи был проведен на основании базы данных исследования MESA, вобравшего 6814 пациентов. Случаи впервые диагностированных заболеваний включали рак, хроническую болезнь почек (ХБП), пневмонию, хроническую обструктивную болезнь легких (ХОБЛ), перелом шейки бедра, деменцию и тромбоз глубоких вен голени. Выявлено, что у пациентов с высоким КИ >400, наряду с повышением риска ССЗ на 471%, наблюдается существенное повышение опасности развития некардиальной патологии, а именно рака на 53%, ХБП – на 70%, пневмонии – на 197%, ХОБЛ – на 271% и риска перелома шейки бедра – на 429%, в сравнении с больными, у которых коронарный кальций отсутствует (КИ=0). При увеличении КИ риск новых случаев вышеуказанных заболеваний значимо возрастал от 11% при КИ=0 до 36,9% при КИ >400. У пациентов с отсутствием коронарного кальция отмечен низкий риск некардиальной патологии по сравнению с пациентами, имеющими КИ >0. В возрасте >65 лет удвоение КИ было связано со статистически значимым увеличением как сердечно-сосудистой, так и другой патологии [36].
В 2021 г. был представлен дополнительный анализ результатов той же базы данных исследования MESA по взаимосвязи экстремально высокого КИ (>1000) с некардиальной патологией [24]. Как и ожидалось, пациенты с КИ >1000 были старше, среди них было больше мужчин, больше лиц, принимавших антигипертензивные препараты и чаще имеющих отягощенную наследственность по инфаркту миокарда. Авторы отметили еще более высокую угрозу возникновения любой некардиальной патологии, особенно рака, ХБП, пневмонии и деменции в сравнении с результатами, представленными по группе пациентов с КИ >400 [36].
Имеются данные, что высокий КИ ассоциирован с повышением риска не только возникновения некардиальных заболеваний, но и смертности от них [36, 37].
Особый интерес представляют исследования по связи КИ и онкологических заболеваний. В одной из ранних работ [39] было продемонстрировано, что при наблюдении 130 пациентов более 1 года почти у четверти больных (23%) с экстремально высоким КИ>1000 диагностировали рак. Данный показатель (КИ >1000) был отмечен у 50% больных с выявленным раком и только у 17% больных без рака (р=0,014).
В другом исследовании было показано, что частота выявления новых случаев рака значимо возрастала не только при экстремальных значениях КИ. У бессимптомных больных с КИ=0, 1–400 и >400 частота выявления рака составляла 6,7, 12,6 и 20,4% соответственно. У пациентов с КИ>400 риск выявления рака был на 53% выше по сравнению с пациентами с КИ=0 (p <0,001). Частота выявления различных видов рака в данном исследовании составляла: 21% – рак простаты; 14% – рак легких; 13% – рак желудочно-кишечного тракта; 10% – рак молочной железы; 9% – рак кожи; 6% – онкогематология; 5% – рак матки/яичников. Скорректированные по полу показатели не выявили связи между КИ и видом рака [36].
КИ является важным показателем для выработки оптимальной тактики ведения больных с раком молочной железы. Среди 15 919 женщин (средний возраст 58 лет), получавших лучевую терапию в связи с этим заболеванием, КИ оценивали при предварительном проведении компьютерной томографии (КТ) для планирования лучевой терапии. Отсутствие коронарной кальцификации было выявлено у 70% женщин. Высокие значения КИ >400 наблюдались у 3% больных. За время наблюдения (52 мес) риск ССЗ (инфаркта миокарда, инсульта, сердечной недостаточности) составил 5% при КИ=0 и 28% при КИ >400. Аналогичные показатели были получены и при анализе общей смертности: 7 и 28% при КИ=0 и КИ >400 соответственно. Наиболее выраженная связь была отмечалась при лечении антрациклинами. У женщин с КИ >400 угроза развития ССЗ была в 6 раз выше, по сравнению с больными с КИ=0, не получавшими антрациклины. При обсуждении результатов этого исследования было подчеркнуто, что у ряда пациентов риск умереть от ССЗ выше, чем от рака молочной железы; это необходимо учитывать при выборе тактики ведения [39].
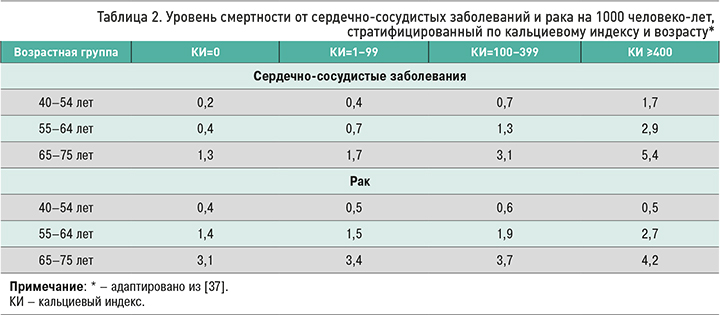
Связь КИ с возрастом и летальностью от двух ведущих причин смертности (ССЗ и рака) проанализирована в недавнем исследовании Whelton S.P. et al. на основании данных 59 502 бессимптомных пациентов 40–75 лет (средний возраст 54 года) без ССЗ с выполненным сканированием КИ [37]. За период наблюдения (в среднем 12,3 года) был зарегистрирован 671 случай смерти от ССЗ и 954 случая смерти от рака. У больных 40–54 лет при КИ=0 отмечалась очень низкая смертность как от ССЗ, так и от рака. С увеличением возраста наблюдалось возрастание КИ. Уровень смертности от ССЗ увеличивался с нарастанием КИ во всех возрастных группах (40–54, 55–64 и 65–75 лет). Уровень смертности от рака у пациентов моложе 55 лет не был связан с КИ и оставался относительно стабильным, а у пациентов старше 55 лет возрастал: в 1,9 раз в группе 55–64 года и в 1,4 раза в группе 65–75 лет при увеличении КИ от 0 до >400 (табл. 2). Показатель смертности от ССЗ превышал показатель смертности от рака при КИ >100 у молодых (40–54 года) и при КИ >400 у пожилых (65–75 лет). При КИ >400 сердечно-сосудистая смертность превышала смертность от рака для всех возрастных групп. С учетом выявленной закономерности авторы исследования предлагают расчет индивидуального показателя КИ, определяющего риск смерти от ССЗ и рака, что, по их мнению, позволит разрабатывать профилактические мероприятия в обоих направлениях.
Отдельные работы были посвящены изучению ассоциации между повышением КИ и снижением когнитивных функций. На основании базы данных исследования MESA показана положительная связь КИ и риска деменции. В сравнении с пациентами, не имеющими коронарной кальцификации (КИ=0), при увеличении КИ риск деменции возрастал на 23, 35 и 71% у пациентов с КИ 1–400, 401–1000 и >1000 соответственно. Выявленная связь частично могла быть обусловлена развитием ССЗ, включая перенесенный инсульт, однако оставалась значимой (p=0,026) после исключения инсультов и не была связана с возрастом, аполипопротеином Е4 (генотипом болезни Альцгеймера) и сосудистыми ФР [40].
При анализе связи КИ и риска развития деменции у пациентов старшего возраста (80+), включенных в исследование CHS Cognition Study, установлено, что частота деменции в данной возрастной группе превышала частоту ИБС. У женщин с КИ=0 встречаемость деменции была в 3 раза ниже относительно женщин с КИ>400 (р=0,04). Для мужчин достоверной связи не прослеживалось. Следует отметить, что данная ассоциация была выявлена на небольшой группе больных в связи с нечасто наблюдаемым низким КИ среди пациентов старше 80 лет [41]. Связь КИ с нарушением когнитивных функций была проанализирована в нидерландском исследовании ImaLife, включающем 4988 пациентов без ранее диагностированных ССЗ. Обнаружено ухудшение показателей оперативной памяти при увеличении КИ у пациентов старше 45 лет вне зависимости от традиционных ФР ССЗ, причем наиболее выраженная связь отмечалась в возрасте 45–54 лет. Ухудшение оперативной памяти наблюдается при различных нейродегенаративных заболеваниях, включая болезнь Альцгеймера и сосудистую деменцию. Авторы подчеркивают необходимость дальнейших исследований, определяющих прогностическую значимость КИ для раннего диагностирования когнитивных нарушений и риска деменции [42].
В современных условиях пандемии новой коронавирусной инфекции итальянскими исследователями проанализирована прогностическая значимость коронарного кальциноза у 1093 госпитализированных больных с подтвержденной инфекцией COVID-19. Кальциноз коронарных артерий определяли при госпитализации во время проведения КТ грудной клетки для выявления поражения легких. По результатам исследования показано, что у пациентов, умерших в стационаре, достоверно чаще по сравнению с выжившими определялось наличие коронарной кальцификации c КИ >0 (85,3 и 62,8%; p <0,001), более высокое значение КИ (467,76±570,92 и 206,80±424,13; p <0,001), большее число коронарных артерий с наличием кальциноза (2 и 1; p <0,01) и больший объем коронарного кальциноза (487,79±565,34 и 207,77±406,81 мм3; p <0,001). Чувствительность показателя объема коронарного кальция в прогнозировании госпитальной летальности была 96%, специфичность – 33%. Авторы делают вывод, что определение КИ может быть полезным инструментом для стратификации риска госпитализированных больных с COVID-19 [43].
ЗАКЛЮЧЕНИЕ
Подводя итоги вышеизложенному, следует отметить, что большинство современных исследований по коронарному кальцию демонстрируют связь КИ с различными заболеваниями, включая как сердечно-сосудистую, так и некардиальную патологию. КИ увеличивается с возрастом. Традиционно он рассматривается как биомаркер коронарного атеросклероза, отражающий воздействия ФР ССЗ на стенку коронарной артерии, что обеспечивает дополнительную ценность данного показателя для прогнозирования кардиоваскулярных событий и для тактики ведения больных с ССЗ атеросклеротического генеза.
Выявление связей КИ с некардиальной патологией позволяет расширить традиционные представления о значимости этого показателя. Многие хронические неинфекционные болезни имеют общие ФР с сердечно-сосудистой патологией. Высказывается предположение, что КИ может выступать интегральным ФР, который отражает влияние как известных (измеряемых), так и неизвестных ФР, действующих на протяжении всей жизни [41]. Таким образом, КИ, возможно, является маркером, отражающим не только сосудистый, но и более общий – биологический возраст, что позволяет оценивать индивидуальный риск различных заболеваний. Интерес к изучению КИ возрастает. Необходимы дальнейшие исследования для уточнения прогностической и клинической значимости коронарного кальция при различной патологии.



