В конце 2023 г. под эгидой Российского научного медицинского общества терапевтов (РНМОТ) состоялся Совет экспертов, который был посвящен рассмотрению проблем, связанных с недостаточностью и дефицитом магния в организме человека, неблагоприятным последствиям такого дефицита и мерам по их предупреждению и коррекции.
Магний – второй по распространенности катион в клетках человека (после K+) и четвертый по распространенности элемент в организме в целом (после кальция, калия и натрия). Основная часть магния (более 99% от общего количества) находится во внутриклеточном пространстве, а основным его депо служат скелетная система/кости, на которые приходится примерно 50–65% всего Mg2+ в организме. В сочетании с кальцием и фосфором он формирует структурный состав скелета [1].
Магний значимо влияет на активность аденилатциклазы, необходимой для образования циклического аденозинмонофосфата (цАМФ), который, в свою очередь, участвует в секреции паратиреоидного гормона (ПТГ) и реализации его эффектов в отношении органов-мишеней. Большую роль в гомеостазе Mg2+, наряду с ПТГ, играют витамин D и эстроген [2].
Магний выступает кофактором на определенных этапах метаболизма витамина D. Дефицит Mg2+ может приводить к снижению количества доступных рецепторов этого витамина в целевых клетках [3].
В целом магний является кофактором в более чем 600 ферментативных реакциях [4] и незаменимым компонентом основных процессов, протекающих в клетках, включая энергетический обмен, апоптоз и пролиферацию. Он модулирует активность ферментов, участвующих в гликолизе, цикле Кребса и дыхательной цепи [5]. Доступность Mg2+ критически важна для углеводного обмена, что может объяснить его роль в развитии сахарного диабета 2-го типа (СД 2) [6]. Магний необходим для формирования правильной структуры и активности ДНК- и РНК-полимераз [7, 8], нормальной работы топоизомераз, хеликаз, экзонуклеаз и различных групп АТФаз; соответственно, он играет значимую роль в репликации ДНК, транскрипции РНК и образовании белков, участвуя в контроле клеточной пролиферации. Более того, Mg2+ имеет решающее значение для поддержания геномной и генетической стабильности, стабилизации естественной конформации ДНК и служит кофактором почти для каждого фермента, вовлеченного в эксцизионную репарацию нуклеотидов и оснований и репарацию ошибочно спаренных нуклеотидов. Учитывая эти эффекты, низкая доступность Mg2+ может быть связана с риском развития рака [9].
Концентрации магния в сыворотке крови тесно связаны с костным метаболизмом, поскольку в организме происходит постоянная замена Mg2+ с поверхности кости на Mg2+ крови [10, 11]. Последствиями его дефицита становятся ускоренная потеря костной массы и уменьшение остеогенеза [12].
Во многих тканях магний участвует в контроле активности некоторых ионных каналов. Он блокирует кальциевый канал в рецепторе NMDA и должен быть вытеснен из клетки для формирования глутаматергического возбуждающего сигнала. Низкие уровни Mg2+ в сыворотке увеличивают активность рецепторов NMDA, что усиливает приток Ca2+ и Na+ и возбудимость нейронов. По этим причинам предполагается наличие дефицита магния при ряде неврологических расстройств, таких как мигрень, хроническая боль, эпилепсия, болезнь Альцгеймера, болезнь Паркинсона, инсульт, а также тревога и депрессия [13]. Уменьшение концентрации Mg2+ в сыворотке крови влечет за собой увеличение высвобождения гормонов стресса, таких как катехоламины, адренокортикотропный гормон и кортизол, и повышает их доступность для головного мозга: тем самым формируется порочный круг снижения устойчивости к стрессу и дальнейшего истощения запасов магния [14].
Магний оказывает существенное влияние на иммунологический ответ как врожденной, так и адаптивной иммунной системы [1, 15]. При хронических заболеваниях он ингибирует образование свободных кислородных радикалов и дегрануляцию тучных клеток, защищает эпителий, нивелирует воспалительное и окислительное повреждение клеток и кровеносных сосудов [16]. Магний способен дозозависимо ингибировать действие многих агонистов агрегации тромбоцитов (например, тромбоксана А2), а также стимулировать синтез простациклина. При гипомагниемии избирательно нарушается высвобождение оксида азота в эндотелии коронарных сосудов, что может способствовать развитию вазоконстрикции и коронарного тромбоза [17].
Существенная роль принадлежит магнию и в формировании соединительной ткани. При его дефиците синтез белков в соединительной ткани замедляется, активность матриксных металлопротеиназ (ММП) возрастает, и внеклеточная матрица прогрессивно деградирует, так как структурная поддержка ткани (в частности, коллагеновые волокна) разрушается быстрее, чем синтезируется [18].
1. Недостаточное потребление и дефицит магния в России являются широко распространенными медицинскими проблемами, при этом на поступление этого макроэлемента в организм и его усвоение влияет значительное количество эндогенных и экзогенных факторов.
Согласно Нормам физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации (2021), у взрослых физиологическая потребность в магнии составляет 420 мг/сут., а у детей – от 55 до 400 мг/сут. У беременных во II–III триместрах и лактирующих женщин потребность в Mg2+ возрастает до 450 мг/сут. [18]. При этом среднее его потребление в настоящее время составляет лишь 175–225 мг/сут. Одна из причин этого – выраженные колебания содержания магния и других макро- и микроэлементов в одних и тех же видах продуктов [19], что может быть обусловлено различными факторами, такими как различия почвы и воды, используемой для ее орошения, удобрения, консервирование, а также методы очистки, обработки и приготовления пищи. Например, семена, бобовые, орехи (миндаль, кешью, бразильские орехи и арахис), цельнозерновой хлеб и крупы (коричневый рис, просо), некоторые фрукты и какао считаются хорошими источниками магния, однако почва, на которой растут эти культуры, может быть обеднена данным макроэлементом. Кроме того, уменьшению уровня магния в продуктах питания способствует применение определенных сельскохозяйственных методов, таких как использование калия и аммония в высоких концентрациях в удобрениях. Некоторые методы обработки пищевых продуктов (варка овощей, рафинирование зерен злаков и т. д.) также вызывают существенное снижение содержания в них магния. Потери магния при переработке пищевых продуктов значительны: так, в случае белой муки эти потери могут достигать 82%, шлифованного риса – 83%, крахмала – 97%, белого сахара – 99%. Нельзя не отметить и то, что к дефициту магния предрасполагает современный «европейский» рацион питания с преобладанием легкой в приготовлении рафинированной и обработанной пищи и фастфуда при почти полном отсутствии бобовых и семян [20].
Основные факторы, влияющие на биодоступность магния, отражены в таблице.
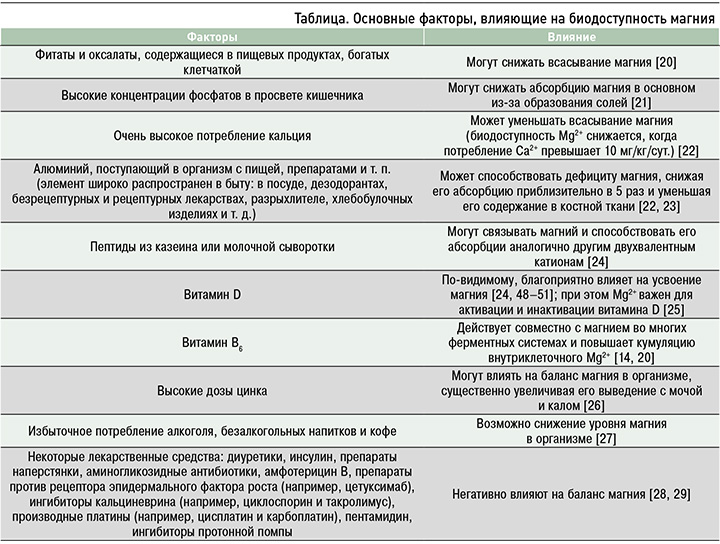
К группам риска дефицита магния относятся [20, 30–32]:
- спортсмены (вследствие больших потерь магния с потом во время интенсивных тренировок);
- пожилые люди (как из-за меньшего потребления пищи, так и вследствие сниженной абсорбции магния в кишечнике и его повышенной почечной экскреции);
- пациенты с заболеваниями желудочно-кишечного тракта и сопутствующей мальабсорбцией, например с болезнью Крона, воспалительными заболеваниями кишечника и целиакией;
- пациенты с СД 2 (хотя до сих пор точно неизвестно, является ли дефицит магния причиной или следствием этого состояния);
- лица, страдающие алкоголизмом;
- пациенты, получающие лечение различными препаратами, влияющими на усвоение магния (см. табл.).
2. Клиническая картина дефицита магния неспецифична, чаще всего связана с нервно-мышечными и нервно-психическими симптомами, при этом длительная недостаточность магния часто сопровождается прогрессированием социально значимых хронических заболеваний, ухудшением репродуктивного здоровья и снижением качества жизни.
Ранние проявления дефицита магния обычно включают нервно-мышечные и нервно-психические изменения. Наиболее частые клинические признаки связаны с повышенной возбудимостью, тремором, головными болями, судорогами, усталостью и астенией [33]. Клиническая картина длительного дефицита магния может варьировать от неспецифических симптомов до возникновения и/или усугубления прогрессирования широкого спектра заболеваний, в том числе сердечно-сосудистой патологии, артериальной гипертензии (АГ), СД 2 и др. [34]. Недостаточность магния ассоциирована с повышением вероятности развития таких состояний, как избыточный вес, нарушение сна, судороги, миопия, ишемический инфаркт мозга, эссенциальная первичная АГ, пролапс митрального клапана, острая реакция на стресс, нестабильная стенокардия, предменструальный синдром, СД 2, пароксизмальная тахикардия и ряд других патологий [35, 36]. Риск анемии обратно пропорционален количеству потребляемого с пищей магния, особенно у женщин и пожилых людей [37]. Низкое потребление Mg2+ связано также со снижением плотности как бедренных костей, так и других костей скелета [38]. При этом увеличение уровня магния в сыворотке крови на каждые 0,1 ммоль/л ассоциировано со снижением заболеваемости АГ на 4–5% [39, 40].
Низкий уровень магния в сыворотке крови сопряжен также с повышенным риском развития фибрилляции предсердий. Смертность при ишемической болезни сердца (ИБС) обратно пропорциональна содержанию магния в питьевой воде [41]. Количество потребляемого с пищей магния обратно пропорционально, а его концентрация в сыворотке крови прямо пропорциональна риску развития сердечно-сосудистых событий, включая инсульт, ИБС и смерть от кардиоваскулярных заболеваний [42].
К наиболее распространенным непосредственным проявлениям дефицита магния при беременности относятся судороги икроножных мышц, повышенный тонус матки, аритмия беременных, АГ. Среди долговременных последствий гипомагниемии можно выделить обменные нарушения: гестационный диабет, избыточную прибавку массы тела, тромбофилию, дисплазию соединительной ткани, остеопению беременных и такие общеизвестные патологии беременности, как гестозы, выкидыши, преждевременные роды и др. [43]. Помимо этого, дефицит магния может приводить к нарушению имплантации эмбриона и тем самым увеличивать риск самопроизвольного аборта [44]. Проявлениями дефицита магния у беременных могут быть кальциноз плаценты, длительная угроза прерывания беременности, преждевременные роды, нарушение родовой деятельности, раскрытия шейки матки в родах, периода изгнания в родах, а также боли в спине, пояснице и тазовом отделе, симфизиопатия и симфизит, преэклампсия и эклампсия [44–46].
Количество потребляемого магния обратно пропорционально уровню индекса массы тела (ИМТ) [47]. Выявлена статистически значимая отрицательная взаимосвязь между количеством потребляемого магния и риском заболеваемости СД 2 [48].
Дефицит магния негативно влияет на психоэмоциональное состояние, тогда как высокое его потребление ассоциировано с более высоким качеством сна [49].
3. Точная лабораторная диагностика дефицита магния затруднена, поскольку его содержание в сыворотке крови не является высокоспецифичным, а референтные данные для такого определения в России отсутствуют. Предпочтительно определение содержания магния в разных субстратах, включая ротовую жидкость.
В связи с тем что гомеостаз магния в организме поддерживается различными механизмами, уровень Mg2+ в крови, соответствующий референтным значениям, может не отражать истощение его запасов в костях и мышцах. Таким образом, диагностика дефицита магния не должна основываться только на определении его уровня в крови; требуется также оценка клинической симптоматики и в некоторых случаях изучение уровня магния в других биологических субстратах (например, в волосах, моче, слюне). При оценке содержания Mg2+ в крови можно определить его концентрацию в цельной крови, плазме и сыворотке крови и отдельно в эритроцитах. Для формирования полного представления о магниевом статусе желательно установить уровни магния во всех указанных биосубстратах крови. На основании данных о концентрации Mg2+ в цельной крови можно судить об уровнях магния во всех форменных элементах крови и в сыворотке. Вычитая из этого показателя уровни магния в эритроцитах и сыворотке крови, можно определить содержание магния в лимфоцитах. Различие между уровнями Mg2+ в плазме и сыворотке указывает на количество магния, связанного с белковой фракцией плазмы крови [50].
Отметим, что при этом на сегодняшний день нет универсальных референтных значений указанных показателей: в России при оценке уровня магния в сыворотке крови используются данные Н.У. Тица (0,66–1,07 ммоль/л), В.В. Меньшикова (0,7–1,2 ммоль/л), И.С. Святова (0,82 ± 0,09 ммоль/л) либо собственные референтные данные лаборатории. В зарубежных публикациях чаще всего используется референтный интервал для сывороточного магния, основанный на данных, полученных в американском исследовании Национальной программы проверки здоровья и питания (National Health and Nutrition Examination Survey, NHANES I), в котором приняли участие около 15 тыс. человек в возрасте от 18 до 74 лет. Соответствующий референтный интервал был определен в диапазоне 0,75–0,955 ммоль/л [33]. Эти данные были получены в 1974 г. при обследовании практически здоровых людей [51]. В настоящее время две независимые исследовательские группы – американская (2016) и немецкая (2021) – нижним пределом референтных значений сывороточного магния предложили считать 0,85 ммоль/л [52, 53]. Согласно резолюции III Международного экспертного совета по проблемам дефицита магния в акушерстве и гинекологии, у беременных за референтные значения нормального содержания магния в сыворотке крови приняты его показатели в диапазоне 0,80–0,85 ммоль/л. В последнее время более распространено исследование уровня магния в плазме крови, при этом следует учитывать, что референтные значения магния в плазме крови должны быть выше, чем в сыворотке крови. Референтные значения для уровней магния в плазме крови в России также четко не установлены [54].
Общее выведение магния из организма можно определить по его содержанию в суточной моче. Однако обычное определение концентрации магния в однократно собранной порции мочи не имеет диагностической ценности, так как его уровень в этом субстрате может сильно различаться в течение суток [54].
4. Пероральный прием препаратов магния может рекомендоваться пациентам с эндокринной патологией, в том числе с повышенным уровнем глюкозы в крови, инсулинорезистентностью, предиабетом, метаболическим синдромом, ожирением, а также женщинам с гестационным СД, беременным женщинам с клиническими проявлениями, указывающими на дефицит магния (гипертонусом матки, судорогами ног, преэклампсией, неврастенией), больным с сердечно-сосудистой патологией, неврологическими и психиатрическими расстройствами, дисплазией соединительной ткани.
Выявлена статистически значимая взаимосвязь между приемом магния оротата и снижением риска повышенного тонуса матки [55]. У пациентов с СД прием магния приводил к статистически значимому снижению уровня глюкозы натощак. Кроме того, у пациентов с риском развития СД на фоне приема магния отмечались улучшение результатов 2-часового перорального глюкозотолерантного теста относительно исходных показателей и снижение уровня липопротеидов низкой плотности по сравнению с приемом плацебо. У пациентов, принимавших магний, наблюдалось статистически значимо более выраженное снижение систолического (САД) и диастолического артериального давления (ДАД) относительно исходных значений, чем у участников, получавших плацебо. Прием магния приводил к среднему снижению САД на 4,18 мм рт. ст. и ДАД на 2,27 мм рт. ст. [56], а также к статистически значимому уменьшению ИМТ преимущественно за счет эффекта у пациентов, исходно имевших дефицит магния, резистентность к инсулину и ожирение [57].
Применение препаратов магния статистически значимо снижает риск развития преэклампсии; этот эффект более выражен у женщин из группы высокого риска развития данной патологии [58]. Установлена статистически значимая взаимосвязь между приемом магния оротата и уменьшением вероятности гипомагниемии, синдрома сосудистой дистонии, утренней головной боли, головной боли напряжения, головокружения, пролапса митрального клапана I степени, регургитации I степени, наджелудочковых и желудочковых экстрасистол, пароксизмальной наджелудочковой тахикардии и АГ [59]. На фоне применения магния регистрировались статистически значимое увеличение времени и эффективности сна, концентрации сывороточного ренина и мелатонина, а также снижение значений индекса выраженности бессонницы, латентного времени засыпания и концентрации сывороточного кортизола [60]. Пероральный профилактический прием препаратов магния значительно снижал частоту и интенсивность приступов мигрени [61]. Клинически значимая эффективность применения магния оротата была зафиксирована у 67,7% пациентов с дисплазией соединительной ткани [62].
5. Рекомендуемые дозы элементного магния и длительность терапии зависят от целей лечения, имеющейся патологии и исходного магниевого статуса и должны рассчитываться с учетом массы тела. В клинической практике следует отдавать предпочтение органическим солям магния ввиду их большей биодоступности, как правило, применяя их в виде лекарственных препаратов в терапевтических целях и биологически активных добавок к пище (БАД) в профилактических целях.
Доза магния должна рассчитываться с учетом массы тела (в среднем 4–6 мг/кг/сут.). У больных с неконтролируемой АГ, получающих антигипертензивные препараты, прием препаратов магния (≥240 мг/сут.) приводил к снижению АД, в то время как у пациентов, не получающих антигипертензивные препараты, для снижения АД требовалось как минимум 600 мг/сут. магния [63]. Прием пероральных препаратов магния сопровождался статистически значимым снижением САД в среднем на 3–4 мм рт. ст. и ДАД – на 2–3 мм рт. ст., причем эффект отмечался при потреблении более 370 мг/сут. элементного магния [64]. В клинической практике используют органические (аспарагинат, ацетат, цитрат, глюконат, лактат, пидолат, оротат) и неорганические (карбонат, сульфат, оксид, хлорид) соли магния. При этом органические соли обладают большей биодоступностью и меньшим количеством нежелательных реакций. Биодоступность хлорида, лактата и аспарагината магния в 2–2,5 раза выше, чем у оксида магния (менее 5%). Среди органических солей наибольшими преимуществами обладает пидолат магния благодаря высокой биодоступности и хорошей пенетрации во внутриклеточное пространство.
Для лекарств существует большое число регуляторных ограничений, не относящихся к БАД. Так, для регистрации лекарственных средств обязательны доклинические и клинические исследования, в то время как для биодобавок – только токсикологические и гигиенические; продажа лекарственных препаратов разрешена только в аптеках, тогда как БАД могут реализовываться как в аптеках, так и в любом розничном предприятии, имеющем лицензию на торговлю пищевыми продуктами.
6. Учитывая, что витамин В6 является фармакокинетическим и фармакодинамическим синергистом магния, эффективно использование препаратов, содержащих их комбинацию.
Применение цитрата, лактата или пидолата магния в комбинации с пиридоксином у беременных ассоциировано с более низким риском невынашивания, плацентарной недостаточности, угрозы прерывания беременности, преэклампсии, преждевременных родов, родоразрешения путем кесарева сечения, госпитализации матери, задержки развития плода [65]. Среди пациентов с тяжелым или очень тяжелым стрессом на фоне приема комбинации магния и витамина B6 снижение стресса было более выраженным (на 24%), чем при лечении только магнием [14]. У лиц с пограничными психическими расстройствами при назначении дополнительно к основному лечению цитрата магния (400 мг/сут. в пересчете на элементарный магний) в сочетании с пиридоксином (40 мг/сут.) на 30-й день терапии наблюдалось уменьшение выраженности симптомов пограничных психических расстройств (нарушений сна, памяти и внимания, тревоги, депрессии) по сравнению с исходными показателями. Прием поддерживающей дозы комбинированного препарата, содержащего цитрат магния и пиридоксин (200 мг/сут. элементного магния), позволяет снизить дозу антидепрессантов на 30% [66].
ЗАКЛЮЧЕНИЕ
Учитывая, что магний является элементом, необходимым для нормальной жизнедеятельности организма, а его дефицит широко распространен и может быть фактором риска развития некоторых заболеваний, а также следствием различных патологических состояний, коррекция такого дефицита будет способствовать улучшению исходов многих заболеваний, качества жизни, самочувствия и общего состояния здоровья пациентов. Принимая во внимание доступность неинвазивных и малоинвазивных методов диагностики данного состояния, а также наличие доступных эффективных пероральных препаратов магния, следует разработать и внедрить в медицинскую практику алгоритм оценки этого состояния врачами различных специальностей у пациентов из групп риска, своевременной его коррекции и адекватной профилактики. Участники заседания Совета экспертов выразили консолидированное мнение о необходимости разработки клинических рекомендаций по диагностике, лечению и профилактике дефицита магния (код заболевания Е61.3 в соответствии с МКБ-10).



