Артериальная гипертония (АГ) — ведущий модифицируемый фактор риска развития сердечно-сосудистых осложнений и смерти во всем мире. Распространенность АГ на территории Российской Федерации составляет 40% [1]. В настоящее время приоритетной задачей является поиск индивидуализированной фармакологической терапии, направленной на разные патофизиологические звенья АГ.
В последние годы вновь возник интерес к определению активности ренина плазмы (АРП) — ключевого регулятора работы ренин-ангиотензин-альдостероновой системы (РААС) — с целью выявления механизма, ответственного за развитие и поддержание АГ, и для выбора тактики антигипертензивной терапии (АГТ) [2—9]. На основании классификации на ренин-ангиотензин- и натрий-объемзависимую формы АГ, предложенной J.Н. Laragh в 1973 г., разработаны алгоритмы назначения АГТ с учетом уровня АРП [2, 4, 5].
Фундаментальным подтверждением двойного механизма долгосрочной регуляции АД является то, что все антигипертензивные препараты снижают артериальное давление (АД) посредством уменьшения концентрации натрия в организме (анти-«объем»-препараты) или через блокирование сосудосуживающего действия РААС (анти-«ренин»-препараты) [4, 5]. Основными представителями анти-«объем»-препаратов являются диуретики, антагонисты кальция (АК), блокаторы альдостероновых рецепторов [10, 11], а представителями анти-«ренин»-препаратов — ингибиторы ангиотензинпревращающего фермента (АПФ) и блокаторы рецепторов ангиотензина II. Такая классификация антигипертензивных препаратов позволяет упростить выбор средства для лечения больных АГ. Однако клинические исследования по оценке значения определения АРП при АГ с участием российской популяции немногочисленны.
Целью настоящего исследования стало изучение антигипертензивного ответа в зависимости от АРП у больных АГ российской популяции, нуждающихся в коррекции недостаточно эффективной комбинированной АГТ.
Материал и методы
В исследование были включены 72 пациента (средний возраст 62,0±8,3 года, 28 мужчин) с АГ, не контролируемой приемом ингибиторами АПФ+АК (клиническое АД≥140/90, дневное АД по СМАД >135/85 мм рт.ст.) на фоне 4-недельной начальной комбинированной терапии ингибитором АПФ квадроприлом в дозе 6 мг/сут и АК фелодипином в дозе 5 мг/сут. Всем пациентам был добавлен индапамид ретард (арифон ретард, «Сервье») в дозе 1,5 мг/сут на 6 мес. В исследование не включали больных с анамнезом ассоциированных клинических состояний, гипокалиемией (К<3,5 ммоль/л), тяжелой гипонатриемией (Na<130 ммоль/л) и со скоростью клубочковой фильтрации <30 мл/мин/1,73 м2. Уровень клинического АД составил 152,2±15,2/81,7±10,8 мм рт.ст. (табл. 1). У всех пациентов был исключен симптоматический характер АГ. Не включали пациентов с нарушениями ритма и тяжелой сопутствующей патологией.
Исследование АРП выполняли в лаборатории «Научно-методический центр клинической лабораторной диагностики Ситилаб» (Москва) радиоиммунным методом с использованием наборов фирмы «Immunotech» (Франция—Чехия). Образцы крови брали натощак в горизонтальном положении пациента после 30-минутного отдыха. АРП определяли как количество ангиотензина I (АТI), образованного путем захвата высокоаффинными антителами в 1 мл образца в течение 1 ч. Выделяли следующие варианты АГ: объемзависимая — АРП <0,65 нг/мл/ч; ренинзависимая — АРП 0,65—6,5 нг/мл/ч.
Клиническое измерение АД осуществляли после 10-минутного отдыха с использованием валидированного осциллометрического прибора (UA 787, AND, Япония). Выполнялось 3 последовательных измерения АД с интервалом 1 мин в положении пациента сидя. Среднее значение 3 измерений принимали за АД на визите.

Суточное мониторирование артериального давления (СМАД) проводили с использованием портативной системы BP Lab Vasotens (ООО «Петр Телегин», Нижний Новгород, Россия) в группе больных АГ, не контролируемой приемом ингибитора АПФ+АК. Интервал между измерениями составил 15 мин днем и 30 мин ночью. Анализ результатов производили в случае не менее 85% успешных измерений, подтвержденных анализом осциллометрического колокола АД. В дни выполнения СМАД пациенты вели дневник, в котором отмечали часы бодрствования, период и качество сна, время принятия лекарственных средств, самочувствие и физическую активность.
Статистическую обработку данных проводили с использованием программы Statistica (версия 7.0). Непрерывные переменные представлены в виде M±SD (среднее ± стандартное отклонение среднего). При непараметрическом распределении данных рассчитывали коэффициент ранговой корреляции Спирмена (r). Для выявления многомерных зависимостей между различными признаками использовали многофакторный пошаговый регрессионный анализ. Различия считали достоверными при двустороннем p<0,05.
Результаты
Оценка эффективности антигипертензивного ответа на добавление диуретика (индапамид ретард) в зависимости от АРП у больных с АГ, не контролируемой приемом ингибитора АПФ и АК. Средний уровень АРП составил 0,87±1,75 нг/мл/ч (минимум 0,1; максимум 6,3). Частота выявления объемзависимой АГ (АРП<0,65 нг/мл/ч) составила 58%, ренинзависимой АГ (АРП≥0,65 нг/мл/ч) — 42%.
При оценке клинико-демографических характеристик в зависимости от АРП установлено, что больные объемзависимой АГ достоверно старше (р<0,01), более длительно болеют АГ (р<0,05), имеют более высокие значения клинического и суточного АД (р<0,01). Больные ренинзависимой АГ характеризуются более высоким индексом массы тела (р<0,05), более выраженными метаболическими нарушениями по показателям липидного (более частым выявлением дислипидемии (р<0,05), достоверно высокими показателями уровнями общего холестерина — ХС, ХС липопротеидов низкой плотности — ЛНП (р<0,05)), углеводного обмена (более высоким уровнем глюкозы в крови натощак) (р<0,05) и мочевой кислоты в сыворотке крови (р<0,01).
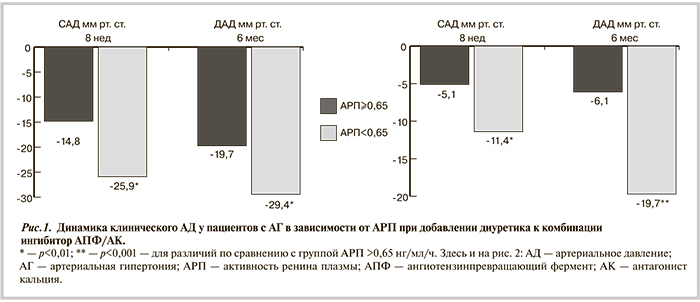
При изучении динамики АД на фоне 6-месячного добавления индапамида ретарда 1,5 мг/сут у больных АГ, не контролируемой приемом ингибитором АПФ +АК, установлено, что наиболее выраженный антигипертензивный ответ наблюдался в группе объемзависимой АГ (рис. 1).
Исходный уровень АД у больных с объемзависимой АГ составил 156,6±14,1/86,7±11,5 8 мм рт.ст. против 151,9±17,1/78,0±7,8 мм рт.ст. у бльных с ренинзависимой АГ. На фоне лечения уровень клинического АД составил соответственно 126,2±10,6/72,5±11,6 и 132,2±9,1/71,9±7,2 мм рт.ст. (р<0,05), целевого клинического АД достигли 95% против 80% пациентов (χ2=10,3; р<0,05). Отмечалось нарастание антигипертензивного эффекта, а достоверность различий выраженности антигипертензивного ответа сохранялась на всем протяжении исследования.
Проведен детальный анализ группы больных с неконтролируемой АГ на фоне терапии индапамидом ретардом в зависимости от АРП по терцилям. По данным этого анализа подтверждена ассоциация низкой АРП с развитием объемзависимой АГ и высокой эффективностью терапии диуретиком. Установлено, что группа с более низкой АРП характеризуется лучшим антигипертензивным ответом, уровень клинического АД составляет 123,4±11,2/67,6±10,3 мм рт.ст., целевого клинического АД достигли 87% пациентов, процент снижения систолического АД (САД) от исходного составил 21,8.
Напротив, группа пациентов с наиболее высокой АРП характеризуется менее выраженным антигипертензивным ответом, уровень клинического АД на фоне терапии составляет 132,4±11,9/73,6±5,1 мм рт.ст., целевого клинического АД достигли 70% пациентов, процент снижения САД от исходного составил 10,1 (табл. 2).
При проведении однофакторного корреляционного анализа по Спирмену установлена достоверная отрицательная взаимосвязь величины снижения САД через 6 мес с АРП (r=–0,48; p<0,01), положительная взаимосвязь с САД клиническим (r=0,66; p<0,000), диастолическим АД (ДАД) клиническим (r=0,56; p<0,000). Установлены ассоциации параметров РААС и развития антигипертензивного эффекта. АРП обратно коррелировала с величиной снижения САД через 8 нед (r= –0,4; p<0,001), величиной снижения САД через 6 мес (r=–0,3; p<0,05).
При многофакторном регрессионном анализе установлена обратная взаимосвязь между величиной снижения через 6 мес для клинического САД и исходной АРП (β=–0,44; p<0,001), клинического ДАД и АРП (β=–0,45; p<0,001), дневного САД и АРП (β=–0,42; p<0,01), дневного ДАД и АРП (β=–0,38; p<0,01).
Результаты СМАД подтвердили различия динамики клинического АД в группах с объемзависимой по сравнению с ренинзависимой АГ после добавления диуретиков (рис. 2). Исходный уровень дневного АД у больных объемзависимой АГ составил 149,4±11,7/88,7±10,9 мм рт.ст., у больных ренинзависимой АГ — 145,5±12,5/82,5±9,0 мм рт.ст, ночного АД — соответственно 144,3±14,2/81,6±12,3 и 145,9±17,6/80,5±11,3 мм рт.ст. (различия недостоверны). На фоне лечения в группе с объемзависимой АГ был достигнут более низкий уровень дневного АД (130,0±11,0/74,1±9,9 мм рт.ст. против 136,5±7,3/78,8±8,2 мм рт.ст.; р<0,05) и ночного АД (127,9±15,8/71±13,5 против 132,6±13,0/74,5±10,2 мм рт.ст.; р<0,05). Кроме того, в группе с объемзависимой АГ отмечено более выраженное увеличение суточного индекса (СИ) САД с 3,9±5,7 до 12,3±6,8% (р<0,05 по сравнению с исходным) против с 3,6±10,3 до 7,8±6,7% (р<0,05 для достигнутых значений), СИ ДАД с 5,0±6,5 до 10,8±10,2% (р<0,05 по сравнению с исходным) против 4,3±10,0 до 6,2±9,3% (р<0,05 для достигнутых значений). Лечение привело к значительному уменьшению вариабельности САД с 15,1±3,3 до 12,2±5,1 мм рт.ст. и ДАД с 12,1±4,5 до 10,5±2,6 мм рт.ст. в дневные часы в группе объемзависимой АГ. Вариабельность САД и ДАД в ночные часы значимо не изменилась в двух группах.
При проведении однофакторного корреляционного анализа между АРП и параметрами СМАД выявлены достоверные взаимосвязи. Обнаружены ассоциации АРП с величиной снижения среднесуточного САД (r=–0,4), среднесуточного ДАД (r=–0,4), дневного САД (r=–0,3), дневного ДАД (r=–0,4), ночного САД (r=–0,3), ночного ДАД (r=–0,3) и с величиной снижения СИ САД (r=–0,4), СИ ДАД (r=–0,3).
Обсуждение
Подход к назначению АГТ, основанный на определении АРП, еще не получил широкого распространения в нашей стране. К примеру, на территории США клинический тест по определению АРП коммерчески доступен и его стоимость возмещается в рамках программы Medicare и большинством страховых компаний. В нашей стране при выборе тактики лечения больного врач чаще руководствуется национальными рекомендациями по диагностике и лечению АГ. Однако показатели контролируемой АГ в России остаются низкими и составляют 27,3% [1], что делает необходимым выделение ведущего патофизиологического звена АГ для целенаправленного выбора оптимального класса препаратов.
Данные о недостижении целевого уровня АД у 15—20% пациентов на фоне двухкомпонентной терапии и включении в терапевтический режим в этом случае тиазидного диуретика, а также ассоциации объемзависимой АГ и высокой эффективности терапии диуретиками делают актуальным изучение назначения диуретика у больных с АГ, особенно у больных неконтролируемой АГ. Одним из наиболее эффективных и часто назначаемых тиазидных диуретиков в России с большой доказательной базой является индапамид ретард.
В нашем исследовании была предпринята попытка изучения антигипертензивного ответа в зависимости от АРП у больных АГ российской популяции, нуждающихся в коррекции недостаточно эффективной комбинированной АГТ.
Необходимо отметить важные характеристики группы наблюдения. Для анализа были выбраны комбинации ингибиторов АПФ и АК, больные с уровнем клинического АД>140/90 мм рт.ст., которые имели узкий возрастной диапазон от 50 до 70 лет. На этапе отбора были исключены ассоциированные клинические состояния, вторичный и злокачественный характер АГ, больные характеризовались сохранной функцией почек.
Результаты, полученные в настоящем исследовании, подтвердили значение определения АРП для прогнозирования антигипертензивного ответа при добавлении диуретика (индапамид ретард). На фоне 6-месячной терапии диуретиком больные с АРП <0,65 нг/мл/ч по сравнению с больными с АРП≥0,65 нг/мл/ч характеризовались лучшим антигипертензивным ответом. Отмечалось нарастание антигипертензивного эффекта, а достоверность различий выраженности антигипертензивного ответа сохранялась на всем протяжении исследования. Кроме того, применение диуретика сопровождалось клинически желательным достоверным увеличением степени ночного снижения АД у больных объемзависимой АГ, чего не наблюдалось у больных ренинзависимой АГ. Это подтверждает гипотезу о назначении анти-«объем»-препаратов пациентам с низкой АРП. Результаты многофакторного регрессионного анализа подтвердили независимую ассоциацию степени снижения АД и АРП. Подтверждение нашим данным получено в нескольких последовательно опубликованных клинических исследованиях [12—14].

В одном из таких исследований была оценена АРП как предиктор антигипертензивного ответа у пациентов при назначении β-адреноблокатора (атенолол) и тиазидного диуретика (гидрохлоротиазид) при монотерапии и добавлении к получаемой терапии [13]. Было установлено, что АРП позволяет прогнозировать антигипертензивный ответ в отношении как САД, так и ДАД. Пациенты с высокой АРП характеризовались большим снижением АД при назначении атенолола, чем гидрохлоротиазида, в то время как пациенты с низкой АРП лучше отвечали на терапию гидрохлоротиазидом.
В одновременно опубликованном исследовании предложен выбор препарата в соответствии с патофизиологическим типом АГ, оцененным с помощью измерения АРП [12]. В исследовании описывается вероятность повышения АД (>10 мм рт. ст.) на фоне терапии атенололом или гидрохлоротиазидом. В ходе исследования было установлено, что 7,7% пациентов были подвержены повышению уровня АД на фоне лечения, причем анти-«ренин»-препараты в 2 раза чаще вызывали повышение АД, чем анти-«объем»-препараты (на 11 и 5,2% соответственно). АРП была разделена с применением терцилей на низкорениновую (<0,74 нг/мл/ч), среднерениновую (0,74—2,0 нг/мл/ч) и высокорениновую (>2,0 нг/мл/ч). Наиболее часто повышение АД происходило при назначении анти-«ренин»-препаратов пациентам с низкой АРП. Более того, отмена анти-«ренин»-препаратов у пациентов с низкой АРП и применение их у пациентов с высокой АРП, а также отмена анти-«объем»-препаратов у пациентов с высокой АРП и применение их у пациентов с низкой АРП могут существенно увеличить вероятность достижения целевого АД при использовании монотерапии, уменьшить вероятность прессорного ответа и побочных эффектов.
В открытом рандомизированном исследовании ASPIRANT оценивалась эффективность добавления спиронолактона у пациентов с резистентной АГ с определением АРП [14]. Была выявлена значительная взаимосвязь между параметрами АРП и антигипертензивным ответом. Пациенты с АРП <1,34 нг/мл/ч характеризовались лучшим антигипертензивным ответом при применении спиронолактона (анти-«объем»-препарат), чем пациенты с более высокими значениями АРП. Изменения в САД (отношение шансов при 95% доверительном интервале), измеренном при 24-часовом амбулаторном мониторировании, составили –19,0 (от –31,0 до 2,1), –12,0 (от –29,0 до 13,0) и –4,0 (от –36,0 до 13,0) мм рт.ст. для низкоренинового (<0,12 нг/мл/ч), среднеренинового (0,13—1,34 нг/мл/ч) и высокоренинового (>1,34 нг/мл/ч) терциля соответственно. Полученные результаты подтверждают важность оценки АРП при объемзависимой АГ и являются отражением исследования с пропранололом у пациентов с ренинзависимой АГ [15].
Клиническая ценность определения АРП не вызывает сомнения. Так, в открытом рандомизированном исследовании сравнивались эффективность алгоритма назначения АГТ на основании определения АРП и обычный подход [7]. В исследование были включены 77 пациентов с неконтролируемой АГ. В группе пациентов, у которых определялась АРП, оценивался вариант АГ (объемзависимая или ренинзависимая) и впоследствии назначалась или отменялась терапия анти-«объем»- и анти-«ренин»-препаратами. Критериями оценки эффективности была динамика АД к концу исследования. Результаты продемонстрировали значительное снижение САД и ДАД в обеих группах. Однако снижение САД было более выраженным в группе пациентов, получавших АГТ на основании АРП, по сравнению с обычным режимом назначения АГТ (–29,1±3,2 против –19,2±3,2 мм рт.ст.; р=0,03). При этом количество антигипертензивных препаратов не изменилось в ходе лечения в двух группах, несмотря на более выраженное снижение САД в группе пациентов, получавших АГТ на основании АРП. Более того, прием 60 и 11% анти-«ренин»-препаратов был прекращен у пациентов с объемзависимой АГ в группе АРП-контроля и стандартной терапии соответственно. Количество антигипертензивных препаратов было снижено в группе АРП-контроля (–0,5±0,3 против 0,7±0,3 препарата; р=0,01). Целевой уровень АД был достигнут в 59% случаев при стандартном подходе к терапии и в 74% — при использовании АРП.
Таким образом, добавление диуретика с учетом уровня АРП может не только повысить эффективность проводимой терапии, уменьшить риск развития сердечно-сосудистых заболеваний, но и уменьшить количество применяемых препаратов, увеличив приверженность пациентов к лечению.



