В настоящее время основным методом оценки насосной функции левого желудочка (ЛЖ) сердца является эхокардиография (ЭхоКГ). Однако фракция выброса (ФВ) ЛЖ как основной показатель насосной функции не позволяет выявлять ранние нарушения систолической функции ЛЖ. В связи с этим в практику внедряются новые методы, позволяющие выявлять систолическую дисфункцию миокарда на самых ранних доклинических стадиях. К ним относят тканевой допплер (ТД) движения фиброзного кольца митрального клапана (МК) и оценку деформации миокарда (так называемого стрейна).
Сравнительные исследования этих двух методов показали, что метод стрейна ЛЖ отличается лучшей воспроизводимостью [1] и более высокой чувствительностью [2] в отношении оценки ранней систолической дисфункции миокарда ЛЖ.
Расчет стрейна ЛЖ можно осуществить двумя способами: на основе допплеровской визуализации тканей и на основе отслеживания пятен серой шкалы ультразвукового изображения миокарда. Последний имеет ряд преимуществ, основной из которых — значимо меньшая вариабельность получаемых показателей [3]. Именно поэтому в последние годы технологии двухмерного отслеживания пятен отдается предпочтение.
Систолическая деформация миокарда ЛЖ происходит в 3 направлениях: продольном, радиальном и циркулярном. Как показали предшествующие работы, первым у больных с аортальным стенозом (АС) снижается продольное сокращение ЛЖ от верхушки к основанию сердца [4—6], что, вероятно, обусловлено субэндокардиальным расположением продольных волокон в ЛЖ и быстро развивающимся интерстициальным фиброзом при постоянной повышенной посленагрузке [7, 8]. Следует также отметить относительно бóльшую простоту и воспроизводимость определения продольного стрейна ЛЖ по сравнению с радиальным, так как расчет последнего сильно зависит от места «ультразвукового среза» верхушки ЛЖ, что может резко варьировать даже у одного исследователя.
Предшествующие работы по изучению продольного стрейна ЛЖ у больных с АС немногочисленны, однако практически все указывают на сниженные показатели стрейна ЛЖ при любой степени стеноза, в том числе у бессимптомных больных [6, 9]. Это подтверждает наличие систолической дисфункции ЛЖ у больных с АС еще до появления признаков сердечной недостаточности (СН).
Следующим шагом в установлении целесообразности включения расчета стрейна ЛЖ в алгоритм ведения больных с АС является накопление данных о прогностической значимости этого показателя. Таких работ проведено пока очень немного, и они касались преимущественно больных с тяжелой степенью порока [4, 8, 10, 11]. Актуальность поиска новых объективных параметров стратификации риска у больных как с бессимптомным тяжелым АС, так и с клинически проявляющимся АС легкой и средней тяжести обусловлена тем, что проведение рекомендованной для этой цели нагрузочной пробы нередко не представляется возможным в этой возрастной группе, а симптомы часто могут быть обусловлены другой сопутствующей патологией, в основном ишемической болезнью сердца (ИБС).

Целью исследования явились изучение взаимосвязи показателей глобального продольного стрейна ЛЖ с клиническими, эхо- и электрокардиографическими параметрами у больных с неоперированным дегенеративным АС всех степеней тяжести, а также оценка прогностической значимости стрейна у больных с АС в течение 1 года наблюдения.
Материал и методы
Обследованы 80 больных с дегенеративным АС различных степеней тяжести, 49 больных без порока, сопоставимых по возрасту, полу и основным сердечно-сосудистым заболеваниям (ССЗ), и 24 здоровых добровольца. Последние обследовались с целью получения референсных значений нормы для использованной нами компьютерной программы оценки стрейна миокарда.
Больные АС находились на стационарном лечении в кардиологическом отделении ГБУЗ «Городская больница №17» ДЗ Москвы с различной патологией. Порок сердца подтверждался или вновь диагностировался при ЭхоКГ.
Критериями включения в основную группу были согласие больного на использование данных обследования в научных целях, площадь аортального клапана (АК) менее 2 см2 и отсутствие сопутствующей тяжелой патологии с предполагаемой продолжительностью жизни менее 6 мес. В исследование не включали больных с другой значимой клапанной патологией, двустворчатым АК, подозрением на ревматический порок, нарушением локальной и/или глобальной сократимости ЛЖ или ФВ ЛЖ<50%.
В группу контроля подбирали больных, сопоставимых по полу, возрасту, набору основных ССЗ, таких как артериальная гипертензия (АГ), ИБС, сахарный диабет, мерцательная аритмия, перенесенный инсульт. Основным отличием больных в контрольной группе было отсутствие клапанных пороков сердца при ЭхоКГ.
Исходно в исследование были включены 104 больных с АС и 88 контрольной группы, однако оценка деформации миокарда ЛЖ оказалась возможной только у 80 больных из группы АС и у 49 из группы контроля.
Группу здоровых добровольцев составили молодые люди, с нормальными показателями при ЭхоКГ.

Обследование включало сбор анамнестических и клинических данных, лабораторные (холестерин и креатинин сыворотки крови) и инструментальные (12-канальная электрокардиография, трансторакальная ЭхоКГ) исследования. Последующее наблюдение включало фиксирование следующих неблагоприятных исходов: смерть от любой причины, развитие нефатального инфаркта миокарда (ИМ), нефатального инсульта, госпитализация по поводу нестабильной стенокардии или прогрессирования СН. Отдельно анализировали риск декомпенсации СН, включавший случаи госпитализации по поводу СН и смерть от СН. Неблагоприятный исход констатировали на основании результатов телефонного контакта или амбулаторного приема.
Трансторакальную ЭхоКГ проводили на ультразвуковом сканере Vivid i с мультичастотным фазированным датчиком 3S-RS (1,7—4,0 МГц) с параллельной записью электрокардиограммы (ЭКГ). Основные позиции двухмерного изображения записывали из парастернального доступа по длинной и короткой оси и верхушечного доступа на 2 (А2С), 4 (А4С) камеры и по длинной оси (LAX). В дальнейшем применяли стандартный протокол исследования, рекомендованный Американской ассоциацией ЭхоКГ [12]. Определение конечного систолического объема (КСО) и конечного диастолического объема (КДО) левых камер сердца проводили методом дисков, расчет ФВ ЛЖ осуществляли по формуле: ФВ ЛЖ=(КДО–КСО)/КДО х 100%.
 Массу миокарда ЛЖ рассчитывали по формуле Devereux: 0,8 х [1,04 (ТМЖП+КДР+ТЗСЛЖ)3 – КДР3]+0,6, где КДР — конечный диастолический размер ЛЖ, ТМЖП — толщина межжелудочковой перегородки в диастолу, ТЗСЛЖ — толщина задней стенки ЛЖ в диастолу.
Массу миокарда ЛЖ рассчитывали по формуле Devereux: 0,8 х [1,04 (ТМЖП+КДР+ТЗСЛЖ)3 – КДР3]+0,6, где КДР — конечный диастолический размер ЛЖ, ТМЖП — толщина межжелудочковой перегородки в диастолу, ТЗСЛЖ — толщина задней стенки ЛЖ в диастолу.
Индексы площади АК, объемов и массы миокарда ЛЖ рассчитывали путем деления на площадь поверхности тела. ТД движения фиброзного кольца МК в латеральной позиции использовали для оценки систолической и диастолической функции ЛЖ. Площадь АК высчитывали с использованием уравнения непрерывности потока согласно объединенным европейским и американским рекомендациям 2009 г. [13].
Оценку глобального продольного стрейна (GLPS) ЛЖ на основе отслеживания пятен серой шкалы проводили с использованием программного обеспечения рабочей станции General Electric. Сегментарную оценку стрейна ЛЖ проводили по видеоизображениям А2С, А4С и LAX, записанным из верхушечного доступа. Частота кадров поддерживалась в интервале 40—80 в секунду. Трассировку полости ЛЖ по границе эндокарда проводили вручную в конце систолы, после чего миокард ЛЖ автоматически разбивался на 6 сегментов в каждой позиции. Затем вновь вручную выполняли корректировку ширины и формы зоны интереса, после чего программа автоматически рассчитывала значения стрейна для каждого сегмента ЛЖ. Сегменты с неоптимальной визуализацией исключались из расчетов программой или исследователем. В результате усреднения всех значений получали показатели глобального продольного стрейна для каждой из трех позиций (GLPS_A2C, GLPS_A4C и GLPS_LAX), а также глобальный продольный стрейн для всего ЛЖ (GLPS_Avg) в виде «бычьего глаза» (рис. 1, см. цветную вклейку).
Запись ЭКГ проводили в 12 отведениях, рассчитывали длительность интервалов QRS и QT от начала зубца Q до окончания зубца S или T соответственно. Вольтажные индексы гипертрофии ЛЖ — ГЛЖ (Соколова, Корнельский и Губнера) рассчитывали как RV5(V6)+SV1(V2), RaVL+SV3 и RI+SIII соответственно.
Статистическую обработку полученных данных проводили с использованием пакета программы SPSS 17.0. Количественные данные представляли в виде средних значений ± стандартное отклонение (M±SD). Средние величины сравнивали с использованием критерия Манна—Уитни, дискретные величины — по критерию χ2 Пирсона. Корреляционный анализ проводили с использованием коэффициента Спирмена. Оценку связи показателей с неблагоприятным прогнозом выполняли с использованием однофакторного регрессионного анализа Кокса. Анализ выживаемости проводили с помощью метода Каплана—Мейера. Для всех видов анализа статистически значимыми считали различия при р<0,05.
Результаты
Группы больных с АС и контроля не различались по возрасту (77,4±8,59 и 75,8±8,08 года соответственно) и полу (75 и 73,5% женщин соответственно). По другим важным клиническим параметрам группы также достоверно не различались (табл. 1), за исключением одышки, на которую жаловались 75% больных с АС и только 36,7% больных из группы контроля (р<0,0001). У большинства имелась АГ, около 20% ранее перенесли инсульт. Функция почек была значительно снижена (скорость клубочковой фильтрации <60 мл/мин) в обеих группах.
Средняя площадь АК в группе больных с АС составила 1,1±0,30 см2, индекс площади АК — 0,6±0,22 см2/м2.
Максимальная площадь АК была 1,9 см2, минимальная — 0,2 см2. Распределение больных по степеням тяжести порока было следующим: I степень (1,5—2,0 см2) — 11 (13,8%), II степень (1,0—1,5 см2) — 36 (45%) и III степень (<1,0 см2) — 33 (41,2%). Сравнение результатов ЭхоКГ у больных с пороком и без него представлено в табл. 2. У больных с АС отмечены достоверно бóльшие объем левого предсердия (p<0,0001), масса миокарда ЛЖ (р=0,003), ТМЖП (р<0,0001) и ТЗСЛЖ (р=0,038). Показатели ТД движения фиброзного кольца МК пики S′ и E′, отражающие систолическую и диастолическую функцию ЛЖ, были значимо ниже у больных с АС (р<0,0001 и р=0,004 соответственно).
Анализ ЭКГ больных в 2 группах выявил ряд достоверных различий. Так, у больных с АС значимо большими оказались интервалы QRS и QT (р=0,010 и р=0,046 соответственно), отражающие процессы де- и реполяризации миокарда, а также вольтажные параметры гипертрофии (см. табл. 2).
Необходимость применения программы расчета стрейна ЛЖ «отсеяла» достаточно большое количество записей больных. В результате из исходно включенных в исследование анализ стрейна миокарда возможно было провести у 76,9% больных с АС и только 55,7% больных из группы контроля. Помимо неудовлетворительной визуализации причинами такой значительной непригодности стали либо высокая частота сердечных сокращений (ЧСС), либо большой разброс ЧСС в ходе исследования. Эти показатели ЧСС у отдельных больных были приемлемы для обычной ЭхоКГ, но стали ограничением для анализа стрейна ЛЖ.
 В ходе последующего анализа деформации миокарда ЛЖ с использованием специального программного обеспечения, всего было проанализировано 1360 сегментов ЛЖ у больных с АС и 833 сегмента ЛЖ у больных из группы контроля. Сегментов, исключенных из анализа ввиду неудовлетворительной визуализации, было 82 в группе АС и 87 в группе контроля, что составило 6 и 10% соответственно.
В ходе последующего анализа деформации миокарда ЛЖ с использованием специального программного обеспечения, всего было проанализировано 1360 сегментов ЛЖ у больных с АС и 833 сегмента ЛЖ у больных из группы контроля. Сегментов, исключенных из анализа ввиду неудовлетворительной визуализации, было 82 в группе АС и 87 в группе контроля, что составило 6 и 10% соответственно.
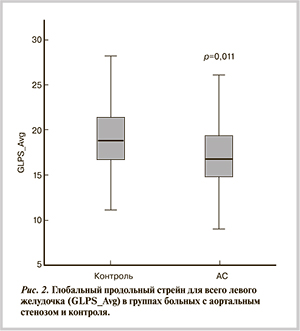
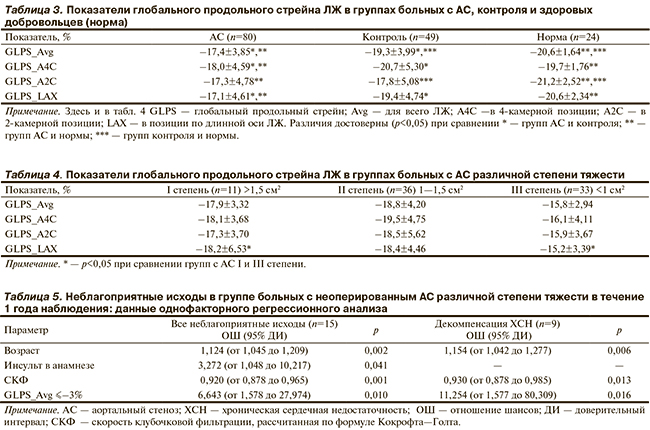
Средние показатели GLPS оказались достоверно более низкими у больных с АС по сравнению с группами контроля и здоровых молодых добровольцев. В свою очередь больные из группы контроля имели более низкие показатели стрейна ЛЖ по сравнению со здоровыми добровольцами (табл. 3; рис. 2).
Анализ значений GLPS в группах больных с АС, разделенных по степеням тяжести, выявил достоверные различия только между группами с I и III степенями и только для позиции по длинной оси ЛЖ. Тем не менее у больных с площадью аортального отверстия менее 1 см2 значения GLPS во всех позициях были ниже (табл. 4). Вероятно, достоверность при сравнении результатов не была получена из-за относительно небольшого количества больных в каждой подгруппе.
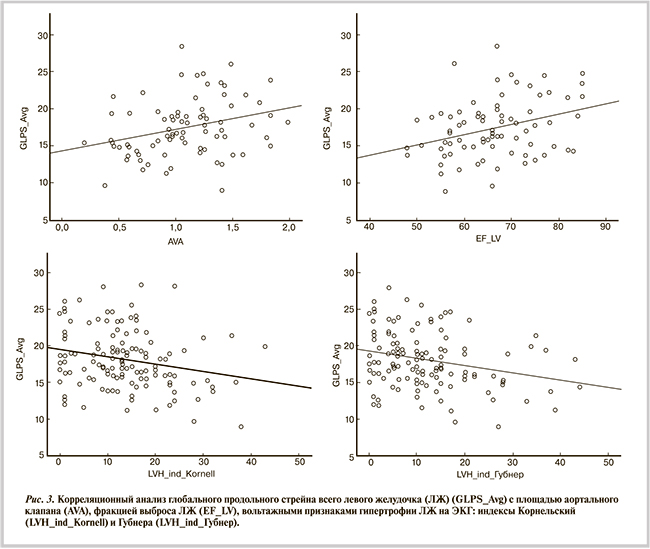
Корреляционный анализ GLPX_Avg с клиническими параметрами, данными ЭхоКГ и ЭКГ в группе больных с АС выявил прямую связь с площадью аортального клапана (r=0,318; р=0,004) и ФВ ЛЖ (r=0,305; р=0,006), и обратную связь с ТМЖП (r=–0,246; р=0,028), длительностью комплекса QRS (r=–0,225; p=0,045) и Корнельским (r=– 0,338; р=0,003) и Губнера (r=– 0,281; р=0,013) индексами (рис. 3).
Анализ течения заболевания. Из 80 больных с АС, включенных в исследование, 7 выбыли из наблюдения по различным причинам (отказ от дальнейших контактов, переезд в другой город, смена контактных данных). В результате сведения о развитии сердечно-сосудистых осложнений и смерти от любой причины были получены у 73 больных с АС.
За период наблюдения (в среднем 1 год) 6 больных умерли (у 1 — внезапная сердечная смерть, 4 — от застойной СН; 1 — от пневмонии), у 1 развился нефатальный ИМ, у 3 — нефатальный инсульт, 5 больных были как минимум однократно госпитализированы в связи с декомпенсацией СН, 1 больному проведено протезирование АК, 2 — операция реваскуляризации на коронарных артериях.
Больные, которым было проведено протезирование аортального клапана или коронарная реваскуляризация, заканчивали участие в исследовании, последним днем оценки исходов считался день операции.
Однофакторный регрессионный анализ выявил ряд параметров, связанных с повышенной вероятностью наступления того или иного неблагоприятного исхода у больных с АС в течение 1 года наблюдения (табл. 5).
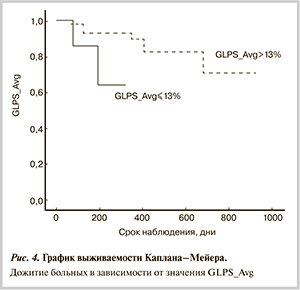
Анализ выживаемости больных с АС в зависимости от значения GLPS_Avg ниже или выше —13% проведен методом Каплана—Мейера (р=0,028) (рис. 4).
Обсуждение
Важно отметить достаточно высокую частоту «непригодности» записей ЭхоКГ для анализа стрейна ЛЖ в нашей работе. Снижение визуализации и ускорение или разброс показателей ЧСС были серьезным ограничением только для оценки стрейна ЛЖ, но не для обычного эхокардиографического исследования. Для выполнимости технологии двухмерного отслеживания пятен требуется достаточно низкая частота кадров, что делает невозможным проведение данного вида анализа при тахикардии [3]. Таким образом, применение метода стрейна для оценки дисфункции миокарда ЛЖ диктует необходимость использования новейших ультразвуковых аппаратов с высоким качеством изображения, а также тщательного контроля ЧСС больного во время исследования.
Первым примером успешного применения новых методов диагностики ранней субклинической дисфункции ЛЖ при АС стал ТД движения фиброзного кольца МК. В целом ряде работ показано снижение продольного систолического движения ЛЖ (пик S′) вслед за утяжелением степени стеноза у больных с АС и сохраненной ФВ ЛЖ [14, 15], а также независимая прогностическая значимость этого маркера ранней дисфункции ЛЖ [10]. В результате использование этого метода для оценки прогноза больных с АС было внесено в Европейские рекомендации по ведению больных с пороками сердца 2012 г. [16].
В нашей работе у больных с АС показатели систолического и раннего диастолического пиков ТД движения фиброзного кольца МК были значимо снижены по сравнению с таковыми в группе контроля и принятыми нормами (S′ и E′ ≥9 см/с). В то же время мы не обнаружили ассоциации неблагоприятных исходов с параметрами ТД.
Показатели продольного стрейна ЛЖ в нашей группе здоровых молодых людей были сопоставимы с ранее представленными данными [3].
Серьезные доказательства отсутствия «возрастного» снижения стрейна ЛЖ, оцениваемого технологией отслеживания пятен, представлены в двух недавно завершившихся крупных популяционных исследованиях. В одном из них, проведенном одновременно в Австралии, Германии и США, обследованы 242 человека в возрасте 18—80 лет без признаков ССЗ и факторов риска [17]. В другом, Фрамингемском исследовании, проанализированы данные стрейна ЛЖ в зависимости от возраста у 738 человек без признаков ССЗ, но с допущением наличия факторов риска. Кроме того, во Фрамингемском исследовании отдельно представлены средние значения GLPS_Avg для разных возрастных групп, в том числе для группы 75—84 лет, которое равнялось –20,6% [18]. Все изложенное позволяет сделать вывод, что показатели GLPS в нашей группе контроля снижены. Этот факт нельзя объяснить возрастом, но можно связать с наличием АГ практически у всех больных.
Снижение показателей стрейна ЛЖ у больных с АГ описывалось и в работах других авторов, причем снижение стрейна ЛЖ регистрируется еще до развития ГЛЖ. С появлением же ГЛЖ показатели стрейна ЛЖ достоверно снижаются [2, 19].
Дальнейшее снижение стрейна ЛЖ при присоединении к АГ аортального порока можно объяснить увеличением негативного влияния все возрастающей посленагрузки, так как по остальным клиническим характеристикам больные с пороком и без порока в нашем исследовании не различались.
Предшествующие работы по применению продольного стрейна ЛЖ у больных с АС немногочисленны, однако все фиксируют сниженные показатели стрейна ЛЖ у больных с умеренным и тяжелым АС, а также корреляцию этого показателя с площадью АК [4, 9]. Полученные нами данные согласуются с предшествующими и дополняют их сведениями о сниженном стрейне ЛЖ уже при начальной стадии порока.
Данные о взаимосвязи показателей стрейна ЛЖ с типичными для АС симптомами (обмороки, стенокардия, одышка) противоречивы [16, 20, 21]. В данной работе нам не удалось выявить взаимосвязей стрейна ЛЖ с симптоматическим статусом больных, что, по нашему мнению, свидетельствует о низкой специфичности клинических проявлений как фактора стратификации риска у больных с АС.
В нашей группе больных с АС электрокардиографические параметры, использующиеся в оценке ГЛЖ, были обратно взаимосвязаны с показателями глобального продольного стрейна ЛЖ. Хорошо известно, что с течением времени у больных с АС развивается ГЛЖ. Однако появление классических признаков гипертрофии на ЭКГ, как правило, сопровождает тяжелую степень порока и даже у больных с критическим стенозом не является обязательным. У больных с АС в нашем исследовании средние значения электрокардиографических индексов гипертрофии, а также длительность комплекса QRS не выходили за пределы нормы. Тем не менее корреляция со стрейном ЛЖ дает возможность обсуждать и изучать вопросы использования этих показателей для оценки ранней дисфункции ЛЖ при аортальном пороке.
Главным результатом нашей работы можно назвать доказательство прогностической значимости изменения продольного стрейна ЛЖ у больных с АС.
В немногочисленных исследованиях изучалась ассоциация изменений стрейна ЛЖ с вероятностью развития неблагоприятных исходов у больных с АС. Продольный стрейн ЛЖ показал свою независимую значимость в прогнозировании неблагоприятного исхода после протезирования АК у больных с тяжелым АС (n=58) [8]. Это объясняется развитием интерстициального фиброза, который находит отражение в снижении показателей продольного стрейна миокарда. В другой работе также у больных с тяжелым, но не оперированным АС (n=65) установлено, что при снижении показателя продольного стрейна ЛЖ ниже –13% значимо ухудшается прогноз по развитию сердечно-сосудистых осложнений в течение года [4]. В одной из недавно опубликованных работ снижение глобального продольного стрейна ЛЖ у больных с АС было связано с увеличением общей смертности [22].
В нашей работе продемонстрированы ухудшение общего прогноза, а также увеличение частоты декомпенсации СН у больных с АС со значением глобального стрейна ЛЖ ниже –13%.
Можно вполне уверенно предполагать, что снижение показателей продольного стрейна ЛЖ, как при АГ и ГЛЖ, так и при АС, связано с прогрессирующим развитием фиброза миокарда в условиях повышенной посленагрузки. У больных с АГ ранее показана связь сниженного стрейна ЛЖ с повышенным уровнем тканевого ингибитора матриксной металлопротеиназы 1-го типа (маркер фиброза) в крови [23]. H.C. Hermann и соавт. показали у больных с АС значимую корреляцию параметров стрейна ЛЖ с выраженностью фиброза ЛЖ, оцененную по данным биопсии, проведенной во время протезирования, и магнитно-резонансной томографии с контрастированием [24]. По-видимому, следует признать перспективными дальнейшие исследования взаимосвязи параметров стрейна ЛЖ с фиброзом миокарда.
Выводы
Больные с аортальным стенозом и нормальной фракцией выброса левого желудочка имели сниженные показатели глобального продольного систолического стрейна левого желудочка во всех трех верхушечных позициях (4-камерной, 2-камерной и по длинной оси левого желудочка), а также для всего левого желудочка, что указывает на наличие ранней дисфункции левого желудочка у больных с аортальным стенозом при любой степени тяжести порока.
Прямая корреляция стрейна левого желудочка с площадью аортального клапана и фракцией выброса левого желудочка подтверждает то, что именно порок является причиной дисфункции миокарда левого желудочка.
Глобальный продольный систолический стрейн левого желудочка при аортальном стенозе коррелирует с параметрами, характеризующими гипертрофию левого желудочка, — толщиной стенки левого желудочка и вольтажными Корнельским и Губнера индексами на электрокардиограмме, а также с длительностью интервала QRS, отражающей деполяризацию миокарда.
Глобальный продольный стрейн левого желудочка может стать параметром стратификации риска у больных с аортальным стенозом при получении подтверждения о его прогностической роли в дальнейших исследованиях.



