Распространенность гемодинамически значимого поражения ствола левой коронарной артерии — ЛКА (стеноз 50% и более) среди больных ишемической болезнью сердца (ИБС) составляет от 2,4 до 7% [1—4]. В ряде работ показано существенное увеличение смертности пациентов у этой категории при естественном течении заболевания по сравнению с аналогичным показателем после реваскуляризации миокарда [5—9]. Выполнение реваскуляризации, прежде всего коронарное шунтирование (КШ), позволяет кардинально улучшить прогноз у пациентов с поражением ствола ЛКА [10—13]. Такие доступные и относительно недорогие неинвазивные методики как электрокардиография покоя, нагрузочные тесты с электрокардиографией, на протяжении многих лет используются для диагностики ишемии миокарда и стратификации риска развития сердечно-сосудистых осложнений [14]. В то же время данные о чувствительности и специфичности электрокардиографических методик в диагностике прогностически неблагоприятного поражения коронарных артерий (КА) — стеноз ствола ЛКА >50%, стенозы >70% в проксимальных сегментах передней нисходящей артерии (ПНА) и огибающей артерии (ОА) — варьируют в широком диапазоне. В представленном обзоре литературы мы проанализировали известные публикации по электрокардиографическим методикам диагностики прогностически неблагоприятных поражений КА.
Электрокардиография покоя
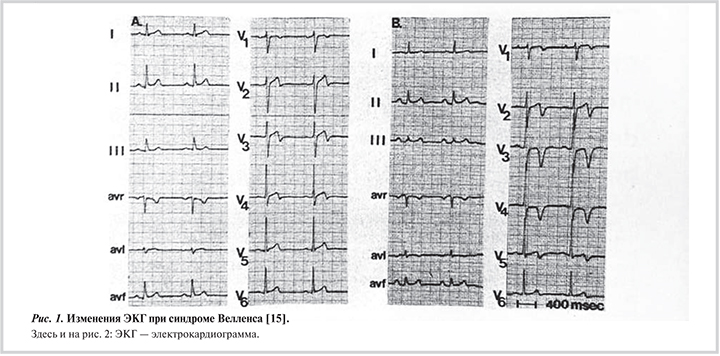
Синдром Велленса. Глубокие отрицательные зубцы Т в прекордиальных отведениях (V2 и V3) впервые были описаны группой кардиологов de Zwaan, Bär и Wellens в 1982 г. у пациентов с острым коронарным синдромом и поражением проксимального сегмента ПНА (рис. 1) [15, 16].
Клинические и электрокардиографические признаки синдрома Велленса:
Электрокардиографические признаки
- Глубокие инвертированные зубцы Т в отведениях V2—V3 (могут быть и в V1—V6)
- Сегмент ST на изолинии или незначительный подъем (менее 1 мм)
- Отсутствие патологического зубца Q в грудных отведениях
- Нормальное нарастание амплитуды зубца R в грудных отведениях
Клинические признаки стенокардии
- Изменения электрокардиограммы (ЭКГ) наблюдаются вне болевого синдрома
- Нормальный уровень или незначительное повышение маркеров некроза миокарда
Из 145 пациентов, госпитализированных с диагнозом нестабильной стенокардии, авторы обратили внимание на группу из 26 (18%) человек с изменениями сегмента ST и отрицательными зубцами Т в грудных отведениях без изменения комплекса QRS. В зависимости от того, была ли выполнена коронарография (КГ), пациенты были разделены на 2 группы: в 1-й группе (без КГ) пациенты получали стандартную на то время консервативную терапию (β-адреноблокаторы и нитроглицерин), у 8 из 9 развился инфаркт миокарда (ИМ), при этом 3 пациента умерли. Во 2-й группе была выполнена КГ, и у 12 пациентов из 13 с теми же изменениями на ЭКГ был выявлен 90% и более стеноз проксимального отдела ПНА. 9 пациентам из 2-й группы успели выполнить операцию КШ с положительным эффектом. Четверым пациентам из 2-й группы КГ проводили после перенесенного ИМ, еще двоим выполнить КШ не успели, пациенты умерли до проведения реваскуляризации. Таким образом, частота развития ИМ без реваскуляризации среди пациентов с синдромом Велленса составила 92% (12 из 13 пациентов), а летальность — 39% (умерли 5 пациентов из 13). При последующем изучении было показано, что отрицательные зубцы Т могут сохраняться на ЭКГ от нескольких часов до нескольких недель и обязательно должны быть приняты во внимание у пациентов с бессимптомными поражениями [17]. Чувствительность синдрома Велленса в диагностике стеноза проксимального сегмента ПНА составляет 92% и специфичность — 92% [18]. Риск развития ИМ при консервативном ведении пациентов с синдромом Велленса составляет 55%. Всего двоим пациентам с синдромом Велленса на ЭКГ необходимо выполнить реваскуляризацию миокарда для предотвращения одного случая ИМ. Синдром Велленса необходимо дифференцировать от других причин появления отрицательных зубцов Т на ЭКГ: тромбоэмболии легочной артерии, блокады правой ножки пучка Гиса, геморрагического инсульта, приема дигоксина, гипертрофии миокарда левого желудочка, гипокалиемии, аритмогенной дисплазии правого желудочка феноменом «электрической памяти сердца».
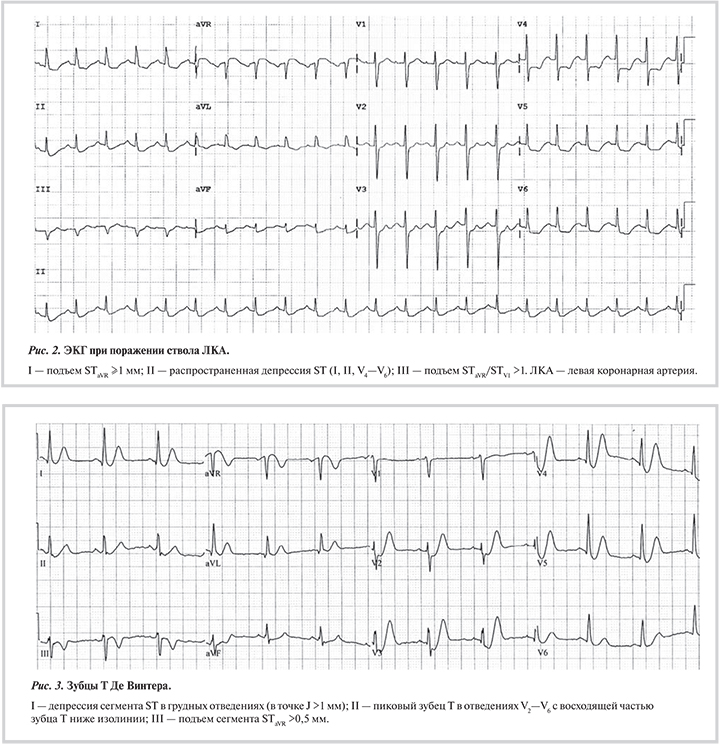
Подъем сегмента ST в отведении aVR. Отведение aVR часто незаслуженно забывается при трактовке заключений ЭКГ, тогда как при прогностически неблагоприятных поражениях КА подъем сегмента STaVR может дать бесценную информацию (рис. 2).
В исследовании D. Engelen и соавт. показано, что подъем сегмента STaVR при переднем ИМ является прогностически значимым предиктором окклюзии проксимального сегмента ПНА [19]. При изучении прогностической значимости соотношения подъема сегмента STaVR/STV1 >1 в качестве предиктора окклюзии ствола ЛКА Н. Yamaji и соавт. [20] отметили высокую чувствительность и специфичность соотношения (81 и 80% соответственно). М. Kosuge и соавт. показали, что подъем STaVR ≥0,5 мм является предиктором поражения ствола ЛКА или трехсосудистого поражения КА (чувствительность 78%, специфичность 86%) [21]. В другой работе тех же авторов отмечено, что подъем STaVR является значимым предиктором тяжелых осложнений у пациентов с ИМ без подъема сегмента ST [22]. P. Rostoff и соавт. анализировали изменения сегмента STaVR у 150 пациентов с острым коронарным синдромом (средний возраст 60,6±9,5 года), у 46 из них в последующем выявлено поражение ствола ЛКА [23]. В группе пациентов с поражением ствола ЛКА в 2 раза чаще отмечался подъем сегмента STaVR (69,6% против 34,6%; p=0,0001). Чувствительность подъема сегмента STaVR в выявлении поражения ствола ЛКА составила 69,6%, специфичность — 65,4%, прогностическая ценность положительного результата — 47,1%, а отрицательного результата — 82,9%. У пациентов с поражением ствола ЛКА чаще отмечалась депрессия ST в других отведениях (45,6% против 23,1%; p<0,01). N. Mahajan и соавт. при длительном проспективном наблюдении разделили пациентов на 2 группы: 1-я группа (n=75) состояла из пациентов с поражением ствола ЛКА, 2-я — из пациентов с поражением ПНА (n=81). Авторы обнаружили, что разница подъем STV6 — STV1 ≥0 и соотношение V6/V1 ≥1 достоверно чаще встречалась в 1-й группе. Кроме того, дельта подъема STV6 — STV1 ≥0 оказалась более точной при диагностике поражения ствола ЛКА, чем соотношение подъема STaVR/STV1 >1 [24]. В недавно опубликованной работе H. Nough и соавт. при проспективном наблюдении за 400 пациентами с острым коронарным синдромом показали, что подъем сегмента STaVR обладает высокой точностью (чувствительность 62,7%, специфичность 73,6%) в диагностике поражения ствола ЛКА [25]. Положительная прогностическая ценность подъема сегмента STaVR составила 25,8%, отрицательная — 93,1%. Очень интересными оказались результаты работы H. Yamaji и соавт., изучавших изменения ЭКГ у пациентов с острой окклюзией ствола ЛКА (n=16), ПНА (n=46) и правой КА (n=24) [26]. Подъем сегмента STaVR встречался у 14 из 16 (88%) пациентов в 1-й группе, тогда как во 2-й группе — у 20 (43%) из 46, а в 3-й группе — лишь у 2 (8%) из 24 пациентов. Амплитуда подъема STaVR также была достоверно больше в 1-й группе (0,16±0,13 мВ) по сравнению со 2-й группой (0,04±0,1 мВ). Чувствительность и специфичность такого показателя как соотношение подъема STaVR/STV1 >1 составили 81 и 80% соответственно. Кроме того, амплитуда подъема STaVR положительно коррелировала со смертностью в группе пациентов с острой окклюзией ствола ЛКА.
Своевременная реваскуляризация миокарда (КШ) у пациентов с подъемом STaVR существенно улучшает прогноз [27]. При проспективном наблюдении за 775 пациентами J. Barrabes и соавт. разделили пациентов на 3 группы: 1-ю группу (n=525) составили пациенты без подъема STaVR, 2-ю — с подъемом STaVR от 0,05 до 0,1 мВ (n=116) и 3-ю — с подъемом STaVR ≥0,1 мВ (n=134). Летальность у пациентов 1, 2 и 3-й групп составила 1,3, 8,6 и 19,4% соответственно (р<0,001). Следует отметить, что при КГ у 437 пациентов трехсосудистое поражение или стеноз ствола ЛКА были выявлены у 22, 42,6 и 66,3% пациентов в 1, 2 и 3-й группах соответственно (р<0,001). При одинаковом уровне повышения кардиоспецифических ферментов у пациентов с подъемом STaVR чаще рецидивировали ишемия миокарда и сердечная недостаточность [28].
Изменения сегмента STaVR могут встречаться в следующих ситуациях: острый перикардит, тромбоэмболия легочной артерии, синдром Бругада, кардиомипатия такацубо, нарушения проводимости, напряженный пневмоторакс, передозировка трициклических антидепрессантов, декстрокардия. При интерпретации ЭКГ у таких пациентов обязательно должна учитываться клиническая картина.
Зубцы Т Де Винтера. Изменения на ЭКГ в виде высокого пикового зубца Т с характерной депрессией сегмента ST (рис. 3) впервые описаны R. De Winter в 2008 г. у пациентов с острой окклюзией ПНА [29]. N. Verouden и соавт. в 2009 г. обнаружили подобные изменения на ЭКГ у 35 (2%) из 1890 пациентов, направленных на ЧКВ в ПНА [30].
Диагностические критерии признаков Де Винтера представлены далее.
Признаки Де Винтера на ЭКГ
- Высокие симметричные зубцы Т в грудных отведениях
- Восходящая депрессия сегмента ST в грудных отведениях в точке J >1 мм
- Отсутствие подъема ST в грудных отведениях
- Подъем сегмента STaVR (0,5—1,0 мм)
В настоящее время накапливается все больше данных о высокой чувствительности и специфичности признаков Де Винтера в диагностике поражения проксимального сегмента ПНА и ствола ЛКА. Некоторые авторы даже предлагают рассматривать зубцы Т Де Винтера как эквивалент переднего ИМ с подъемом сегмента ST.
Тесты с физической нагрузкой
Изменение сегмента ST. С момента внедрения нагрузочного теста с ЭКГ в широкую клиническую практику было предпринято множество попыток стратификации риска развития сердечно-сосудистых осложнений [14]. Далее перечислены предикторы неблагоприятного прогноза при проведении нагрузочных тестов с ЭКГ.
Прогностически неблагоприятные показатели при проведении стресс-тестов с ЭКГ (цит. по [14])
ЭКГ
- Косонисходящая или горизонтальная депрессия сегмента ST ≥1 мм при нагрузке
- Ишемическая депрессия сегмента ST ≥2 мм при минимальной нагрузке (до 2 ступени или при частоте сердечных сокращений — ЧСС ≤130 уд/мин)
- Подъем сегмента ST (кроме отведений с патологическим Q и отведения aVR)
- Направление изменений сегмента ST (косонисходящая, горизонтальная)
- Большое число отведений (>5) с депрессией сегмента ST
- Раннее появление (1 ступень) или длительная (>5 мин) депрессия сегмента ST
- ST/ЧСС индекс (6 мВ/мин)
- Парная желудочковая экстрасистолия или пробежки желудочковой тахикардии во время первых ступеней или в периоде восстановления
- Время начала изменений сегмента ST
Гемодинамика
- Низкая толерантность к физической нагрузке
- Недостаточный прирост артериального давления — АД (<130 мм рт.ст.) или снижение АД ниже исходного уровня на нагрузке
Симптомы
- Хронотропная дисфункция
- Стенокардия во время нагрузки, особенно на первых ступенях нагрузки
- Симптомы, ограничивающие продолжение нагрузки
- Время нагрузки до появления стенокардии
Что касается поражения ствола ЛКА или ПНА, то, несмотря на большое количество исследований, данные этих работ противоречивы: в ряде работ такие критерии удалось выявить, тогда как в других — нет. Это связано, скорее всего, с низкой точностью нагрузочных тестов в выявлении ишемии, их низкой специфичностью, тогда как чувствительность нагрузочных тестов с ЭКГ в выявлении прогностически неблагоприятных поражений КА оказалась высокой.
В 1981 г. D. Blumenthal и соавт. сравнили нагрузочный тест и КГ у 40 пациентов со стенокардией I функционального класса или без клинических признаков ишемии миокарда, 9 из которых перенесли ИМ и не имели симптомов заболевания [31]. Следующие критерии были проанализированы в качестве предикторов стволового поражения коронарного русла: 1) ранняя (на 1 или 2 ступени нагрузки) депрессия сегмента ST; 2) депрессия сегмента ST ≥2 мм; 3) косонисходящая депрессия сегмента ST; 4) артериальная гипотензия на пике физической нагрузки; 5) длительная (более 8 мин) депрессия сегмента ST после остановки теста; 6) депрессия сегмента ST в передних и нижних отведениях. Наибольшей точностью в определении поражения ствола ЛКА обладал критерий депрессия ST в передних и нижних отведениях.
В 1985 г. P. Siostrzonek и соавт. сравнили результаты тредмил-тестов с данными КГ у пациентов с поражением ствола ЛКА (n=29) и одно-, двух- и трехсосудистым поражением КА (n=40) [32]. Группа со стволовым поражением была разделена на пациентов с умеренным (50—70%) и значительным (>70%) стенозом ствола ЛКА. По результатам нагрузочного теста авторам удалось выделить группу со значительным стенозом и трехсосудистым поражением (депрессия ST возникала достоверно раньше и была большей амплитуды), тогда как умеренный стеноз ствола ЛКА и одно-, двухсосудистое поражение КА практически не различались. По данным КГ, при положительном результате нагрузочного теста стеноз ствола ЛКА, трех-, двух- и однососудистое поражение были выявлены у 10, 50, 23 и 16% пациентов соответственно. Таким образом, определить клинически значимые критерии поражения ствола ЛКА авторам не удалось.
A. Jánosi и соавт. в 1991 г. в рамках регистра проанализировали результаты нагрузочных тестов у 2378 пациентов, которым в последующем была выполнена КГ [33]. Поражение ствола ЛКА было выявлено у 65 (2,7%) пациентов, из них у 9 было выявлено изолированное поражение ствола ЛКА (1-я группа), у 28 — ствол ЛКА и поражение других коронарных артерий (2-я группа), у 27 — сужение ствола ЛКА, других КА и постинфарктный кардиосклероз (3-я группа), у 27 — гемодинамически значимые стенозы как ПНА, так и ОА (4-я группа). Время нагрузки, потребление кислорода, максимальная нагрузка, время депрессии ST, тип депрессии сегмента ST и максимальная величина депрессии ST достоверно между группами не различались. Авторам не удалось найти признак или группу признаков, позволяющих выделить пациентов с поражением ствола ЛКА.
T. Kawaguchi и соавт. в 1993 г. опубликовали работу, в которой попытались найти характерные для поражения ствола ЛКА признаки у пациентов с широким спектром поражения КА [34]. В работу вошли 595 мужчин с ИБС, всем пациентам были выполнены тредмил-тест и КГ, стеноз ствола ЛКА был выявлен у 42 пациентов, эквивалент стеноза ствола ЛКА (>70% стенозы в проксимальных сегментах ПНА и ОА) — у 30, однососудистое поражение — у 186, двухсосудистое — у 118, трехсосудистое — у 67, поражение ствола без вовлечения ПКА — у 26 и поражение ствола с вовлечением ПКА — у 46 пациентов. Депрессия сегмента ST увеличивалась, а фракция выброса ЛЖ, максимальная ЧСС, максимальное систолическое АД и толерантность к физической нагрузке уменьшались по мере увеличения тяжести поражения КА. Пошаговый регрессионный анализ показал, что наиболее важным предиктором тяжести поражения КА была величина депрессии ST (р<0,001), тогда как, по данным пошагового регрессионного анализа Кокса, статистически значимыми предикторами выживаемости были хроническая сердечная недостаточность, фракция выброса <50% и низкая толерантность к физической нагрузке (<5 МЕТ).
A. Garini и соавт. в 1999 г. опубликовали работу, в которой попытались найти клинические и инструментальные различия между пациентами с поражением ствола ЛКА (n=70) и трехсосудистым поражением коронарного русла (n=66) [35]. Несмотря на то что в 1-й группе достоверно чаще встречалась фибрилляция предсердий и блокада левой ножки пучка Гиса, а у пациентов 2-й группы достоверно больше было время выполнения физической нагрузки, авторам не удалось выделить клинически значимые различия между двумя группами.
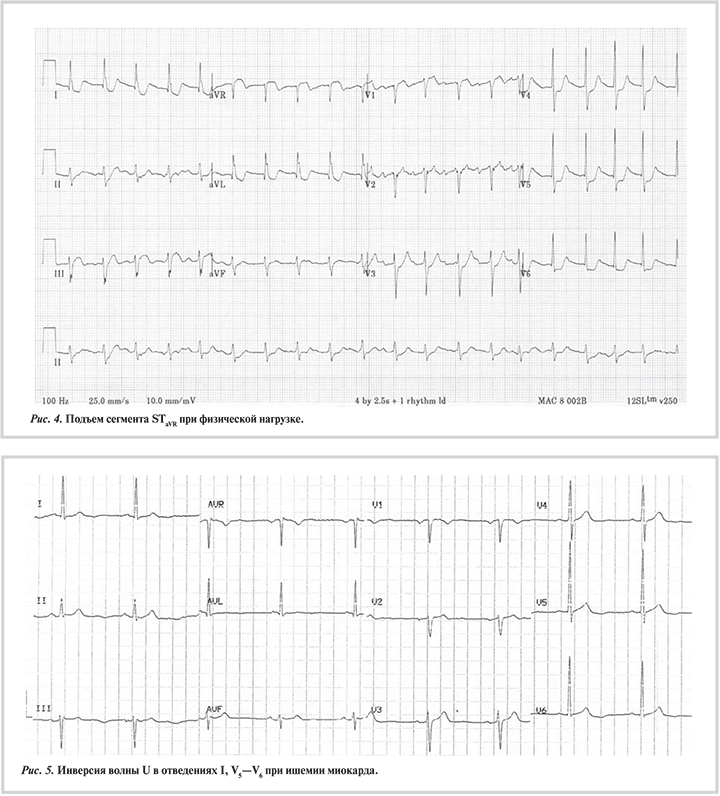
Отведение aVR и тесты с физической нагрузкой. В ряде работ была показана ценность изменения сегмента ST в отведении aVR во время физической нагрузки в диагностике прогностически неблагоприятных поражений КА (рис. 4).
A.P. Michaelides и соавт. в 1999 г. изучали изменения сегмента ST в aVR и V5 у 229 пациентов с ИБС [36]. Всем пациентам выполняли тест с физической нагрузкой, перфузионную сцинтиграфию миокарда с нагрузкой и КГ. Авторы показали, что при изолированном поражении ПНА подъем сегмента STaVR и снижение сегмента ST в V5 наблюдались у 81%. При этом у 80% пациентов с поражением ПНА отмечалась ишемия при перфузионной сцинтиграфии миокарда с нагрузкой. В 2008 г. была опубликована работа, в которой Т. Katircibaşi и соавт. определяли значение подъема ST в aVR и V1 в диагностике поражения ствола ЛКА у 104 пациентов с индексом Дюка ≤–11 [37]. У 26 (40%) из 65 с подъемом STaVR (чувствительность 92,9%, специфичность 48,6%) и у 24 (63,2%) из 38 пациентов с подъемом ST в aVR и V1 (чувствительность 85,7%, специфичность 81,6%) было выявлено поражение ствола ЛКА.
Инверсия волны U и тесты с физической нагрузкой. Инверсия волны U во время нагрузочного теста — еще один нечастый, но чувствительный маркер ишемии миокарда (рис. 5).
 M. Gerson и соавт. в 1979 г. проанализировали инверсию волны U у 248 пациентов, которым были выполнены нагрузочный тест и КГ [38]. У 36 (15%) пациентов отмечалась инверсия волны U во время нагрузки, у 35 (97%) из них при КГ было выявлено гемодинамически значимое поражение КА, а у 33 (94%) из 35 пациентов — стеноз проксимального сегмента ПНА или ствола ЛКА. Только у одного (1,2%) страдающего кардиомиопатией пациента из 82 без клинически значимого атеросклеротического поражения отмечалась инверсия зубца U. Чувствительность инверсии волны U в диагностике гемодинамически значимых поражений КА составила 21%, специфичность — 99%, а прогностическая ценность — 97%. Чувствительность инверсии волны U в диагностике поражения ПНА составила 30%, специфичность — 98%, а прогностическая ценность — 92%.
M. Gerson и соавт. в 1979 г. проанализировали инверсию волны U у 248 пациентов, которым были выполнены нагрузочный тест и КГ [38]. У 36 (15%) пациентов отмечалась инверсия волны U во время нагрузки, у 35 (97%) из них при КГ было выявлено гемодинамически значимое поражение КА, а у 33 (94%) из 35 пациентов — стеноз проксимального сегмента ПНА или ствола ЛКА. Только у одного (1,2%) страдающего кардиомиопатией пациента из 82 без клинически значимого атеросклеротического поражения отмечалась инверсия зубца U. Чувствительность инверсии волны U в диагностике гемодинамически значимых поражений КА составила 21%, специфичность — 99%, а прогностическая ценность — 97%. Чувствительность инверсии волны U в диагностике поражения ПНА составила 30%, специфичность — 98%, а прогностическая ценность — 92%.
К сожалению, нам не удалось найти современных, хорошо спланированных исследований по определению прогностической роли инверсии волны U при физической нагрузке, в литературе представлены лишь описания отдельных клинических случаев [39, 40].
Заключение
Точность диагностики прогностически неблагоприятных поражений коронарных артерий при помощи электрокардиографических методик представлена в таблице.
Проведение специально спланированной работы, в которой будут учтены все известные на сегодняшний день электрокардиографические признаки поражения ствола левой коронарной артерии и проксимального сегмента правой нисходящей артерии, по нашему мнению, позволит разработать единый алгоритм, обладающий высокой специфичностью и чувствительностью в выявлении прогностически неблагоприятных поражений коронарного русла.



