Основными компонентами структуры неблагоприятного прогноза при инфаркте миокарда (ИМ) являются не только развитие летального исхода, прогрессирование коронарной и миокардиальной недостаточности, но и развитие сосудистых осложнений в некоронарных бассейнах — экстракраниальном, артериях нижних конечностей (АНК) [1].
Атеросклеротическое поражение артерий — системный процесс, склонный к прогрессированию и распространению за пределы клинически манифестирующего бассейна, при этом поражение сосудов одного артериального бассейна является скорее исключением, чем правилом [2, 3], и ассоциируется с большей тяжестью и неблагоприятным прогнозом [4, 5]. Пациенты с мультифокальным атеросклерозом (МФА) относятся к группе очень высокого риска развития сердечно-сосудистых осложнений как при острых, так и при хронических формах ишемической болезни сердца (ИБС).
По результатам ранее проведенных немногочисленных исследований, у пациентов с ИМ и атеросклеротическим поражением некоронарных бассейнов наблюдается высокий риск развития острых сосудистых осложнений в указанных бассейнах даже при наличии гемодинамически «незначимых» стенозов [6, 7].
В литературе описаны различные факторы риска (ФР) развития и прогрессирования атеросклероза: пол, возраст, курение, избыток массы тела, нарушения липидного обмена, артериальная гипертония (АГ) и др. В исследовании J. Gariepy и соавт. [8] показана разная чувствительность каротидного бассейна и АНК к атерогенному влиянию ФР.
Таким образом, проблема МФА актуальна, и оценка факторов, повышающих риск прогрессирования периферического атеросклероза, позволит обосновать эффективные подходы к вторичной профилактике.
Цель исследования состояла в оценке связи между клинико-анамнестическими факторами и степенью прогрессирования атерoсклеротического процесса в магистральных некоронарных артериях у пациентов через год после перенесенного ИМ с подъемом сегмента ST (ИМпST).
Материал и методы
В исследование были включены 168 мужчин, перенесших в течение 2008 г. ИМпST и вошедших в регистр острого коронарного синдрома, проводимый в Научноисследовательском институте комплексных проблем сердечно-сосудистых заболеваний (НИИ КПССЗ) СО РАМН г. Кемерово.
Критериями включения были: мужской пол; диагноз ИМпST давностью до 12 ч от начала заболевания, установленный, согласно критериям Всероссийского научного общества кардиологов (2007); подписанное больным информированное согласие для участия в исследовании; факт дожития до 1 года после ИМ; полный объем исследований для выявления МФА в госпитальном периоде ИМ и возможность такого обследования через 1 год.
Критериями исключения явились: наличие значимых сопутствующих не сердечно-сосудистых заболеваний, которые могли бы влиять на прогноз; наличие факторов, ассоциированных с плохой ультразвуковой визуализацией, ограничивающей осмотр брахиоцефальных артерий (БЦА) и магистральных АНК; ИМ, возникший как осложнение чрескожного коронарного вмешательства (ЧКВ) или операции коронарного шунтирования (КШ).
Исследование выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинской декларации. Протокол исследования одобрен локальным этическим комитетом НИИ КПССЗ СО РАМН.
Средний возраст пациентов составил 59,5 (от 57,7 до 60,4) года. Клинико-анамнестическая характеристика пациентов представлена в табл. 1.
При поступлении в стационар всем пациентам в течение первых 12 ч проводили коронарографию (КГ) для оценки характера поражения коронарного русла и выявления инфарктзависимой артерии по стандартной методике Джадкинса на ангиографических установках. Коронарный кровоток оценивали по классификации TIMI [9]. Большинству больных проведена реперфузия с помощью ЧКВ — 126 (75%); 12 (7%) — аортокоронарное шунтирование (АКШ) в течение 1-го месяца после ИМ, 16 (10%) — тромболитическая терапия.
Для оценки наличия МФА всем пациентам на госпитальном этапе и через 12 мес проводили ультразвуковое цветовое дуплексное сканирование (ЦДС) БЦА и магистральных АНК на ультразвуковом диагностическом комплексе. Для обеспечения минимальной межэкспертной вариабельности измерений в работе принимали участие два специалиста функциональной и ультразвуковой диагностики высшей категории с опытом проведения более 3000 исследований ЦДС; 25% пациентов осмотрены независимо обоими специалистами. Допустимая ошибка экспертов при определении степени стенозов некоронарного русла составляла не более 5%. Измерение толщины интимы—медии (ТИМ) осуществляли, согласно стандарту: в общей сонной артерии (СА) на 1—1,5 см проксимальнее бифуркации по задней ее стенке в области максимального утолщения [10]. Наличие атеросклероза магистральных АНК оценивали путем исследования кровотока общей бедренной, подколенной и большеберцовых артерий. Основным ультразвуковым признаком, свидетельствующим о наличии атеросклеротического поражения некоронарных магистральных артерий, считали ТИМ более 1,0 мм. По степени выраженности стенозов пациенты были подразделены на группы на основе индексов стеноза NASCET и ECST: отсутствие стенозов; стеноз менее 30% (малый); стеноз 30—49% (умеренный); стеноз 50—69% (выраженный); стеноз 70—99% (критический); окклюзия [10].
Прогрессирование степени некоронарных стенозов через 12 мес оценивали как в БЦА, так и в бассейне магистральных АНК. По степени прогрессирования атеросклероза пациенты были разделены на 3 группы: отсутствие прогрессирования, умеренное и значимое прогрессирование. Умеренным прогрессированием атеросклеротического поражения считали переход из одной градации стеноза в другую с более значимым процентом сужения, значимым — при увеличении степени стеноза через группу. Сохранение прежней ультразвуковой картины принимали как отсутствие динамики.
Общий холестерин (ОХС), холестерин липопротеидов низкой плотности (ХС ЛНП), холестерин липопротеидов высокой плотности (ХС ЛВП), триглицериды определяли фотометрическим методом (фотометр КФК-3, реактивы OLVEX); кардиоспецифические ферменты — креатинфосфокиназу и фракцию МВ креатинфосфокиназы — спектрофотометрическим методом.
Через 12 мес наблюдения оценивали также наличие у пациента «конечных точек», включая смерть (кардиальную и некардиальную); повторные госпитализации по поводу повторных ИМ, нестабильной стенокардии и угрожающих жизни нарушений ритма; сердечную недостаточность (СН) и стенокардию высоких функциональных классов (III—IV), острые нарушения мозгового кровообращения (ОНМК).
Все пациенты на госпитальном этапе получали стандартную коронароактивную и дезагрегантную терапию: ацетилсалициловую кислоту — 168 (100%) больных; клопидогрел — 168 (100%); β-адреноблокаторы (метопролол, карведилол) — 165 (98%); ингибиторы ангиотензинпревращающего фермента – АПФ (эналаприл, рамиприл) — 154 (92%), нефракционированный гепарин — 168 (100%); диуретики (фуросемид, спиронолактон, гипотиазид) — 112 (66%); антагонисты кальция (дигидропиридины) — 120 (71,4%); статины (симвастатин, аторвастатин, розувастатин) — 132 (78,5%).
На амбулаторном этапе в течение 12 мес пациенты принимали ацетилсалициловую кислоту — 113 (67,3%); клопидогрел — 50 (29,7%); β-адреноблокаторы (метопролол, карведилол, бисопролол) — 120 (71,4%); ингибиторы АПФ (эналаприл, периндоприл, рамиприл) — 104 (61,9%); диуретики (фуросемид, спиронолактон, гипотиазид) — 24 (14,3%) больных; пролонгированные нитраты — 15 (8,9%); антагонисты кальция (дигидропиридины) — 58 (34,5%); статины (аторвастатин, розувастатин) — 128 (76,2%).
Статистическую обработку полученных данных осуществляли с помощью программы Statistica 8. Для относительных величин значения представлены в виде процентного соотношения, для количественных — в виде медианы, 95% доверительного интервала или среднеквадратического отклонения. Использовали непараметрические критерии сравнения неправильно распределенных сопряженных выборок (критерии знаков и Вилкоксона). Статистически значимыми считали различия при р<0,05.
Результаты
Частота выявления МФА на госпитальном этапе составила 92%. У 13 (8%) пациентов выявлен изолированный атеросклероз КА без стенозов и без признаков увеличения ТИМ в БЦА и АНК. У 33 (20%) пациентов поражение КА сочеталось с атеросклерозом БЦА или АНК, у 121 (72%) выявлялось атеросклеротическое поражение всех трех исследуемых артериальных бассейнов (КА+БЦА+АНК). Стенозы более 50% выявлены у 10 (6%) пациентов в экстракраниальном бассейне и у 10 (6%) — в АНК. Стенозы БЦА и АНК менее 30% имелись соответственно у 36 (21,4%) и 60 (35,7%) пациентов; 30—49% — у 14 (8,3%) и 22 (13,1%); 50—69% — у 4 (2,4%) и 2 (1,2%); более 70% по БЦА — у 4 (2,4%) больных. Окклюзии БЦА выявлены у 2 (1,2%) пациентов, окклюзии АНК — у 8 (4,8%). Не обнаружены атеросклеротические бляшки в СА у 108 (64,3%) больных, в АНК — у 76 (45,2%). Однако в отсутствие бляшек выявлены начальные признаки атеросклероза в виде увеличения ТИМ, его неровности, повышения плотности, неоднородности эхоструктуры. ТИМ в БЦА составила 1,17 (1,14; 1,20) мм, в АНК — 1,05 (0,96; 1,10) мм. Таким образом, частота выявления МФА у пациентов с ИМ в данном исследовании оказалась высокой.
Через год после перенесенного ИМ все 168 обследуемых имели одновременное поражение не менее двух сосудистых бассейнов. У 12 (7,1%) больных поражение КА сочеталось только с атеросклерозом БЦА, у 156 (92,9%) пациентов имелось атеросклеротическое поражение всех трех исследуемых артериальных бассейнов (КА+БЦА+АНК). В результате 12-месячного наблюдения гемодинамически значимые стенозы выявлены у 18 (10,8%) пациентов в экстракраниальном бассейне и у 12 (7,2%) — в АНК. Стенозы БЦА и АНК менее 30% имелись соответственно у 74 (44%) и 92 (54,8%) пациентов; 30—49% — у 38 (22,6%) и 38 (22,6%); 50—69% — у 8 (4,5%) и 4 (2,4%); стенозы БЦА более 70% — у 8 (4,5%) больных. Окклюзии БЦА выявлены у 2 (1,2%) пациентов, окклюзии АНК — у 8 (4,8%). Не обнаружено атеросклеротических бляшек в СА у 38 (22,6%) больных, в АНК — у 26 (15,4%). ТИМ в бассейнах без атеросклеротических бляшек в БЦА составила 1,23 (1,19; 1,27) мм, в АНК — 1,08 (0,98; 1,17) мм.
На основании динамического наблюдения степени прогрессирования атеросклероза в группу значимого прогрессирования вошли 32 (19%) пациента с поражением БЦА и 42 (25%) — АНК. Группу незначимого прогрессирования составили 96 (57%) пациентов с поражением БЦА и 104 (62%) — АНК. Отсутствовало увеличение степени стеноза в БЦА у 40 (24%) пациентов, в АНК — у 22 (13%).
При оценке частоты развития «конечных точек», по итогам 12 мес наблюдения, констатирован неблагоприятный прогноз заболевания у 22 (13%) пациентов. При этом нестабильная стенокардия в течение 12 мес наблюдения явилась поводом для повторной госпитализации у 8 (4,8%) больных, повторный ИМ — у 8 (4,8%), ОНМК развились у 6 (3,6%) пациентов. Смертельных исходов и декомпенсации хронической СН выявлено не было. Плановые процедуры реваскуляризации миокарда в течение 12 мес выполнены у 58 (34,5%) больных, из них ЧКВ — у 26 (15,5%), КШ — у 32 (19%).
В табл. 2 представлена частота развития «конечных точек» у пациентов с ИМ в зависимости от степени прогрессирования атеросклероза в БЦА. Наибольшее количество осложнений зарегистрировано у пациентов с прогрессированием атеросклеротического процесса. Необходимо указать, что только в группах с прогрессированием атеросклероза на экстракраниальном уровне зафиксированы случаи ОНМК. В группе со значимым прогрессированием ОНМК встречалось достоверно чаще, чем в группе с менее выраженным прогрессированием. ИМ за период наблюдения развился у пациентов, вошедших в группы с умеренным прогрессированием и его отсутствием. Рестенозы и тромбозы в месте стентирования КА отмечались во всех анализируемых группах. В группах больных с прогрессированием атеросклеротического процесса в БЦА рестенозы в КА диагностированы чаще, однако статистически значимых различий между группами не отмечено.
Таким образом, суммируя все «конечные точки» в группах с различной степенью прогрессирования атеросклеротического процесса, необходимо отметить, что в группах с прогрессированием атеросклероза имеется тенденция к увеличению числа случаев сердечно-сосудистых осложнений по сравнению с таковым у пациентов без прогрессирования.
При оценке влияния различной степени прогрессирования атеросклероза в АНК на риск развития неблагоприятных исходов получены следующие результаты (табл. 3). ОНМК и ИМ зарегистрированы только в группах с прогрессированием атеросклеротического процесса. Чаще в этих группах зафиксированы рестенозы и тромбозы в месте стентирования КА, однако статистически значимых различий между группами не отмечено. Вместе с тем, суммируя «конечные точки», можно отметить, что в группе значимого прогрессирования число случаев достоверно превышает таковую в группе с незначимым прогрессированием и его отсутствием.
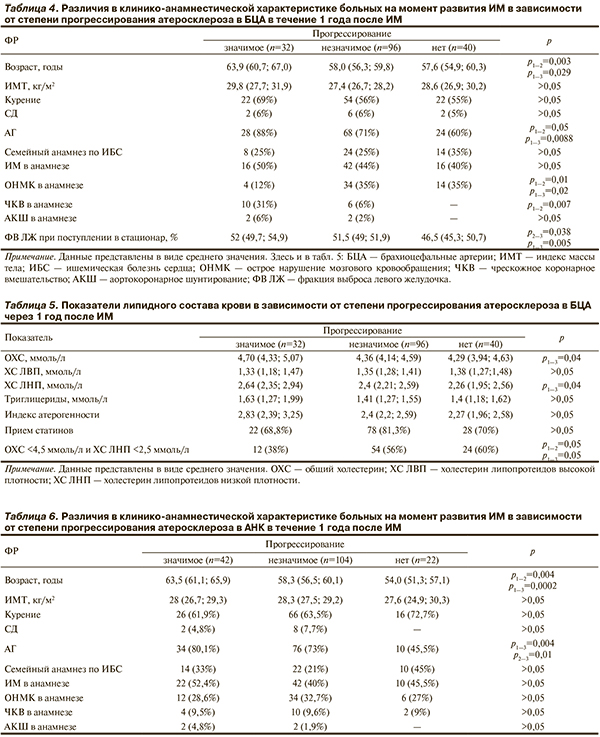
В табл. 4 представлены особенности распределения ФР у больных с различной степенью прогрессирования атеросклеротического поражения в БЦА. В группе со значимым прогрессированием пациенты были старше, чем в группах с умеренным прогрессированием и его отсутствием. Кроме того, в группе значимого прогрессирования более 50% пациентов (достоверно больше, чем в других группах) имели различной степени выраженности стенозы на экстракраниальном уровне, выявленные на госпитальном этапе. Только в группах с прогрессированием атеросклероза в анамнезе проводились процедуры ЧКВ и АКШ. Установлено, что по мере увеличения степени прогрессирования атеросклероза частота выявления у пациентов АГ была также больше. Достоверно больше пациентов с АГ выявлено в группе со значимым прогрессированием некоронарного атеросклероза. Различия по частоте перенесенных ранее до индексного события ИМ не выявлены.
Частота развития ОНМК в анамнезе в группах без прогрессирования и с умеренным прогрессированием была выше, чем в группе со значимым прогрессированием. Индекс массы тела (ИМТ), курение, наличие сахарного диабета (СД) не влияли на степень прогрессирования атеросклеротического процесса.
При анализе липидного состава крови на госпитальном этапе достоверных различий в группах не выявлено. Необходимо отметить, что, несмотря на наличие в анамнезе ИБС, число пациентов, принимавших статины до развития ИМ, оказалось крайне небольшим. При этом ни в одной из групп у пациентов не было достигнуто целевых показателей липидного состава крови.
При оценке липидограммы через 1 год после ИМ отмечены достоверно более высокие уровни ОХС и ХС ЛНП в группе со значимым прогрессированием (табл. 5). Кроме того, достоверно меньшее число пациентов в данной группе достигли целевых уровней ОХС (менее 4,5 ммоль/л) и ХС ЛНП (менее 2,5 ммоль/л). В группе со значимым прогрессированием целевые уровни достигнуты у 12 (38%) пациентов, в то время как в группе с незначимым прогрессированием — у 54 (56%), а в группе без прогрессирования — у 24 (60%). При этом следует отметить, что в группах с разной степенью прогрессирования атеросклероза доля пациентов, принимавших статины после выписки из стационара, достоверно не различалась.
Таким образом, из традиционных ФР, которые служат предикторами развития атеросклероза, значимыми для прогрессирования в БЦА явились возраст, наличие АГ, наличие и выраженность атеросклеротических стенозов на экстракраниальном уровне на момент развития ИМ, уровни ОХС и ХС ЛНП, определенные через 1 год после ИМ, а также наличие ЧКВ и АКШ в анамнезе.
При анализе ФР развития сердечно-сосудистых осложнений у больных с различной степенью прогрессирования атеросклеротического поражения в АНК в группе пациентов со значимым прогрессированием возраст также оказался достоверно больше, чем в группах с умеренным прогрессированием и в его отсутствие. Кроме того, в этой группе статистически значимым было большее число пациентов с наличием стенозов различной степени выраженности. Группы не различались между собой по ИМТ, приверженности курению, наличию в анамнезе ИМ, ОНМК, ЧКВ.
Обращает на себя внимание, что в группе без прогрессирования не было пациентов с СД, а также с наличием в анамнезе проведенных ранее АКШ. Число пациентов с АГ в группе с умеренным и значимым прогрессированием было достоверно больше, чем в группе в ее отсутствие (табл. 6).
Статистически значимых различий показателей липидограммы в разных группах как на госпитальном этапе, так и через 1 год после ИМ не выявлено. В то же время по сравнению с группами прогрессирования в группе без прогрессирования атеросклероза достоверно большее число пациентов принимали статины и достигли целевых значений показателей липидограммы. В группе без прогрессирования целевые уровни достигнуты у 18 (81%) пациентов, в группе значимого прогрессирования атеросклероза — у 18 (43%), незначимого — у 54 (52%).
Обсуждение
Настоящая работа предполагала оценку роли различной степени прогрессирования атеросклероза в развитии риска сердечно-сосудистых осложнений, в определении наиболее важных клинико-анамнестических факторов, повышающих риск прогрессирования атеросклероза. В ряде работ показано, что прогрессирование атеросклеротических бляшек заметно увеличивает риск развития клинических осложнений в любом сегменте артериального русла [11, 12].
При анализе частоты развития «конечных точек» у больных ИМ в зависимости от степени прогрессирования атеросклероза в БЦА установлено, что наибольшее число осложнений развивается у пациентов с прогрессированием атеросклеротического процесса. Необходимо указать, что только в группах с прогрессированием атеросклероза на экстракраниальном уровне зафиксированы случаи развития ОНМК. В группе со значимым прогрессированием эпизоды ОНМК встречались достоверно чаще, чем в группе с менее выраженным прогрессированием. Вместе с тем ИМ за период наблюдения развился у пациентов, вошедших как в группы с умеренным прогрессированием, так и без него.
При оценке влияния различной степени прогрессирования атеросклероза в АНК на риск развития неблагоприятных исходов ОНМК и ИМ были зарегистрированы только в группах с прогрессированием атеросклеротического процесса. Таким образом, прогрессирование атеросклероза в некоронарных сосудистых бассейнах ассоциируется с увеличением риска как коронарных, так и некоронарных осложнений.
Полученные результаты согласуются с данными, представленными S. Sabeti и соавт. [12], которые, оценивая прогностическую значимость прогрессирования атеросклеротического процесса у пациентов с бессимптомным атеросклерозом на экстракраниальном уровне, установили, что у пациентов с прогрессированием риск развития клинически значимых осложнений в разных сосудистых областях выше, чем у пациентов без прогрессирования болезни. Авторы считают, что прогрессирование стенозов в БЦА идентифицирует пациентов с высоким риском развития осложнений в коронарном, церебральном и периферическом руслах, отражая системность атеросклеротической болезни, которая затрагивает обширные части артериального дерева и объясняет сосуществование клинически значимых осложнений в данных областях. В исследовании ICARAS [19], в котором оценивали влияние прогрессирования атеросклероза на развитие осложнений у пациентов с бессимптомными атеросклеротическими бляшками, отмечено, что за 7,5 мес наблюдения инсульт развился у 3,9% пациентов с прогрессированием атеросклеротического процесса в БЦА против 0,9% у пациентов без прогрессирования.
В литературе описаны различные факторы возникновения и прогрессирования атеросклероза: пол, возраст, курение, избыток массы тела, нарушения липидного обмена, АГ. В ранее опубликованных исследованиях G. Romano [13] и F.A. Spenser [14] показано, что с увеличением возраста больных растет частота выявления мультифокального атеросклеротического поражения магистральных артерий, что предопределило и повышение частоты развития фатальных и нефатальных исходов у пациентов этой категории. У мужчин отмечена связь между ТИМ бедренной артерии и систолическим артериальным давлением (АД), уровнем глюкозы в крови, курением. При этом ТИМ СА сильнее, чем ТИМ бедренной артерии связана с возрастом, ИМТ, уровнями ОХС и ХС ЛВП.
В Роттердамском исследовании возраст, курение, ОХС, АГ были ассоциированы с умеренным и выраженным, СД — только с выраженным прогрессированием атеросклероза в БЦА и АНК [15]. В исследовании APRIS у пациентов с большей площадью атеросклеротических бляшек в нисходящей аорте выявлена более высокая распространенность АГ по сравнению с теми, у кого обнаружены мелкие бляшки или сосуд оставался интактным [16]. Значимость исходного объема атеросклеротического поражения для степени его прогрессирования описана в работе Н.С. Носенко [17]. Более выраженное прогрессирование атеросклероза в АНК описано у пациентов с исходной хронической ишемией нижних конечностей II степени и более, т.е. у пациентов с гемодинамически значимыми стенозами. Кроме того, прогрессирование атеросклеротического поражения АНК в 3 раза чаще наблюдалось у пациентов с гемодинамически значимыми стенозами в экстракраниальном бассейне, чем у тех, у кого стенозы были менее 50%; наличие же СД не влияло на степень прогрессирования атеросклероза. В исследовании S.H. Johnsen и соавт. [18] холестерин, возраст, систолическое АД и курение были независимыми предвестниками роста атеросклеротических бляшек в течение 7 лет. В исследовании ICARAS [19] возраст, курение, ОНМК в анамнезе и степень исходного стеноза БЦА были ФР прогрессирования заболевания.
Таким образом, существуют различные данные о прогностической роли тех или иных ФР в прогрессировании атеросклероза.
В настоящей работе курение, семейный анамнез по ИБС, ИМТ, наличие ОНМК и ИМ в прошлом не расценены как факторы прогрессирования атеросклероза. В качестве таких факторов определены возраст, исходное наличие атеросклеротической бляшки, АГ, уровни ОХС и ХС ЛНП, СД, АКШ и ЧКВ в анамнезе. При этом возраст, АГ, наличие исходных стенозов в БЦА, уровни ОХС и ХС ЛНП ассоциированы с прогрессированием атеросклероза в экстракраниальном бассейне. Для прогрессирования атеросклероза в АНК значение имели возраст и исходное наличие в этих сосудах атеросклеротической бляшки.
Таким образом, настоящее исследование продемонстрировало высокую частоту выявления МФА у пациентов с ИМ, а также бóльшую степень прогрессирования некоронарного атеросклероза в течение года после перенесенного острого коронарного осложнения. Феномен прогрессирования ассоциируется с большей вероятностью развития новых сосудистых осложнений в течение 1 года после ИМ. Выявление факторов, способных повышать риск прогрессирования, определяет необходимость их тщательного анализа и контроля.