Кровотечение у больных с острым коронарным синдромом (ОКС) — хорошо известный фактор неблагоприятного течения заболевания [1—3]. Возникновению кровотечений способствует использование антитромбоцитарных и антикоагулянтных препаратов, особенно в связи с выполняемыми у этих больных инвазивными процедурами (коронарография, чрескожные коронарные вмешательства). В испытаниях, в которых выявлено неблагоприятное прогностическое значение кровотечений, частота выполнения инвазивных процедур была очень высокой. Результаты этих испытаний экстраполируют и на больных, не подвергаемых инвазивному обследованию и лечению, однако фактические данные о роли кровотечений у этих пациентов практически отсутствуют. Кроме того, отсутствуют сведения о факторах, способствующих развитию кровотечений у больных с ОКС в российских стационарах, в том числе не имеющих возможностей для инвазивного обследования и лечения.
Целью настоящей работы стало выявление факторов, связанных с возникновением крупных кровотечений за время пребывания в стационаре после первичной госпитализации у больных с ОКС без подъемов сегмента ST на ЭКГ (бпST), леченных без применения инвазивных вмешательств.
Материал и методы
Набор больных осуществляли в московской клинической больнице (МКБ) №29 (стационар, не имеющий
возможности проводить инвазивное вмешательство при ОКС). Исследование было наблюдательным и не предусматривало какое-либо вмешательство в лечение.
Группы больных. Сформированы 2 группы больных: 1-я — больные с ОКСбпST, доставленные в МКБ № 29 с ноября 2009 г. по апрель 2011 г., у которых во время госпитализации развились тяжелые кровотечения; 2-я — больные с ОКСбпST без признаков крупного кровотечения (группа сравнения), эта группа сформирована из контингента регистра ОКС, осуществлявшегося в МКБ №29. В этот регистр ежемесячно (начиная с 1-го числа) включали по 25 последовательно госпитализированных больных с ОКСбпST.
Критерии ОКСпST были следующими:
— начало симптомов не более чем за 24 ч до госпитализации И;
— симптомы, заставляющие предположить ОКС (ангинозная боль в покое ≥ 20 мин, впервые возникшая стенокардия как минимум III функционального класса, нарастание класса стенокардии до III функционального класса) И;
— отсутствие на электрокардиограмме (ЭКГ) признаков ОКС с подъемами сегмента ST (может не быть никаких изменений на ЭКГ).
Критерии тяжелого кровотечения. Развившееся в стационаре кровотечение считалось крупным, или тяжелым, если оно соответствовало критериям тяжелого кровотечения по шкале GUSTO или TIMI. Тяжелым по шкале GUSTO считаются внутричерепные кровотечения, а также кровотечения, вызывающие нестабильность гемодинамики или обусловливающие необходимость вмешательства [4].
Тяжелыми кровотечениями по шкале TIMI считаются внутричерепные кровотечения, любые видимые кровотечения (в том числе с помощью различных методов визуализации) со снижением уровня гемоглобина (Hb) на >50 г/л или гематокрита (Ht) на ≥15%, случаи тампонады сердца, а также случаи, когда кровотечения являлось причиной смерти [5].
Методика формирования группы сравнения (контрольной). К каждому больному с ОКСбпST и развившимся в стационаре тяжелым кровотечением подбирали больных с ОКСбпST без тяжелого кровотечения. Принципы подбора были следующими:
— соотношение больных с кровотечением и без него 1:3;
— больные с крупным кровотечением и без них должны были соответствовать друг другу по возрасту;
— если соответствующих по возрасту больных без кровотечения было >3, то для анализа отбирали тех
из них, дата поступления которых в стационар была более близкой к дате поступления соответствующего больного с кровотечением. Это было необходимо, чтобы избежать возможной системной ошибки, связанной с различием в лечении, обусловленным наличием или отсутствием
различных препаратов в стационаре.
Некоторые определения. Упоминаемые ниже перенесенные заболевания и состояния регистрировали на основании расспроса больных либо имеющихся предыдущих медицинских документов.
Для оценки риска развития ишемических осложнений и кровотечений использовали прогностические шкалы GRACE и CRUSADE, а также шкалу РЕКОРД, созданную на основании данных одноименного ограниченного Российского регистра ОКС. Границы высокого риска были следующими: по шкале GRACE — >140 баллов [6], по шкале РЕКОРД — ≥2 балла [7], по шкале риска развития кровотечений CRUSADE — >40 баллов [8].
Критерием для диагностики инфаркта миокарда (ИМ) были клинические, электрокардиографические, лабораторные критерии: повышение уровня фракции МВ креатинфосфокиназы (МВ-КФК) или тропонина Т, а также данные эхокардиографии.
Взятие крови для определения уровней гемоглобина, гематокрита, лейкоцитов, креатинина осуществляли сразу при поступлении больных в стационар. Взятие крови для определения КФК и ее фракции МВ выполняли в момент поступления, а также повторно несколько раз через 6—12 ч в последующие 2 сут.
Статистическая обработка данных. Для статистической обработки данных использовали пакет программ Statistica 6.0. Сравнение дискретных величин проводили с применением критерия χ2 с коррекцией непрерывности по Йетсу, непрерывных с неправильным распределением — методом непараметрической статистики Манна— Уитни. Статистически значимым считалось различие при
р<0,05.
Результаты
С ноября 2009 г. по апрель 2011 г. у 24 больных с ОКСбпST были зарегистрированы признаки тяжелого
кровотечения по одному из вышеупомянутых критериев.
За это же время в больничный регистр были включены 507 больных с ОКСбпST, из которых выбраны 72
больных без тяжелых кровотечений, соответствующих по возрасту больным с кровотечениями. Основные демографические, анамнестические данные у больных с тяжелым кровотечением в стационаре и без него представлены в табл 1.
В табл. 2 представлены сравнительные данные, полученные при поступлении в стационар больных с развившимся впоследствии тяжелым кровотечением и без него.
Частота использования различных лекарственных препаратов до развития ОКС и после у больных с тяжелым кровотечением в стационаре и без него представлена в табл. 3.
Таблица 1. Демографические, анамнестические данные больных с ОКСбп ST c тяжелым кровотечением и без него в стационаре.
Таблица 2. Сравнительные клинические данные, полученные при поступлении в стационар больных с развившимся за время пребывания в стационаре тяжелым кровотечением и без него.
Таблица 3. Частота использования различных лекарственных препаратов у больных с тяжелым кровотечением в стационаре и без него.
Острый ИМ диагностирован у 79,2% больных с развившимся в стационаре тяжелым кровотечением и у 40,3% без тяжелого кровотечения (р=0,001).
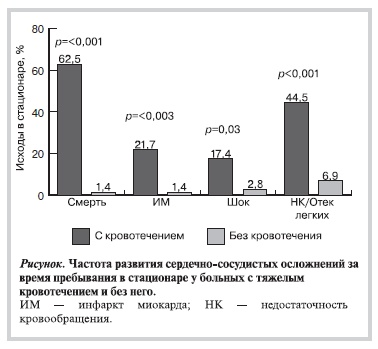
Частота сердечно-сосудистых осложнений, развившихся в стационаре у больных с тяжелым кровотечением и без него, представлена на рисунке.
Летальность больных с ОКСбпST и тяжелым кровотечением была чрезвычайно высокой (62,5%). Из 15 больных, умерших за время пребывания в стационаре, кровотечение было непосредственной причиной смерти у 4 (26,7%): у 3 больных — тяжелое желудочно-кишечное кровотечение, у одного — геморрагический инсульт.
Кровотечения у 8 (33,3%) больных лечили только с использованием лекарственных средств, у 9 (37,5%)
выполнена гемотрансфузия, у 4 (16,7%) — хирургическое
лечение.
Обсуждение
Согласно современным рекомендациям для лечения ОКС используется одновременно несколько антитромботических препаратов [6]. В связи с этим у больных с ОКС, в том числе у тех, кто не подвергался инвазивным вмешательствам, повышается риск развития кровотечений. При этом чем выше у больных риск развития ишемических осложнений ишемической болезни сердца, тем требуется активнее использовать антитромботические препараты, а это повышает риск развития геморрагических осложнений. В клинической практике порой нелегко соблюсти баланс между предотвращением как ишемических, так и геморрагических осложнений. Таким образом, очевидно, что тема поиска связи лечения в ранний период ОКС с развитием тяжелых кровотечений важна и актуальна. Представленная работа была построена по принципу регистра, что позволило вовлечь широкий круг больных с ОКС (т.е. максимально приблизить изучаемую группу больных к реальной клинической практике).
Строгий подбор больных в группу сравнения был предпринят для того, чтобы исключить влияние посторонних факторакторов на риск кровотечений. В отличие от традиционного подбора контрольных групп, сопоставимых по полу и возрасту, в настоящем исследовании мы сделали иначе. Женский пол является хорошо известным предиктором развития кровотечений у больных с ОКС
[7, 9]. Поэтому пары подбирали только по возрасту. При этом единственным искусственно оставленным ФР кровотечений был возраст.
Группы больных с тяжелым кровотечением и без него в стационаре были сопоставимы по большинству демографических и анамнестических данных. Исключение составили больные с хронической почечной недостаточностью и кровотечениями в прошлом, число которых оказалось достоверно больше в группе с кровотечением.
При поступлении в стационар среди больных с развившимся впоследствии кровотечением было достоверно больше пациентов с признаками недостаточности кровообращения — НК (Killip ≥2), а также больных с повышенными оценками по шкале GRACE. Связь прогностической шкалы GRACE не только с ишемическими, но и геморрагическими осложнениями была продемонстрирована ранее [10]. Другим важным отличием больных с развившимся кровотечением была достоверно более высокая частота развития ИМ. Эта находка — еще одно подтверждение того, что ФР развития ишемических
и геморрагических осложнений во многом схожи.
Больные с кровотечением и без него достоверно отличались оценками по шкале GRACE, но не по шкале CRUSADE, которая специально создана для оценки риска кровотечений. Недавно появившиеся рекомендации Европейского кардиологического общества по ОКСбпST предлагают использовать эту шкалу при определении тактики лечения больных [6].
Отсутствие различий между группами по шкале CRUSADE сложилось из-за того, что в группе без кровотечений было относительно много больных с высоким риском кровотечений (см. табл. 2). По-видимому, это могло быть связано с особенностями дизайна работы: группа больных без кровотечений соответствовала по возрасту группе с кровотечениями, в которой было очень много пожилых больных. Так как ряд факторов шкалы CRUSADE отчасти зависят от возраста (почечная недостаточность, сосудистые заболевания, сахарный диабет), то не удивительно, что в группах, одинаковых по возрасту, эти факторы могут нивелироваться. В результате может исчезать различие между группами по шкале CRUSADE. Нельзя не учитывать и то, что эта шкала создавалась на материале крупного регистра в США, в котором многие больные подвергалась инвазивному лечению [8]. Высокая значимость шкалы для прогнозирования геморрагических осложнений подтверждена также на больных ОКСбпST, подвергавшихся катетеризации сердца [11]. Авторы соответствующей публикации подчеркнули, что для оценки применимости шкалы CRUSADE в подгруппе больных, получающих 2 антитромботических препарата или более и не подвергаемых катетеризации сердца,
нужны дополнительные исследования.
Если больные с последующим тяжелым кровотечением и больные без кровотечений в среднем получали одинаковое лечение до развития ОКС, то в лечении, проводившемся на догоспитальном этапе, обнаружены некоторые различия. Больные, у которых впоследствии развилось тяжелое кровотечение, реже получали потенциально опасные в отношении кровотечений препараты — ацетилсалициловую кислоту и парентеральные антикоагулянты. Это можно, по крайней мере, отчасти объяснить тем, что у больных с развившимся в последующем кровотечением было больше ФР кровотечений (см. табл. 1), что и учитывали принимавшие решения о лечении работники бригады скорой медицинской помощи.
Больные с развившимся тяжелым кровотечением в первые 24 ч пребывания в стационаре достоверно реже, чем больные без кровотечений, получали низкомолекулярные гепарины — НМГ (эноксапарин). Не исключено, что это могло быть связано с тем, что больным из группы высокого риска реже проводится лечение более современными препаратами, в том числе НМГ. Подобная тенденция
была выявлена еще в регистре РЕКОРД [12].
Существующие данные неоднозначно оценивают влияние НМГ и нефракционированных гепаринов (НФГ) на частоту кровотечений. Так, в исследовании ESSENCE не выявлено достоверных различий по частоте крупных кровотечений за 30 дней у больных с ОКСбпST, лечившихся НФГ или эноксапарином (7% против 6,5%) [13].
Мета-анализ результатов лечения больных с тромбозом глубоких вен с применением НФГ или НМГ показал преимущество последнего в отношении развития крупных кровотечений (отношение шансов 0,57 при 95% доверительном интервале — ДИ от 0,39 до 0,83) [14]. В крупном шведском обсервационном исследовании среди более 3000 больных, получавших НФГ или НМГ, частота умеренных и тяжелых кровотечений была достоверно выше у леченных НФГ (отношение шансов 4,72 при 95% ДИ от 2,17 до 10,30; p<0,001) [15]. У больных, включенных в регистр ОКС GRACE, использование НМГ (только НМГ, без «перекреста» с другими антикоагулянтами) ассоциировалось с достоверно меньшей частотой кровотечений (отношение шансов 0,7 при 95% ДИ от 0,57 до 0,85; p=0,0003) [16].
Таким образом, данные, полученные в нашей работе, можно рассматривать как косвенное подтверждение того, что применение НМГ, в частности эноксапарина, у больных с ОКС связано с меньшим риском тяжелых кровотечений. Хотя следует отметить, что эноксапарин использовался только у 20% пациентов группы сравнения. Соответственно маловероятно, что именно он был существенным фактором, способствовавшим отсутствию кровотечений в этой группе.
В отношении ассоциации использования диуретиков с возникновением кровотечений данные нашей работы также совпадают с результатами регистра GRACE. В нем диуретики были одним из факторов, достоверно связанных с крупным кровотечением у больных с ОКС (отношение шансов 1,69 при 95% ДИ от 1,44 до 1,99; р<0,0001) [16]. Частота применения диуретиков в первые 24 ч пребывания в стационаре в нашей группе больных также была достоверно больше у пациентов с тяжелым
кровотечением. Это, очевидно, обусловлено тем, что среди них было достоверно больше больных с НК (Killip ≥2) (см. табл. 2).
Обращает внимание большая частота проведения гемотрансфузий для лечения кровотечений в нашем
исследовании — около 5% у всех больных с ОКСбпST. Это почти в 2 раза больше, чем, например, в исследовании ACUITY [17]. Существующие данные указывают на связь гемотрансфузий с неблагоприятными исходами у больных с ОКС [18], хотя выделить роль именно переливания крови среди различных эффектов крупного кровотечения, безусловно, чрезвычайно трудно.
В целом результаты нашей работы показали, что в группе российских больных с ОКС, поступавших в обычный «неинвазивный» стационар, с развитием тяжелых кровотечений связаны известные предикторы геморрагических осложнений, включая использование диуретиков.
Заключение
Тяжелые кровотечения (по классификации TIMI или GUSTO у больных с острым коронарным синдромом
без подъемов сегмента ST, не подвергнутых инвазивному лечению, в период госпитализации, 1) были связаны с их известными предикторами: сердечной и почечной недостаточностью, кровотечениями в анамнезе; 2) возникали у больных с высоким риском развития ишеми-ческих осложнений и смерти и были сопряжены с очень высокой летальностью. У больных с острым коронарным синдромом без подъемов сегмента ST с тяжелым кровотечением по сравнению с больными без кровотечений на разных этапах лечения реже применялись некоторые антитромботические средства.



