Аортальные пороки (АП) сердца входят в число самых распространенных среди приобретенных пороков. Социальная значимость пороков аортального клапана обусловлена тем, что они поражают людей трудоспособного возраста и являются одной из причин ранней инвалидности и смертности. Статистические наблюдения за естественным течением аортального стеноза (АС) показали, что после появления симптомов нарушения кровообращения при лекарственном лечении ко 2-му году после начала медикаментозного лечения умирают 50% больных. При естественном течении клинически выраженного АС смертность в течение 10 лет составляет 80—90% [1]. Распространенность АС среди клапанных пороков сердца составляет 3—7%, с увеличением возраста частота его выявления возрастает до 15—20% [2].
Из данных литературы также известно, что у пациентов с гипертрофией левого желудочка (ГЛЖ) при систолической перегрузке может развиться типичная стенокардия без окклюзионного заболевания коронарных артерий [3].
Как известно, развитие гипертрофии проходит 3 стадии: 1) компенсаторная гипертрофия; 2) стабильная гипертрофия; 3) истощение миокарда с развитием сердечной недостаточности. Так как в компенсации АС принимает участие мощный левый желудочек (ЛЖ), порок длительное время протекает без расстройств кровообращения. Длительный период компенсации — особенность этого порока [4]. Поэтому в случае, если ЛЖ поддерживает необходимый минутный объем кровообращения, состояние больного остается стабильным до тех пор, пока прогрессирующий кардиосклероз, фиброэластоз эндокарда и коронарная недостаточность не приведут к сердечной декомпенсации [5].
После операции и регрессии массы ЛЖ наблюдается тенденция к нормальному отношению размера коронарных артерий к массе ЛЖ [6]. В результате коррекции АП устраняется препятствие оттоку крови из ЛЖ и, таким образом, происходит снижение нагрузки на миокард ЛЖ, что влечет за собой снижение потребности сердечной мышцы в кислороде и соответственно перестройку микроциркуляторного кровотока (МЦК) [7].
Целью настоящего исследования явилась оценка функционального состояния МЦК в стенках различных камер сердца до и после коррекции порока у пациентов с АС при различной стадии ХСН.
Материал и методы
Обследованы 52 пациента до и после хирургической коррекции порока, средний возраст 54,2±1,2 года, с АС III—IV степени, ХСН II—IV функционального класса (ФК) по Нью-Йоркской классификации.
Диагноз ставили на основании данных эхокардиографии (ЭхоКГ) с определением площади отверстия аортального клапана, а также пикового систолического градиента давления между ЛЖ и аортой (СГЛЖ/Ао). У всех пациентов площадь отверстия аортального клапана составила от 1 до 0,7 см², СГЛЖ/Ао — выше 80 мм рт.ст. Всем больным проводилась электрокардиография, при которой были зарегистрированы признаки ГЛЖ, а также рентгенологическое исследование с регистрацией аортальной конфигурации сердца.
Критерием включения было наличие приобретенного АС. У всех больных использовали стандартное анестезиологическое пособие и методы защиты миокарда. Инотропную поддержку в интраоперационном периоде не использовали. Критерием исключения было наличие сопутствующей органической патологии клапанов, наличие ИБС с хирургически значимым поражением коронарного русла, наличие сахарного диабета. В общей группе было 40 (77%) мужчин и 12 (23%) женщин. У 75% включенных в исследование пациентов в аортальную позицию были имплантированы механические протезы, у 25% — биологические протезы.
У всех пациентов исследовали микроциркуляторный кровоток стенок камер сердца с помощью метода лазеродопплеро-флоуметрии (ЛДФ) на BLF-21 Transonic System Inc(США) в комплексе с персональным компьютером.
Метод ЛДФ — быстродействующий неинвазивный прямой количественный метод определения величины перфузии крови в ткани в реальном времени в миллилитрах на 100 г ткани в минуту, позволяющий оценить состояние кровотока на капиллярном уровне, который оказывает непосредственное влияние на метаболические процессы в органах и тканях. Исследование микроциркуляции стенок различных камер сердца у пациентов с АС не проводилось другими авторами.
Записи МЦК производили во время операции на работающем сердце поверхностным датчиком типа «R» (rite angle) в течение 20 с на эпикарде каждой камеры сердца: центральная часть левого и правого предсердий (ЛП, ПП), боковая поверхность левого желудочка (ЛЖбп), а также область верхушки левого желудочка (ЛЖв), передняя поверхность правого желудочка (ПЖ) с последующим расчетом средней величины кровотока. Фиксировали исходные показатели МЦК перед хирургической коррекцией порока и подключением аппарата искусственного кровообращения (АИК) и после устранения порока и отключения аппарата АИК на фоне стандартного анестезиологического обеспечения.
Одновременно с МЦК регистрировали основные показатели гемодинамики: АДС, АДД, АДср. и ЧСС. Для оценки степени ГЛЖ у всех пациентов по данным ЭхоКГ анализировали размеры и объемы ЛЖ: конечный диастолический размер (КДР), конечный систолический размер (КСР), конечный диастолический объем (КДО), конечный систолический объем (КСО), толщину межжелудочковой перегородки (ТМЖП) и толщину задней стенки (ТЗС) ЛЖ, размеры правого и левого предсердий до коррекции порока и в ранний послеоперационный период (7—10-е сутки после операции). Систолическую функцию ЛЖ оценивали по фракции выброса (ФВ), используя данные ЭхоКГ до и в ближайшие сроки после коррекции порока. Рассчитывали индексированные показатели ЛЖ: ИКДО, ИКСО — конечный диастолический и конечный систолический объемы, отнесенные к площади поверхности тела. Кроме того, анализировали СГЛЖ/Ао до и после коррекции порока при снятии нагрузки на ЛЖ. Для определения величины ГЛЖ рассчитывали массу миокарда ЛЖ (ММЛЖ) по формуле N. Reicheck и R. Devereux и затем ее отнесенную к площади поверхности тела величину индекса ММЛЖ (ИММЛЖ) [8]. При наличии ГЛЖ, по данным приведенных авторов, ИММЛЖ превышает 118 г/м2 у мужчин и 104 г/м2 у женщин. Относительную толщину миокарда определяли по формуле:
ОТМ=2 × ТЗСЛЖ/КДР [9].
У всех пациентов был выявлен концентрический тип ГЛЖ.
Статистическую обработку полученных данных проводили с использованием пакета прикладных программ Statistica 6.1. Для определения статистической значимости различий применяли методы вариационной статистики. Данные представлены в виде среднего ± ошибка среднего (M±m). Для всех проведенных анализов различия считали достоверными при уровне значимости p<0,05, где минимальная достоверность различий составила 95%.
Результаты
В зависимости от ФК ХСН все больные были разделены на 2 группы: в 1-ю группу (n=40; 77%) вошли пациенты с ХСН II ФК, 2-ю группу составили больные (n=12; 23%) с ХСН III—IV ФК. По возрасту и антропометрическим показателям группы пациентов были сопоставимы.
На рис. 1, 2 представлены результаты МЦК до и после коррекции порока у пациентов 2 групп. В 1-й группе пациентов с ХСН II ФК средний МЦК до коррекции порока колебался от наиболее высокого по ЛЖв — 85,8±5,2 мл/100 г/мин до наиболее низкого в области ЛП — 62,4±4,2 мл/100 г/мин (см. рис. 1). Таким образом, уровень микроциркуляции по стенкам правых отделов сердца и по ЛЖв составлял более 80 мл/100 г/мин, МЦК по ЛЖбп также был на высоком уровне — более 75 мл/100 г/мин. В свою очередь МЦК по ЛП до операции статистически значимо был ниже, чем при МЦК.
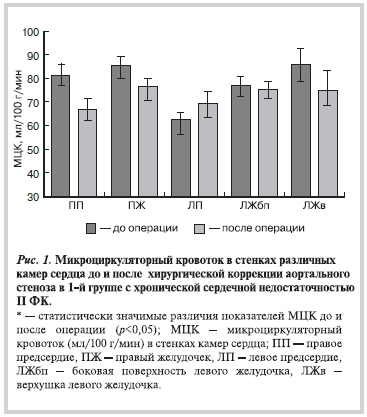
В 1-й группе с изначально высоким МЦК по стенкам всех камер сердца, кроме ЛП, после коррекции АП происходило перераспределение кровотока по всем камерам. Средние различия МЦК между камерами сердца до операции составляли 23,4 мл/100 г/мин (между ЛЖв и ЛП), после операции градиент по МЦК значительно снизился и составил 5,8 мл/100 г/мин (между ЛЖбп и ЛП). При этом уровень МЦК статистически значимо снизился в области ПП и ПЖ (р<0,05). Микроциркуляторный кровоток по ЛЖбп практически не изменился, оставаясь на высоком уровне (более 70 мл/100 г/мин), а по ЛП имел тенденцию к повышению, что составило около 70 мл/100 г/мин. Уровень МЦК по ПП после операции был достоверно ниже, чем по ПЖ и ЛЖбп (р<0,05) (см. рис. 1).
Таким образом, в 1-й группе после операции происходило равномерное распределение МЦК по стенкам всех камер сердца со значительным снижением градиента МЦК.
По данным ЭхоКГ, в 1-й группе пациентов с ХСН II ФК средний уровень ФВ ЛЖ оставался в пределах нормы — 62%, СГЛЖ/Ао был высоким, что составило около 90 мм рт.ст., выявлены значительное увеличение ТЗСЛЖ, МЖП, увеличение ММЛЖ, ИММЛЖ, а также размеров ЛП и ПП. В ближайшие сроки после операции отмечена тенденция к уменьшению размеров и объемов ЛЖ, ММЛЖ и ИММЛЖ. Отмечено статистически значимое снижение СГЛЖ/Ао и размеров ЛП (табл. 1).
Таблица 1. Динамика показателей ЭхоКГ до хирургической коррекции АС и в ближайшие сроки после нее у пациентов 1-й группы с ХСН II ФК
Примечание. Здесь и в табл. 2: ЭхоКГ — эхокардиография; АС — аортальный стеноз; ХСН — хроническая сердечная недостаточность; ФК — функциональный класс; ФВ — фракция выброса; КДР — конечный диастолический размер; КСР — конечный систолический размер; КДО — конечный диастолический объем; ИКДО — индекс конечного диастолического объема; КСО — конечный систолический объем; ИКСО — индекс конечного систолического объема; СГЛЖ/Ао — пиковый систолический градиент давления между ЛЖ и аортой; ТЗСЛЖ — толщина задней стенки левого желудка; ТМЖП — толщина межжелудочковой перегородки; ММЛЖ — масса миокарда левого желудочка; ИММЛЖ — индекс массы миокарда левого желудочка; ЛП — левое предсердие; ПП — правое предсердие; * — достоверность различий с данными до операции (p<0,05)
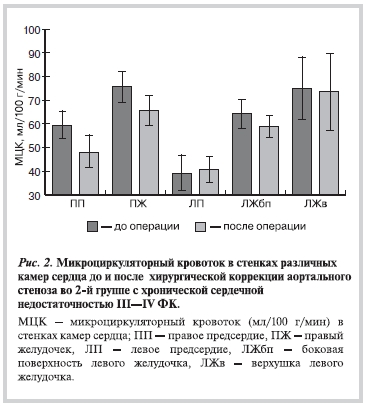
При исследовании МЦК различных камер сердца у пациентов 2-й группы с ХСН III—IV ФК было выявлено, что МЦК до коррекции АП по ПЖ и по ЛЖв составил более 70 мл/100 г/мин, МЦК по ЛЖбп был в пределах 64 мл/100 г/мин. В свою очередь уровень МЦК по ЛП до операции был очень низким — около 40 мл/100 г/мин и статистически значимо различался с МЦК других камер сердца (р<0,05) (см. рис. 2).
Таким образом, во 2-й группе показатели МЦК колебались от 76,0±7,2 мл/100 г/мин по ПЖ до наиболее низкого — 39,4±7,7 мл/100 г/мин по ЛП. Высокий МЦК отмечался только по ЛЖв и по ПЖ, что составило более 70 мл/100 г/мин (см. рис. 2).
После коррекции АП во 2-й группе происходила тенденция к снижению уровня МЦК по стенкам ПП, ПЖ и ЛЖбп. Микроциркуляторный кровоток по ЛЖв практически не изменился и составил более 70 мл/100 г/мин. При этом отсутствовало увеличение МЦК в области ЛП, где после операции уровень МЦК в этом отделе оставался значительно сниженным — в пределах 40 мл/100 г/мин. Средние различия МЦК между камерами сердца до операции в данной группе составили 36,6 мл/100 г/мин (между ПЖ и ЛП), после операции градиент по МЦК между данными камерами умеренно снизился, но при этом еще оставался достаточно высоким — 25,1 мл/100 г/мин.
Таким образом, во 2-й группе после операции сохранялся высокий градиент по МЦК между камерами сердца за счет низкого уровня МЦК по ЛП.
По данным ЭхоКГ, во 2-й группе пациентов с ХСН III—IV ФК средний уровень ФВ ЛЖ был ниже нормы — в пределах 39%. В данной группе было также выявлено значительное увеличение размеров и объемов ЛЖ, ММЛЖ, ИММЛЖ, размеров ЛП и ПП, СГЛЖ/Ао (табл. 2). В ближайшие сроки после операции в данной группе выявлены статистически значимое увеличение ФВ ЛЖ — до 48% с уменьшением СГЛЖ/Ао, снижение размеров и объемов ЛЖ, а также размеров ЛП и ПП. Отмечена тенденция к уменьшению ММЛЖ и ИММЛЖ.
Таблица 2. Динамика показателей ЭхоКГ до хирургической коррекции АС и в ближайшие сроки после нее у пациентов 2-й группы с ХСН III—IV ФК
Сравнительный анализ двух групп позволил выявить, что наиболее выраженный градиент МЦК между камерами сердца до и после коррекции порока наблюдался во 2-й группе пациентов с ХСН III—IV ФК. В этой же группе до операции выявлен наиболее низкий МЦК по стенкам ПП и ЛП (p<0,05). По желудочкам сердца наиболее низкий уровень МЦК также отмечен во 2-й группе, но статистически значимых различий выявлено не было. После коррекции порока во 2-й группе пациентов определялся статистически значимо наиболее низкий уровень МЦК по ПП, ЛП и ЛЖбп. При этом МЦК в области ЛЖв в обеих группах практически не различался между собой и был на достаточно высоком уровне — более 70 мл/100 г/мин.
Наряду с наиболее низким МЦК до и после операции по левым отделам сердца и ПП по сравнению с 1-й группой во 2-й группе пациентов с ХСН III—IV ФК отмечены наиболее высокие абсолютные и индексированные показатели размеров и объемов ЛЖ (p<0,05) как до, так и в ближайшие сроки после операции: КДР, КСР, КДО, ИКДО, КСО, ИКСО. Кроме того, во 2-й группе до и после операции фиксировались наиболее высокие показатели ММЛЖ, ИММЛЖ, а также размеры ЛП и ПП (p<0,05) (см. табл. 1, 2). Систолический градиент ЛЖ/Ао до и после коррекции АП достоверно не различался в двух группах, как ТМЖП и ТЗСЛЖ.
Таким образом, во 2-й группе пациентов с ХСН III—IV ФК до и после коррекции АС выявлен наиболее низкий уровень МЦК по стенкам левых отделов сердца и в области ПП, а также наиболее высокие абсолютные и индексированные показатели ЛЖ и предсердий по данным ЭхоКГ. ФВ ЛЖ во 2-й группе до и в ближайшие сроки после коррекции АС статистически значимо была ниже, чем в 1-й группе.
По интраоперационным показателям центральной гемодинамики (ЧСС, АДС, АДД, АДср.) после коррекции АП отмечались достоверно более низкие показатели ЧСС во 2-й группе (p<0,05) по сравнению с 1-й группой. По остальным показателям — АДС, АДД, АДср. до и после операции не было выявлено статистически значимых различий между двумя группами.
Обсуждение
Часто исходом АС является декомпенсация гипертрофированного сердца в связи с тем, что процесс гипертрофии ограничен возможностью кровоснабжения органа. Со временем, по мере нарастания массы органа, возникает относительная недостаточность кровоснабжения, т.е. возникает хроническая ишемия. Нарушаются обменные процессы в гипертрофированном сердце, возникают дистрофические изменения, а затем необратимые изменения — гибель клеток с разрастанием на их месте соединительной ткани, т.е. развивается сердечная недостаточность, которая и является причиной смерти [10].
Естественно, что перфузионные нарушения миокарда развиваются с различной скоростью у разных больных; при этом возможно выделение начальной стадии, когда наблюдается усиленная перфузия (возможно, вследствие достаточно полноценного ангиогенеза), и поздней стадии, когда отмечается снижение перфузии вплоть до появления перфузионных дефектов миокарда ЛЖ. Нарушение МЦК в миокарде больных с АП имеет существенное значение для развития ХСН, а также для появления ишемических очагов в миокарде [11].
В нашем исследовании указанные морфологические изменения в гипертрофированном сердце на фоне АС отражены в снижении объемной скорости МЦК в стенках левых его отделов во 2-й группе с ХСН III—IV ФК, что позволяет констатировать срыв компенсаторных механизмов микрососудистой системы без адекватного поддержания энергоснабжения кардиомиоцитов в данных отделах сердца и как следствие — снижение сократительной функции миокарда ЛЖ. Данное снижение уровня микроциркуляции в левых отделах сердца сопровождалось выраженной ГЛЖ со значительным увеличением абсолютных и индексированных его размеров и объемов, а также выраженным увеличением ММЛЖ, ИММЛЖ и размеров обоих предсердий по сравнению с нормой. В этой же группе после коррекции АС оставался сниженным МЦК по левым отделам с сохранением высокого градиента МЦК между ЛП и ПЖ. Наиболее высокий уровень МЦК наблюдался в области верхушки ЛЖ как до, так и после коррекции АП, вероятно, за счет того, что здесь отмечается максимальная сила сокращения, которая поддерживается высоким уровнем кровотока.
В свою очередь низкий уровень МЦК по ЛП как до, так и после операции в группе пациентов с ХСН III—IV ФК можно связать с дисфункцией ЛЖ, повлекшей за собой дилатацию стенок ЛП, и как следствие — снижение функции данного отдела сердца. Эти изменения в ЛП сопровождались застойными явлениями в малом круге кровообращения с умеренным повышением давления в легочной артерии (около 42 мм рт.ст.). Это подтверждается данными других авторов, изучавших клинико-гемодинамические результаты после протезирования клапанов сердца, где снижение скорости кровотока в ушке ЛП авторы объясняли выраженностью дисфункции ЛЖ. Изменения предсердного комплекса при пороках АК эти авторы связывают с хроническим воздействием гипертрофии и дилатации ЛЖ на ЛП, чему способствует появление митральной недостаточности, ведущей к понижению диастолической податливости [12].
Заключение
Ремоделирование сердца при ХСН может проявляться по-разному. У отдельных больных оно носит адаптивный характер и не приводит к значительному увеличению размеров полости ЛЖ, поддержанию сократительной способности его и стабилизации миокардиального стресса (в нашем исследовании это наблюдалось в 1-й группе пациентов с ХСН II ФК и средней ФВ ЛЖ 62%). У других больных ремоделирование приводит к прогрессирующей дилатации ЛЖ, росту миокардиального стресса и снижению его сократительной функции (что наблюдалось во 2-й группе с ХСН III—IV ФК при средней ФВ ЛЖ 39%). Эти морфофункциональные изменения носят дезадаптивный характер и приводят к появлению клинических признаков ХСН [13]. Таким образом, процесс ремоделирования сердца у различных больных неоднозначен и может носить как адаптивный, так и дезадаптивный характер, что зависит, по-видимому, от сложного взаимодействия определяющих его факторов, в том числе генетического. При выраженной гипертрофии миокарда и недостаточности сердца имеются признаки срыва и полного истощения компенсаторно-приспособительных механизмов коронарных артерий и микроциркуляторного русла [14]. По нашим данным, именно в группе пациентов с ХСН III—IV ФК результаты нарушения компенсаторно-приспособительных механизмов микроциркуляции с дезадаптивным ремоделированием ЛЖ привели к снижению объемной скорости микроциркуляторного кровотока по левым отделам сердца с сохранением высокого градиента между предсердиями и желудочками.
На основании изложенного можно сделать вывод, что по мере прогрессирования анатомо-функциональных изменений ЛЖ на фоне аортального стеноза и развития ХСН снижается объемная скорость микроциркуляторного кровотока в стенках левых отделов сердца.



