«Если бы я не курил, я убежден,
что без страданий прожил бы еще несколько лет»
С.П. Боткин
С 1 июня 2013 г. за исключением нескольких положений вступил в силу Федеральный закон Российской Федерации от 23 февраля 2013 г. № 15-ФЗ «Об охране здоровья граждан от воздействия окружающего табачного дыма и последствий потребления табака», запрещающий курение в общественных местах, спонсорство и рекламу табака, а также вовлечение детей в употребление табака. Принятые радикальные меры на столь высоком уровне акцентируют внимание на проблеме и последствиях курения. И это обоснованно, поскольку тривиальные профилактические мероприятия, проводимые врачами (беседы, школы и т.п.) для искоренения этой привычки, не решают всей проблемы.
Никотиновая зависимость является причиной смерти каждого десятого жителя планеты, приводя к 5 млн смертей в год [1]. При этом по оценкам специалистов, в 2030 г. смертность от курения составит 10 млн человек в год [2]. В настоящее время 46,3 млн человек (25,7% от населения планеты) являются курильщиками [3], в их числе 24 млн мужчин и 22,3 млн женщин. Чаще употребляют табак лица молодого возраста (25—44 года). В США курение и его последствия являются причиной смерти 440 тыс. человек в год, в странах Европейского Союза это число достигает 500 тыс. человек [4]. В то время как в экономически развитых странах число курящих стабилизировалось или снижается, в развивающихся странах их число увеличивается примерно на 3,4% в год.
Распространенность курения в Российской Федерации чрезвычайно высока: среди взрослого населения курят 60% мужчин и около 22% женщин [5]. Курение резко снижает продолжительность жизни (мужчины, которые выкуривают ≥10 сигарет в день, а женщины ≥6 сигарет в день, живут соответственно на 10,5 и 6 лет меньше тех, кто не курит [6]). Это в очередной раз подтверждает обоснованность мер борьбы с этой пагубной привычкой.
Компоненты табачного дыма. Кроме никотина листья табака содержат от 70 до 300 химических веществ, которые под действием высоких температур образуют компоненты табачного дыма. Табачный дым представляет собой гетерогенный аэрозоль с частицами размером 0,2—0,5 мкм. Парадокс химического состава сигарет состоит в том, что в процессе курения происходит потребление не тех веществ, которые содержатся в изделии, а тех, которые образуются в результате его сгорания (а это более 4000 компонентов). Все компоненты табачного дыма в зависимости от физико-химических свойств могут быть разделены на 3 группы:
- сильнодействующие и физиологически активные вещества (никотин, анабазин, синильная кислота и др.);
- газовые компоненты (оксиды углерода, цианистый водород, ацетон, изопрен и др.);
- твердые составляющие (фенол, калий, натрий, цинк, мышьяк и др.).
Данные, приведенные в таблице, демонстрируют некоторые свойства компонентов табачного дыма. Никотин служит естественной защитой табачного растения от поедания насекомыми. В равных количествах никотин обладает в 3 раза большей токсичностью, чем мышьяк. Случайным образом это естественное средство защиты от насекомых оказалось близким по химической структуре ацетилхолину, который ответственен за передачу нервных импульсов в головном мозге человека. Смертельная доза никотина для человека составляет 100 мг. В одной сигарете содержится 1,0—2,5 мг никотина, а в пачке из 20 сигарет — 20—50 мг.
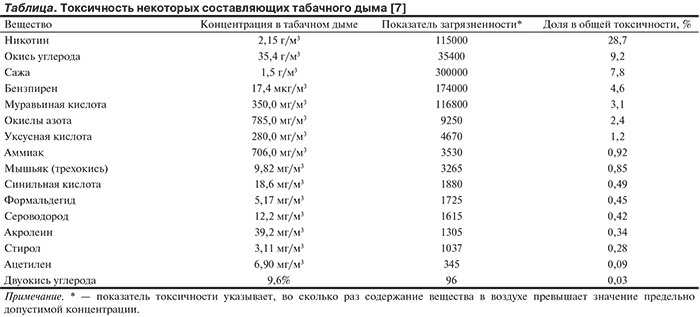
Кроме никотина в табачном дыме содержатся смолы, угарный газ (монооксид углерода, способность которых связываться с гемоглобином в 200 раз выше, чем у кислорода), синильная кислота (цианистый водород, который ингибирует активность железосодержащих ферментов, ответственных за процессы внутриклеточного и тканевого дыхания), акролеин, оксиды азота (усиливают адсорбцию никотина; ингибируют эндогенную продукцию NO), свободные радикалы (участвуют в реализации оксидантного стресса), металлы (хром, никель, кадмий, железо), радиоактивные вещества (полоний-210, свинец-210, калий-4, радий-228, торий-228, цезий-134, 137) и многие другие компоненты. Кроме того, табачный дым содержит в своем составе канцерогены. Среди известных канцерогенов табачного дыма можно выделить полициклические ароматические углеводороды и нитрозамины (действие которых обусловлено образованием соединений с молекулами ДНК, изменением ее структуры и последующим злокачественным ростом клеток).
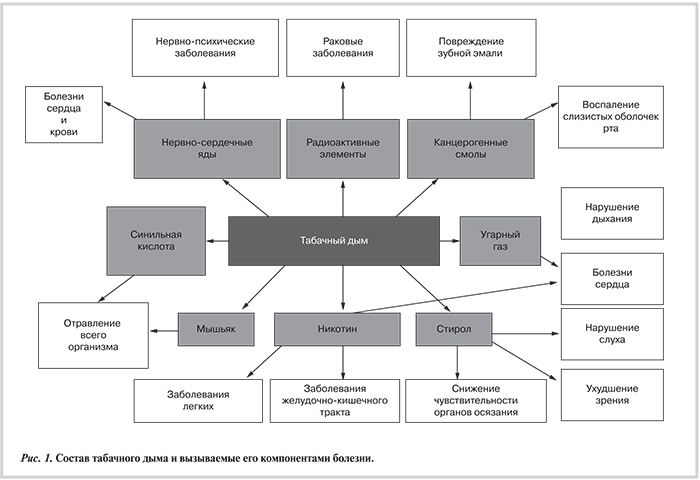
Каждый из компонентов табачного дыма в большей или меньшей степени участвует в развитии повреждений систем и органов организма человека. Рис. 1 наглядно иллюстрирует роль некоторых элементов в развитии различных заболеваний.
Влияние табачного дыма на сердечно-сосудистую систему. Курение служит фактором риска развития заболеваний многих систем и органов человека, в том числе сердечно-сосудистых заболеваний (ССЗ). Эффект никотина и других компонентов табачного дыма развивается сразу же после начала курения. Можно выделить несколько патогенетических звеньев, через которые опосредуются эффекты курения на ССЗ.
Курение способствует воспалению, повышению проагрегантной активности тромбоцитов, активации оксидантного стресса. Установлено, что вещества, входящие в состав табачного дыма, вызывают дисфункцию и повреждение эндотелия путем образования эндотелина, супероксидных анионов, снижения продукции NO [8, 9]. Под влиянием компонентов табачного дыма происходит активация симпатической части вегетативной нервной системы. Это приводит к высвобождению катехоламинов, стимулирует продукцию вазопрессина. В результате происходит повышение артериального давления (АД) и увеличение числа сердечных сокращений (ЧСС). Длительное стойкое повышение АД и ЧСС увеличивает потребность миокарда в кислороде, что клинически может проявляться в виде ишемии, стенокардии напряжения или дисфункции миокарда.
В одном из исследований 10 курильщиков с нормальным уровнем АД выкуривали по 1 сигарете каждые 15 мин в течение 1 ч. При этом уровни АД и ЧСС измерялись во время курения и в течение 1 ч после курения. Другие 6 курильщиков с нормальными уровнями АД выкуривали по 2 сигареты в 1 ч в течение всего дня, при этом измерение АД и ЧСС проводилось каждые 10 мин в течение 8 ч. В первой группе пациентов выраженный подъем АД и ЧСС отмечался после выкуривания первой сигареты, а достигнутый пик сохранялся при выкуривании всех последующих сигарет. Гемодинамический ответ был отчетливо выражен, а уровни АД и ЧСС в период курения были достоверно выше соответствующих гемодинамических показателей в последующий час без курения. Во второй группе уровни АД и ЧСС также были выше во время курения, чем без курения. Авторы исследования пришли к выводу, что курение связано со стойким повышением АД и ЧСС [10]. Снижение АД и ЧСС отмечалось на 20-й минуте после прекращения курения. Исследование показало, что клинически значимое снижение АД и ЧСС достижимо только при полном отказе от курения. Уместно будет упомянуть, что по результатам анализа крупных международных исследований (MRC, HDFP, MRFIT, ANBP) смертность среди курящих пациентов с артериальной гипертензией в 2 раза выше, чем среди некурящих больных.
Курение увеличивает агрегацию тромбоцитов и способствует ускорению тромбобразования.
Таким образом, курение приводит к нарушениям эндотелийзависимой вазодилатации коронарных сосудов, повышению АД, ЧСС и ускорению процессов тромбообразования. Эти факторы и являются патофизиологическими звеньями, которые приводят к увеличению риска коронарных осложнений у курящих пациентов.Кроме того, следует обратить внимание, что компоненты табачного дыма оказывают клинически значимое влияние на эффективность лекарственных препаратов, которые применяются в кардиологии (β-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента, диуретики и др.):
- на фармакокинетическом уровне: путем нарушения процессов всасывания лекарственных препаратов, их связи с белками, метаболизма и элиминации;
- на фармакодинамическом уровне: за счет воздействия компонентов табачного дыма на физиологические процессы организма, с одной стороны, и за счет изменения реактивности органов-мишеней у курильщиков — с другой.
Курение и длина теломеров. Результаты клинических последних исследований свидетельствуют, что отрицательные эффекты курения можно проследить даже на молекулярно-генетическом уровне. Для полного понимания вопроса авторы настоящей статьи позволят себе напомнить о структуре и функциях теломеров.
Теломеры представляют собой специализированные концевые районы линейной хромосомной дезоксирибонуклеиновой кислоты (ДНК), состоящей из многократно повторяющихся коротких нуклеотидных последовательностей и связанных с ними белков [11]. У человека теломеры состоят из повторов (TTAGGG)n, длина составляет от 2 до 20 тыс. пар нуклеотидных остатков (т.п.н.).
Основными функциями теломеров являются следующие [12]:
- Механические: теломеры участвуют в фиксации хромосом к ядерному матриксу.
- Стабилизационные: а) если в клетке нет теломеразы, то наличие теломеров предохраняет от недорепликации генетически значимые отделы ДНК; б) если же в клетке есть теломеразная активность, то появляется еще одна возможность — стабилизация концов разорванных хромосом. В присутствии же теломеразы к местам разрыва присоединяется теломерная ДНК. Это стабилизирует хромосомные фрагменты и позволяет им функционировать.
- Влияние на экспрессию генов: активность генов, расположенных рядом с теломерами, снижена (репрессирована). При значительном укорочении теломеров эффект положения пропадает и прителомерные гены активируются.
- «Счетная» функция: теломерные отделы ДНК выступают в качестве часового устройства, которое отсчитывает количество делений клетки после исчезновения теломеразной активности. После этого нарушается клеточный цикл и, в конечном счете, клетка погибает.
С каждым последующим делением клетки длина теломеров укорачивается. Когда длина теломеров в соматической клетке достигает критической (менее 2 кб), наступает резкое изменение метаболизма клетки (в первую очередь происходит нарушение репликации ДНК), запускаются механизмы клеточного старения и апоптоза, за которыми следует гибель клетки. Таким образом, очевидно, что теломеры играют одну из ключевых ролей в процессе старения клетки.
Известно, что короткие теломеры ассоциируются с риском развития ССЗ. В частности, ассоциативные связи прослеживаются между короткими теломерами и артериальной гипертензией [11], хронической сердечной недостаточностью (ХСН) [12], атеросклерозом [13]. От длины теломеров зависит время наступления смерти клетки. При этом артериальная гипертензия, ХСН и атеросклероз являются «спутниками» старения. Несмотря на внушительное количество исследований, в настоящее время нет единого мнения экспертов о причинно-следственной связи между длиной теломеров и развитием ССЗ.
Связь между длиной теломеров и ССЗ иллюстрирует рис. 2. Следует заметить, что многие из факторов, которые играют важную роль в развитии ССЗ, в одинаковой степени влияют и на скорость укорочения теломер в хромосомах. В рамках данного обзора остановимся на процессе курения.
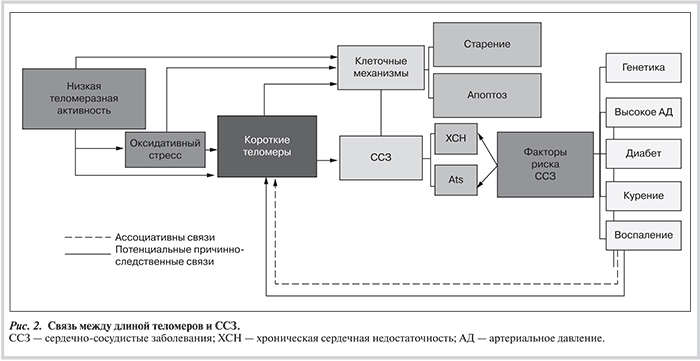
Группа исследователей во главе с A.M. Valders анализировали связь между длиной теломеров и курением у женщин [14].С этой целью в исследование были включены 1122 женщины в возрасте 18—76 лет. Из них 531 (47%) никогда не курила, 369 (33%) курили в прошлом, но на момент включения в исследование отказались от курения, 203 (18%) курили на момент включения в исследование. Установлено, что с каждым годом у испытуемых длина теломеров укорачивалась на 27 пар оснований. При этом женщины, которые никогда не курили, имели бо'льшую длину теломеров, чем те, которые курили. Удалость выяснить, что длина теломеров снижалась пропорционально количеству выкуренных сигарет. Каждая упаковка сигарет была эквивалентна потере 5 пар оснований (или 18% от среднегодовой потери) длины теломеров с поправкой на возраст по сравнению со скоростью укорочения теломеров в общей когорте.
M. Morla и соавт. определяли связь между курением листьев табака и скоростью укорочения теломеров у пациентов с хронической обструктивной болезнью легких (ХОБЛ) [15]. С этой целью в исследование были включены 76 мужчин, из них 26 никогда не курили, 24 курили, но имели нормальные показатели функции легких, 26 имели ХОБЛ. Возраст участников исследования составил от 40 до 75 лет. Было установлено, что лица, которые курят табак (вне зависимости от наличия признаков ХОБЛ), имеют меньшую длину теломеров по сравнению с некурящими пациентами.
Исследование под руководством J. Huzen также свидетельствует о том, что курение способствует укорочению теломеров [16]. В общей сложности было изучено 16 783 образцов ДНК у 8074 участников исследования (возрастной диапазон участников 39—60 лет). Продолжительность исследования составила 10 лет. Установлено, что активное курение является основным независимым фактором, определяющим скорость истощения теломеров (p<0,0001). Кроме того, значительную роль (но в меньшей степени) играют компоненты метаболического синдрома (отношение окружности талии; р=0,007; уровень глюкозы в крови; р=0,045; уровень холестерина липопротеидов высокой плотности; р<0,001).
Подобные результаты в отношении влияния курения табака на длину теломеров получены в исследовании под руководством L. Mirabello [17]. В исследование были включены 612 лиц, у которых был диагностирован рак предстательной железы, и 1049 человек контрольной группы (без рака предстательной железы). Установлено, что у курящих пациентов длина теломеров была статистически значимо меньше, чем у лиц, которые никогда не курили.
Негативное влияние курения на длину теломеров прослеживается и в других исследованиях. Ниже приведены результаты некоторых из них.
- Длина теломеров у курильщиков (n=82) меньше, чем у лиц, которые не курят (n=189): 6,72 (р=0,06) и 6,91 кб (р=0,04) соответственно [18].
- Длина теломеров больше у лиц, которые никогда не курили (n=118), по сравнению с лицами, которые курят (n=62) или курили, но на момент включения в исследование отказались от курения (n=193) [19].
- В исследовании с участием 635 пациентов у курильщиков (33,7%) отмечалась меньшая длина теломеров по сравнению с лицами, которые не курили табак (с поправкой на возраст 7,370 и 7,492 кб соответственно; р=0,0479). Средний возраст пациентов на момент включения в исследование составлял 31,4 года [20].
- В исследовании с участием 1203 пациентов (средний возраст 59 лет, 51% женщины), длина теломеров была статистически меньше у курящих, чем у пациентов, которые никогда не курили табак, — 6,84±0,04 (р=0,0012) и 7,0158±0,03 (р=0,0012) кб соответственно [21].
Таким образом, перечисленные исследования свидетельствуют о том, что активное курение табака негативно сказывается на длине теломеров. В свою очередь увеличение скорости укорочения теломеров является причиной раннего старения клетки и организма в целом.
Заключение
Роль курения в развитии различных заболеваний широко известна и доказана. В то же время ввиду сложного компонентного состава табачного дыма остаются неизвестными многие механизмы повреждающего действия на органы-мишени. В настоящее время в достаточной мере изучены эффекты патологического влияния никотина и других компонентов табачного дыма на сердечно-сосудистую систему. Одним из механизмов влияния курения на общую продолжительность жизни и риск развития сердечно-сосудистых заболеваний может быть отрицательное влияние компонентов табачного дыма на скорость укорочения теломеров в хромосомах. Активное курение способствует истощению теломеров. В свою очередь короткие теломеры ассоциируются с развитием артериальной гипертензии, хронической сердечной недостаточности, атеросклероза и других хронических заболеваний. Данный механизм заслуживает более детального изучения. Тем не менее очевиден факт: отказ от курения является основным принципом профилактики сердечно-сосудистых заболеваний.



