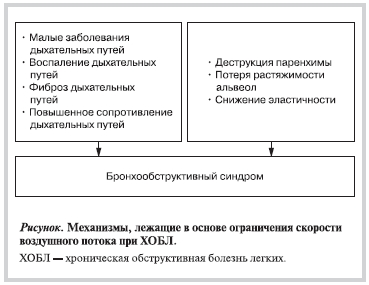
Хроническая обструктивная болезнь легких (ХОБЛ) — предупреждаемое и поддающееся лечению заболевание, характеризующееся постоянным ограничением воздушного потока, которое со временем прогрессирует и связано с повышенной хронической воспалительной реакцией в дыхательных путях и легких в ответ на попадание в них вредных частиц или газов [1] (см. рисунок). ХОБЛ остается одной из основных проблем общественного здравоохранения.
Существующие данные о распространенности ХОБЛ вариабельны. Это связано с различиями в методах обследования, диагностических критериях и аналитических подходах [2]. Однако не менее 6% взрослого населения в большинстве стран мира страдают ХОБЛ [2—3].
В целом проблема роста распространенности ХОБЛ связана с сохраняющимися факторами риска (ФР) ее развития. Распространенность ХОБЛ обусловлена в основном двумя «большими» ФР: курением табака и загрязненностью воздуха, а также тенденцией к постарению населения, а, следовательно, старению дыхательных путей и паренхимы [1, 4—5].
Систематический обзор и мета-анализ исследований, проведенных в 28 странах в период с 1990 по 2004 г., дополнительные исследования в Японии свидетельствуют, что распространенность ХОБЛ заметно выше у курильщиков и бывших курильщиков, чем у некурящих, у лиц старше 40 лет по сравнению с более молодыми, у мужчин по сравнению с женщинами [1, 6]. По данным латиноамериканского проекта PLATINO [7], распространенность ХОБЛ варьирует от 7,8 до 19,7%.
В последние годы отмечается рост заболеваемости ХОБЛ среди женщин [8] и значительное распространение (3—11%) этой патологии среди никогда не куривших [9]. В Российской Федерации более 11 млн человек страдают ХОБЛ [10].
ВОЗ ежегодно публикует статистические данные о смертности по отдельным причинам смерти для всех регионов. В 10-м пересмотре МКБ смертность от ХОБЛ входит в широкую категорию «ХОБЛ и смежные состояния» (коды МКБ-10 J42-46). По этой причине данные о летальности должны интерпретироваться осторожно [11—13].
По результатам международных плацебо-контролируемых исследований TORCH [14], Uplift [15], Eclipse [16], смертность больных в течение 3 лет увеличивалась в зависимости от степени тяжести ХОБЛ с 11% при умеренной ХОБЛ до 24% при крайне тяжелой ХОБЛ.
В настоящее время ХОБЛ занимает 4-е место по причине смертности во всем мире [1, 17—19]. По прогнозам ВОЗ, к 2020 г. ХОБЛ будет занимать 3-е место в мире по летальности и 5-е — по экономическим затратам [1, 19]. Так, в странах Европейского союза около 6% бюджета здравоохранения приходится на заболевания легких. Из них 56% трат — на ХОБЛ (38,6 млрд евро) [20]. В США на лечение ХОБЛ расходуется 49,9 млрд долларов в год, из них чуть менее половины приходится на непрямые траты [21].
Поскольку ХОБЛ практически всегда связана с длительным курением у больных среднего и пожилого возраста, то у таких пациентов часто наблюдается сопутствующая патология, для которой курение и возраст также являются ФР [22—25]. В первую очередь это касается сочетания ХОБЛ с сердечно-сосудистыми заболеваниями (ССЗ) [26]. Патология сердечно-сосудистой системы — не только наиболее частое, но и наиболее важное по влиянию на прогноз коморбидное состояние при ХОБЛ [22, 26]. Таким образом, сочетание ССЗ и ХОБЛ является предметом междисциплинарного изучения терапевтами, кардиологами и пульмонологами [27].
Тактика ведения больных с ХОБЛ в сочетании с ССЗ. Эксперты Global Initiative for Chronic Obstructive Lung Disease (GOLD) в пересмотре документа от 2011 г. указывают, что отказ от курения является наиболее важным вмешательством, направленным на замедление прогрессирования ХОБЛ (уровень доказательности А) [1]. Но всегда ли это возможно в условиях реальной клинической практики?
Зачастую пациенты продолжают курить, а врачи вынуждены использовать медикаментозную терапию с целью коррекции коморбидных состояний с учетом негативного воздействия на организм никотина. При выборе препарата у больных с ХОБЛ в сочетании с ССЗ нужно руководствоваться следующими принципами:
• препарат должен эффективно улучшать состояние сердечно-сосудистой системы;
• отсутствие негативного влияния на бронхиальную проходимость;
• отсутствие клинически значимого гипокалиемического эффекта;
• косвенно препарат должен уменьшать степень системной воспалительной реакции;
• препарат должен оказывать антиоксидантное действие;
• отсутствие прокашлевого действия;
• отсутствие взаимодействия с бронхолитическими препаратами.
• по возможности препарат должен способствовать уменьшению легочной гипертонии;
• препарат должен снижать агрегацию тромбоцитов;
• препарат не должен оказывать неблагоприятное влияние на органы-мишени [28—29].
В настоящем обзоре будут рассмотрены наиболее часто встречаемые сопутствующие ССЗ у лиц с ХОБЛ: ишемическая болезнь сердца (ИБС): стенокардия, постинфарктный кардиосклероз, сердечная недостаточность (СН), фибрилляция предсердий (ФП), а также артериальная гипертензия (АГ) и тактика ведения больных в различных клинических ситуациях.
ИБС. Распространенность ИБС увеличивается у лиц с ХОБЛ в некоторой степени из-за неблагоприятного профиля риска ИБС у больных ХОБЛ [25, 26, 30—34]. Анализ данных литературы свидетельствует о высокой распространенности ИБС у больных ХОБЛ: от 21 до 61,7% [35—38]. Так, данные исследования, полученные J. Chen и соавт. при участии 201 752 пациентов с ИБС, показали, что ХОБЛ встречается у таких больных в 21% случаев [39]. В исследовании А.М. Шилова и соавт. при участии 70 больных распространенность ИБС у больных с ХОБЛ составила 47,5% [40].
Существует доказательство того, что ишемические изменения миокарда упускаются из виду у больных ХОБЛ и, следовательно, не выставляется диагноз ИБС [41].
Стенокардия, постинфарктный кардиосклероз. Большинству пациентов со стенокардией, либо после перенесенного инфаркта миокарда показано назначение β-адреноблокаторов.
Эта группа препаратов используется в клинике с середины 60-х годов XX века. Основным свойством β-адреноблокаторов является способность блокировать β-адренергические рецеп торы. Главная проблема при выборе препарата из группы β-адреноблокаторов — наличие бронхиальной обструкции. Это обусловлено тем, что при их назначении происходит блокада не только β1-адренорецепторов, которая обусловливает антиангинальный и антигипертензивный эффекты этих препаратов, но и β2-адренорецепторов, что приводит к спазму средних и мелких бронхов, а ухудшение вентиляции легких вызывает гипоксемию, что клинически проявляется усилением одышки и учащением дыхания. Большое значение для клиники имеет степень кардиоселективности, т.е. влияние на β1- и β2-рецепторы: у метопролола это соотношение составляет 1:20, у атенолола — 1:35, у бисопролола — 1:75 [42]. Небиволол превосходит бисопролол по кардиоселективности в 3,5 раза. Кардиоселективность β-адреноблокаторов снижается или полностью исчезает при назначении высоких доз препаратов [43]. Отдельно следует отметить блокатор β- и α-рецепторов карведилол. Уникальность препарата в том, что одновременная блокада α- и β-адренорецепторов благоприятна для пациентов с ХОБЛ. α-Адреноблокада вызывает небольшую бронходилатацию, которая противостоит бронхоконстрикции, возникающей при блокаде β-адренорецепторов [44].
И.Е. Чазова приводит результаты мета-анализа, опубликованного в 2002 г., 19 плацебо-контролируемых исследований, в которых использовали атенолол, метопролол, бисопролол, практолол, целипролол и ацебутолол [45]. Было установлено, что применение этих β-адреноблокаторов не отличается от плацебо по влиянию на вентиляционные и дыхательные симптомы при назначении β2-агонистов. Это позволило авторам сделать вывод о том, что кардиоселективные β-адреноблокаторы не ухудшают дыхательную функцию и их применение безопасно у больных ХОБЛ [46].
В 2004 г. в Европейском журнале «Сердце» был опубликован согласительный документ по применению β-адреноблокаторов у пациентов с ССЗ. В нем указано, что β-адреноблокаторы могут вызывать угрожающее жизни повышение сопротивления дыхательных путей и поэтому противопоказаны пациентам с бронхиальной астмой и бронхообструктивными формами ХОБЛ [47]. Эксперты GOLD (2011) считают, что преимущества назначения кардиоселективных β-адреноблокаторов при ИБС превышают потенциальные риски, связанные с лечением, даже у пациентов с тяжелой ХОБЛ. Бронхиальная астма, тем не менее, должна считаться противопоказанием к назначению β-адреноблокаторов, но ХОБЛ не является противопоказанием к их назначению [1, 46]. А.Ю. Гурова и соавт. приводят данные, полученные в голландском ретроспективном обсервационном исследовании при участии 3371 пациентов, которым выполнялась кардиоваскулярная операция в период между 1990 и 2006 гг. в Erasmus Medical Center, Роттердам [35]. Исследование включало 1265 (39%) пациентов с ХОБЛ, из которых 462 (37%) принимали кардиоселективные β-адреноблокаторы. Среди пациентов с ХОБЛ интенсивная, а не низкодозовая терапия селективными β-адреноблокаторами была ассоциирована со снижением 30-дневной смертности (относительный риск 0,26 при 95% доверительном интервале от 0,10 до 0,66) у пациентов с ХОБЛ, перенесших крупное кардиоваскулярное хирургическое вмешательство. Эти данные согласуются с результатами других исследований, показавших положительное влияние β-адреноблокаторов у пациентов с ХОБЛ, перенесших инфаркт миокарда [39, 48].
Следует отметить, что селективные β-адреноблокаторы в меньшей степени повышают периферическое сосудистое сопротивление, поэтому их можно шире использовать у пациентов с нарушениями периферического кровообращения (например, у больных с перемежающейся хромотой) [49].
Помимо кардиоселективности β-адреноблокаторы различаются по наличию дополнительных свойств, а также по продолжительности действия [49].
Бисопролол удачно сочетает достоинства жиро- и водорастворимых β-адреноблокаторов: высокую эффективность, длительный период полувыведения и небольшое число побочных эффектов. Бисопролол выводится двумя путями, что позволяет назначать его при нарушениях функции как печени, так и почек. Высокая кардиоселективность бисопролола (более чем в 3 раза превосходящая таковую метопролола сукцината) обеспечивает безопасность применения препарата даже у пациентов с ХОБЛ [50—56].
К базисной терапии ХОБЛ относят бронходилататоры (β2-агонисты, антихолинергические препараты являются более предпочтительными, чем производные метилксантинов), глюкокортикостероиды и ингибиторы 4-фосфодиэстеразы [1].
Несмотря на отсутствие крупных рандомизированных исследований по ведению больных с ХОБЛ и нестабильной стенокардией, представляется разумным избегать высоких доз β2-агонистов [1]. В то же время имеются данные о незначительном увеличении частоты развития сердечно-сосудистых осложнений при постоянном приеме м-холинолитика ипратропия бромида [57—58]. Полученные результаты по применению антихолинергических препаратов требуют проведения дополнительных исследований.
СН. Часто сочетается с ХОБЛ. Примерно у 30% пациентов с ХОБЛ имеется СН различной степени тяжести [59—60]. Декомпенсация СН является важной для дифференциальной диагностики обострения ХОБЛ. Сопутствующая ХОБЛ часто является причиной госпитализации по поводу острой СН [61], при этом значимо ухудшается прогноз, так как объем форсированного выдоха за 1-ю секунду (ОФВ1) служит сильным предиктором смерти при СН [62]. Необходимо проводить тщательную дифференциальную диагностику у больных с СН, ХОБЛ и бронхиальной астмой из-за наличия общего симптома — одышки.
Лечение СН у пациентов с ХОБЛ должно проводиться в соответствии с национальными и международными рекомендациями [63—65], так как нет доказательств того, что при наличии ХОБЛ медикаментозная терапия требует коррекции. Лечение с помощью кардиоселективных β-адреноблокаторов оказывает существенное положительное влияние на выживаемость больных с СН и наличие ХОБЛ является наиболее значимой причиной для пациентов, не получающих β-адреноблокаторы в достаточных дозировках [66]. Однако лечение кардиоселективными β-адреноблокаторами считается безопасным для пациентов с СН, страдающих ХОБЛ [67].
Наибольшую доказательную базу среди всех кардиоселективных β-адреноблокаторов имеет бисопролол. Исследования показали, что лечение бисопрололом при СН с сопутствующей ХОБЛ приводит к незначительному снижению ОФВ1, но без вредного воздействия на симптомы и качество жизни [68] и что кардиоселективные β-адреноблокаторы действительно предпочтительнее, чем неселективные β-адреноблокаторы, при сочетании СН с ХОБЛ [69]. Преимущества кардиоселективных β-адреноблокаторов при СН явно превышают любые потенциальные риски, связанные с лечением даже у пациентов с тяжелой ХОБЛ [1].
Терапия ХОБЛ не требует коррекции при наличии СН [1]. Это утверждение основано на результатах крупных проспективных исследований среди пациентов с СН и сопутствующей ХОБЛ [70—72]. Однако закрытое рандомизированное исследование показало повышенный риск смерти и госпитализаций у лиц с СН, получавших ингаляционные β2-агонисты [73]. Полученные результаты указывают на необходимость тщательного наблюдения за пациентами с тяжелой СН, которые применяют для лечения ХОБЛ ингаляционные β2-агонисты. У этой когорты больных предпочтительнее использование антихолинергических препаратов [56].
ФП. Наиболее частое нарушение ритма сердца. У пациентов с ХОБЛ заболеваемость ФП выше, чем у лиц без ХОБЛ [74—75]. Сочетание ХОБЛ с ФП представляет серьезную проблему для врачей из-за наличия удушья и потери трудоспособности [1]. При лечении ФП у пациентов с ХОБЛ необходимо руководствоваться общими принципами ведения больных с ФП [76—78], так как не доказано, что пациенты с ХОБЛ нуждаются в особом подходе к терапии [1]. Если есть потребность в использовании β-адреноблокаторов, то предпочтение следует отдавать кардиоселективным препаратам [1].
Принципы терапии ХОБЛ должны сохраняться при ведении больных с ФП. Однако нет достоверных данных об использовании препаратов для лечения ХОБЛ у пациентов с ФП, в связи с чем эта когорта пациентов часто исключалась из клинических испытаний. На наш взгляд, следует проявлять осторожность при использовании β2-агонистов, так как их прием может затруднить надлежащий контроль частоты сердечных сокращений. Не следует назначать метилксантины с учетом риска возникновения и предсердных, и желудочковых аритмий, в том числе фатальных [79].
АГ. Наиболее часто встречающееся сопутствующее заболевание у лиц ХОБЛ. Она значимо ухудшает прогноз у больных с ХОБЛ [26]. Распространенность АГ у пациентов с ХОБЛ варьирует от 6,8 до 76,3%, составляя в среднем 35% [29]. АГ и ХОБЛ сближают различные ассоциированные факторы, играющие важную роль в течении и прогрессировании каждого из этих двух заболеваний [28]. Так, к общим факторам прогрессирования АГ и ХОБЛ относят курение, избыточную массу тела, низкую физическую активность, вторичный эритроцитоз, вторичный гиперальдостеронизм, обструктивное апноэ во сне, легочную гипертонию, гипертензивный эффект некоторых лекарственных препаратов при лечении ХОБЛ (глюкокортикоиды, β2-адреномиметики).
С учетом данных об общих ФР прогрессирования, а также патогенеза развития АГ и ХОБЛ разработаны рекомендации по лечению больных с ХОБЛ в сочетании с АГ, которые включают следующее:
• Коррекцию ФР, общих для ХОБЛ и АГ (курение, избыточная масса тела, низкая физическая активность).
• Своевременное купирование обострений ХОБЛ (бронхиальная обструкция, гипоксемия, легочная гипертония, эритроцитоз).
• Выбор гипотензивного препарата с учетом клинической ситуации (наличие хронического легочного сердца, сопутствующей ИБС, нарушений ритма, СН, сахарного диабета, хронической почечной недостаточности и др.).
• Коррекцию гипотензивной терапии в случае ее неэффективности (доза препарата, замена препарата, комбинация различных гипотензивных препаратов).
Проводя терапию АГ у пациентов с ХОБЛ, необходимо учитывать особенности лечения ХОБЛ на фоне антигипертензивной терапии. Как правило, антибиотики, муколитические и отхаркивающие препараты, назначаемые больным с ХОБЛ, не влияют на лечение АГ и эффективность гипотензивной терапии. В то же время ингаляции β-адреномиметиков в больших дозах способны вызвать у больных АГ тахикардию и спровоцировать повышение артериального давления (АД) вплоть до гипертонического криза. Ингибитор фосфодиэстеразы аминофиллин и теофиллиновые производные, обладающие бронхолитическими свойствами, способны вызвать тахикардию, однако повышение АД на этом фоне обычно кратковременное и редко приводит к существенной дестабилизации состояния. Ингаляции стероидных средств обычно не влияют на уровень АД. В тех случаях, когда требуется длительный прием глюкокортикостероидов, вероятны задержка натрия, жидкости, увеличение массы тела и стабильное повышение АД.
Выбор антигипертензивного средства для лечения АГ в сочетании с ХОБЛ регламентирован российскими и международными рекомендациями по профилактике, диагностике и лечению АГ [80—84].
β-Адреноблокаторы по-прежнему рекомендуют рассматривать как препараты первого ряда для лечения АГ у больных сте нокардией напряжения, перенесших инфаркт миокарда с признаками СН, тахиаритмиями, глаукомой (это новое показа ние, отсутствующее для других групп антигипертензивных средств), а также у беременных женщин.
Современные селективные β-адреноблокаторы (бисопролол, небиволол) в крупных контролируемых рандомизированных исследованиях не при менялись. В небольших и кратковременных исследованиях высокоселективный β-адреноблокатор бисопролол зарекомендовал себя у больных АГ с наилучшей стороны [85]. Кардиоселективные β-адреноблокаторы следует назначать больным ХОБЛ с АГ в малых дозах под контролем электрокардиограммы и бронхиальной проходимости. Для измерения степени ограничения скорости воздушного потока всем больным с ХОБЛ рекомендовано исследование функции внешнего дыхания (ФВД) с применением метода спирометрии, так как он является наиболее доступным и воспроизводимым тестом функции легких [1]. При появлении клинических симптомов ухудшения бронхиальной проходимости и неблагоприятном влиянии на показатели ФВД дозировку β-адреноблокаторов следует уменьшить, а при сохранении снижения ФВД их необходимо отменить.
Считается, что кардиоселективные β-адреноблокаторы оптимальны по их влиянию на ФВД [56]. Доказательная база данных по ряду исследований отдает предпочтение бисопрололу.
Каковы же преимущества высокоселективных β-адреноблокаторов перед другими группами антигипертензивных препаратов первого ряда?
Во-первых, кардиоселективные β-адреноблокаторы не влияют на клиренс мокроты, в то время как диуретики могут ухудшать течение ХОБЛ за счет сгущения мокроты и затруднения ее отхождения.
Во-вторых, кардиоселективные β-адреноблокаторы не оказывают прокашлевое действие. Следует помнить, что одним из побочных эффектов ингибиторов ангиотензинпревращающего фермента является сухой кашель (до 10% случаев) за счет накопления брадикинина, вещества Р и увеличения продукции оксида азота в дыхательных путях, что также может стимулировать кашлевой рефлекс и бронхоспазм у больного ХОБЛ [45].
Заключение
В настоящее время из кардиоселективных β-адреноблокаторов целесообразно использовать бисопролол, метопролола сукцинат, карведилол и небиволол для лечения больных с сердечно-сосудистыми заболеваниями (ССЗ) в сочетании с хронической обструктивной болезнью легких (ХОБЛ).
Из всех кардиоселективных β-адреноблокаторов наибольшую доказательную базу данных по эффективности и безопасности применения у больных с ХОБЛ и ССЗ имеет бисопролол.
При использовании кардиоселективных β-адреноблокаторов целесообразно контролировать функцию внешнего дыхания. В случае появления клинических симптомов ухудшения бронхиальной проходимости и неблагоприятном влиянии на показатели функции внешнего дыхания дозировку β-адреноблокаторов следует уменьшить, а при сохранении снижения функции внешнего дыхания их необходимо отменить. В целом применение кардиоселективных β-адреноблокаторов у больных с ССЗ в сочетании с ХОБЛ является безопасным, и польза от приема этой группы препаратов превышает возможные риски обострения ХОБЛ.
При терапии ХОБЛ применение β₂-агонистов по возможности нужно ограничить с учетом их негативного влияния на состояние сердечно-сосудистой системы у больных с ССЗ, предпочтительнее использование антихолинергических средств.



