Основными целями лечения и вторичной профилактики сердечно-сосудистых заболеваний (ССЗ), в частности ишемической болезни сердца (ИБС), являются снижение числа осложнений и смертности, продление жизни пациентов и повышение ее качества. В последние годы в нашей стране в отношении ССЗ достигнуты определенные успехи.
Так, начиная с 2003 г. в России наметилось снижение смертности от ССЗ, которое стало устойчивым с 2006 г. [1—3].
С 2003 по 2013 г. число умерших от ССЗ на 100 тыс. населения сократилось в России на 25% (с 927,5 до 698,1). Тем не менее ситуация продолжает оставаться хуже, чем в других европейских странах [4]. При этом ССЗ занимают в нашей стране в структуре смертности бóльшую долю, чем в среднем по Европе (55,7% против 46% [5]), причем 29,4% всех смертей приходится на ИБС. Эти цифры свидетельствуют о необходимости дальнейшего совершенствования оказания медицинской помощи пациентам с ССЗ, в частности с ИБС.
Важной составляющей оптимизации лечения и вторичной профилактики ИБС являются разработка и внедрение клинических рекомендаций, основанных на принципах доказательной медицины, а также получение обратной связи о степени их соблюдения, что позволяет выбрать тактику последующей работы со всеми участниками процесса лечения больного — врачами, пациентами, организаторами здравоохранения. С этой целью проводятся регистры и мониторинговые исследования, которые реализуются как на национальном, так и на международном уровнях.
Так, рутинная практика лечения пациентов с ИБС оценивалась в ряде российских исследований, таких как Российский регистр острых коронарных синдромов — ОКС (2000—2001) [6, 7], РЕЛИФ (2006) [8], Регистр ОКС РЕКОРД (2007—2008) [9, 10].
По сравнению с национальными исследованиями участие страны в международных проектах, объединенных единой методологией и проводимых в один и тот же временной период, обладает значительными преимуществами, поскольку дает возможность корректного сравнения ситуации в стране с картиной в целом по Европе и в других европейских странах. В начале 2000-х гг. участие России в международных исследованиях по мониторингу вторичной профилактики ИБС ограничилось относительно небольшим исследованием Angina Treatment Patterns (ATP) Survey (2001—2002 гг., 7074 пациента, 7 стран-участниц) [11, 12]. В связи с этим для нашей страны стало очень важно присоединиться к крупнейшему проекту Европейского общества кардиологов по мониторингу вторичной профилактики ИБС в европейских странах — исследованию EUROASPIRE (EUROpean Action on Secondary Prevention through Intervention to Reduce Еvents). В настоящее время проведено четыре этапа исследования: в 1995—1996 гг. EUROASPIRE I с участием 9 европейских стран и 3569 пациентов с ИБС [13], в 2000—2001 гг. EUROASPIRE II с участием 15 европейских стран и 5556 пациентов [14], в 2006—2007 гг. EUROASPIRE III с участием 22 европейских стран и 13 593 пациентов [15] и, наконец в 2013 г. EUROASPIRE IV с участием 24 европейских стран и 13 586 пациентов [16]. В рамках исследования EUROASPIRE IV впервые проведен проспективный этап исследования (выяснение жизненного статуса пациентов ИБС через 1 год после включения в исследование); кроме того, впервые осуществлен дополнительный скрининг с целью выявления сахарного диабета по данным теста на толерантность к глюкозе. Россия принимала участие в последних двух исследованиях (EUROASPIRE III и EUROASPIRE IV), что дает возможность проведения сравнительной оценки как с Европой в целом и другими европейскими странами, так и оценки динамики ситуации за прошедшие годы у нас в стране.
 В настоящей статье представлены данные по наличию и уровню основных факторов риска (ФР) развития ССЗ и достижению целевых показателей вторичной профилактики ИБС. В последующих публикациях будут представлены данные по медикаментозной терапии, проводившейся на этапах стационарного лечения и выписки пациентов из стационара, а также приверженности рекомендованному лечению, по данным визита-интервью при включении пациентов в исследование EUROASPIRE IV. Третью часть статьи планируется посвятить психосоциальным факторам ССЗ и результатам оценки качества жизни (КЖ) больных.
В настоящей статье представлены данные по наличию и уровню основных факторов риска (ФР) развития ССЗ и достижению целевых показателей вторичной профилактики ИБС. В последующих публикациях будут представлены данные по медикаментозной терапии, проводившейся на этапах стационарного лечения и выписки пациентов из стационара, а также приверженности рекомендованному лечению, по данным визита-интервью при включении пациентов в исследование EUROASPIRE IV. Третью часть статьи планируется посвятить психосоциальным факторам ССЗ и результатам оценки качества жизни (КЖ) больных.
Материал и методы
По дизайну исследование EUROASPIRE IV представляет собой поперечное исследование, в котором принимали участие 24 страны Европы: Бельгия, Болгария, Босния и Герцеговина, Великобритания, Германия, Греция, Ирландия, Испания, Кипр, Латвия, Литва, Нидерланды, Польша, Россия, Румыния, Сербия, Словения, Турция, Украина, Финляндия, Франция, Хорватия, Швеция. В каждой из стран выбирали одну или несколько географических областей и идентифицировали центры (больницы) кардиологического профиля, из которых выбирали один или несколько центров таким образом, чтобы пациенты из данной географической области с ОКС или показаниями к реваскуляризации миокарда с помощью аортокоронарного шунтирования (АКШ) или чрескожных коронарных вмешательств (ЧКВ) имели шансы на госпитализацию.
В центрах — участниках исследования, по данным повседневно ведущихся регистров или выписных эпикризов идентифицировались все без исключения последовательно поступавшие пациенты (в возрасте от 18 до 80 лет), госпитализированные по поводу острого инфаркта миокарда (ОИМ) с подъемом/без подъема сегмента ST или ОКС без формирования инфаркта миокарда (с отрицательным результатом анализа на тропонин), или планового/экстренного ЧКВ — баллонной ангиопластики/стентирования коронарных артерий, или плановой/экстренной операции АКШ в период от 6 мес до 3 лет перед включением в исследование. Каждой из стран-участниц рекомендовалось включить в исследование не менее 400 пациентов, пришедших в центры для включения в исследование. Критериями исключения служили тяжелые острые состояния, хронические заболевания в стадии декомпенсации, тяжелые психические расстройства, наркотическая или алкогольная зависимость, отказ пациента от участия в исследовании. Все идентифицированные по медицинским документам пациенты ИБС приглашались на визит-интервью с целью оценки отдаленных результатов лечения, наличия и уровней ФР, клинического, психологического статуса и показателей КЖ, а также оценки адекватности предоставленных пациентам рекомендаций по немедикаментозным вмешательствам и медикаментозному лечению. Каждый пациент подписывал информированное согласие на участие в исследовании.
При анализе медицинской документации (данных электронных регистров или историй болезни) учитывались социально-демографические характеристики пациентов; данные анамнеза; наличие информации по ФР; назначенная при госпитализации и выписке терапия (с названиями препаратов и их суточными дозами), а также записи о предоставленных пациентам рекомендациях по изменению образа жизни.
Во время визита-интервью с помощью структурированной регистрационной карты проводился детальный опрос пациентов по основным аспектам образа жизни (курение, питание, физическая активность, психосоциальные факторы), приему препаратов и соблюдению рекомендаций по немедикаментозным вмешательствам. Регистрировались антропометрические данные: рост и масса тела в легкой одежде и без обуви, окружность талии — ОТ (на середине расстояния между нижним краем реберной дуги и гребнем подвздошной кости по средней подмышечной линии в положении пациента стоя). Артериальное давление (АД) измерялось дважды после 5-минутного отдыха на правом плече с 5-минутным интервалом в положении больного сидя с использованием автоматического цифрового сфигмоманометра Omron M6.Факт курения объективизировался по концентрации монооксида углерода в выдыхаемом воздухе с помощью прибора Smokerlyser. Уровень физической активности пациентов оценивался с помощью Международного опросника физической активности (IPAQ — International Physical Activity Questionnaire) и Опросника физической активности во внерабочее время Година. Психологический статус пациентов изучали по данным Госпитальной шкалы тревоги и депрессии (HADS — Hospital Anxiety and Depression Scale), показатели КЖ — с помощью опросника HeartQol. Все перечисленные данные вносились в единую для всех стран бумажную регистрационную карту пациента, а также в электронную карту пациента в системе EUR Observational Research Program Европейского общества кардиологов.
Во время визита-интервью производился забор образцов венозной крови натощак для определения уровней общего холестерина, холестерина липопротеидов высокой плотности (ЛВП), триглицеридов, холестерина липопротеидов низкой плотности (ЛНП) (с расчетом по формуле Фридвальда), а также уровня глюкозы в крови и гликированного гемоглобина (HbA1c). Всем пациентам без сахарного диабета (СД) и в отсутствие уровня глюкозы в крови натощак ≥11,1 ммоль/л проводился пероральный тест на толерантность к глюкозе с 75 глюкозы в 200 мл воды после не менее чем 10-часового голодания.
Кровь для определения уровня холестерина и его фракций забирали в пробирку, содержащую активатор сгустка, для определения уровня HbA1с – ЭДТА (Venosafe). Кровь центрифугировали (2000 об/мин) при комнатной температуре в течение 10 мин, после чего плазму помещали в кодированные пробирки, замораживали в холодильной камере при температуре -70 °C и отправляли из всех стран-участниц исследования в единую лабораторию Disease Risk Unit, National Public Health Institute, где проводились измерения надлежащих показателей на биохимическом анализаторе Architect c8000.
Статистический анализ данных настоящего исследования проводился на кафедре Общественного здравоохранения Гентского Университета (Бельгия) с помощью версии 9.3 пакета прикладных статистических программ SAS (Statistical Analysis System, SAS Institute Inc., США) с применением стандартных алгоритмов вариационной статистики.
В России в исследовании EUROASPIRE IV участвовали 3 центра — ФГБУ ГНИЦ профилактической медицины Минздрава России (Москва), городская больница №36 ДЗМ (Москва) и Московский областной кардиологический центр (г. Жуковский), Российская часть исследования EUROASPIRE IV проведена под эгидой Национального медицинского общества профилактической кардиологии и при поддержке исследовательского гранта, предоставленного компанией Фармстандарт.
Результаты и обсуждение
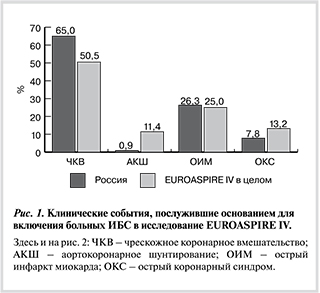
Всего в российских центрах были включены в исследование 746 пациентов с ИБС, средний возраст которых на момент клинического события составил 62,2±9,5 года, доля женщин 29,5% (в целом по Европе 13 586 пациентов; средний возраст 62,7±10,0 года; женщин 26,2%). При этом 10,7% включенных в России пациентов были в возрасте моложе 50 лет, 28,8% — 50—59 лет, 34,4% — 60—69 лет и 26% — 70 лет и старше. У большинства наших пациентов клиническим событием, послужившим основанием для включения в исследование, было ЧКВ, в каждом четвертом случае — ОИМ (рис. 1).
 Большинство российских пациентов еще до клинического события и связанной с ним госпитализации имели серьезный анамнез ИБС: 42,1% ранее перенесли ОИМ, 5% — ОКС, 21,9% — ЧКВ и 4% — АКШ. В общей популяции исследования эти события отмечались гораздо реже (23,6%, 6,1, 19,5 и 6,2% соответственно).
Большинство российских пациентов еще до клинического события и связанной с ним госпитализации имели серьезный анамнез ИБС: 42,1% ранее перенесли ОИМ, 5% — ОКС, 21,9% — ЧКВ и 4% — АКШ. В общей популяции исследования эти события отмечались гораздо реже (23,6%, 6,1, 19,5 и 6,2% соответственно).
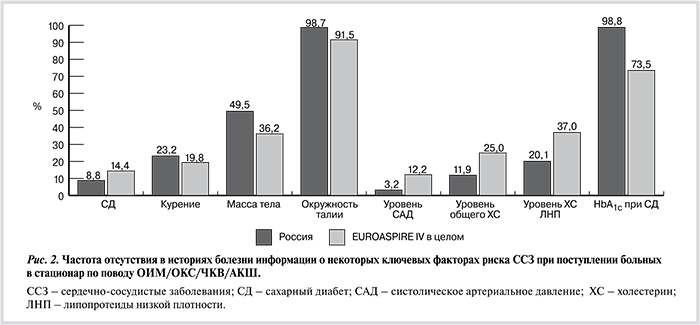
При анализе записей в историях болезни при поступлении как у российских пациентов, так и в общей популяции исследования были выявлены существенные пробелы в регистрации ФР развития ССЗ (рис. 2). Так, у абсолютного большинства пациентов отсутствовала информация об ОТ, более чем у 1/3 — информация о массе тела, у каждого пятого — информация о статусе курения. У нас реже вносилась в истории болезни информация об уровне HbA1c у пациентов с СД, курении, массе тела и ОТ, при этом было меньше недостатков в регистрации уровня систолического АД, липидов крови и СД, чем в Европе в целом.
В выписных эпикризах российских пациентов не было информации о курении в 18,4% случаев, об ожирении — в 18,9%, об артериальной гипертонии (АГ) — в 4,2%, о дислипидемии — в 16,6%, о нарушениях метаболизма глюкозы — в 8,2%. В общей популяции исследования показатели были несколько хуже: записи отсутствовали соответственно в 26%, 38, 12,8, 19,4 и 19,7% случаев.
На визит-интервью в российские центры пришли 424 пациента (56,8% пациентов, идентифицированных по медицинским документам и включенных в исследование), среди них 25,2% женщин. В общей популяции исследования явка была несколько ниже — 48,7% (24,4% женщин). Средний возраст наших пациентов, пришедших на интервью, составил 63,4±9,0 лет (5,9% моложе 50 лет, 30,4% — 50—59 лет, 37,7% — 60—69 лет, 25,9% — 70 лет и старше), в общей популяции — 64,0±9,6 года.
Визит-интервью состоялся в российских центрах в среднем через 1,33 (1,0—2,39) года после исходной госпитализации, в общей популяции – через 1,35 (0,95—1,93) года. За период между индексной госпитализацией и визитом-интервью 6,4% наших пациентов перенесли кардиальные осложнения (4% — ОИМ и 2,4% — ОКС), 13,7% пациентов — ЧКВ, а 3,1% — операцию АКШ. Обращает на себя внимание большое число госпитализаций среди российских пациентов: по поводу стенокардии — 24,6%, сердечной недостаточности — 3,6%, атеросклероза периферических артерий — 1,9%, инсульта — 1,2%. В общей популяции исследования госпитализаций по всем перечисленным причинам было существенно меньше, особенно заметным это различие было в отношении стенокардии (стенокардия — 5,4%, сердечная недостаточность — 2,1%, ОИМ — 2%, ОКС — 1,7%, периферический атеросклероз — 1,1%, инсульт — 0,7%). Следует отметить, что 1% российских пациентов стояли в очереди на плановую операцию АКШ, а 2,3% — на ЧКВ (в общей популяции практически столько же — 0,9 и 2% соответственно). И в общей популяции исследования, и у нас 70% пациентов с ИБС, пришедших на визит-интервью, находились после индексной госпитализации под наблюдением кардиолога (73 и 72,9% соответственно).
Образовательный уровень российской когорты оказался в целом выше, чем в общей популяции исследования: высшее образование имели 44,3%, среднее специальное — 37,5%; среднее — 15,5% и неоконченное среднее — 2,7% пациентов (в целом — 22,3%, 19,7, 40,5 и 17,4% соответственно).
При анализе данных, полученных на отдаленном этапе после клинических событий в российских центрах и в Европе в целом, было обнаружено значительное поле для совершенствования мероприятий по коррекции ФР развития ССЗ.
Несмотря на ранее перенесенные осложнения ИБС и вмешательства по реваскуляризации миокарда, во время визита-интервью сообщили о факте курения 27,9% пациентов-мужчин и 5,6% женщин (22,2% российских пациентов — мужчин и женщин). В общей популяции исследования курящих было в целом меньше (15%), при этом мужчины курили реже (16,6%), а женщины почти в 2 раза чаще (10,2%). Эти данные были подтверждены результатами исследования монооксида углерода в выдыхаемом воздухе. По частоте курения среди пациентов с ИБС мы находились на четвертом месте после Кипра (27,8%), Франции (24,4%) и Турции (21,8%), а реже всего курили пациенты с ИБС из Бельгии (7,3%) и Финляндии (6,7%).
Эффективность проводившихся мероприятий по борьбе с курением у российских пациентов была очень невысокой. Из тех, кто курил в течение 1 мес перед исходным клиническим событием, послужившим основанием для госпитализации, продолжали курить на момент визита-интервью (подтверждение пациента или уровень монооксида углерода в выдыхаемом воздухе >10 ppm) 64,5% больных (65,4% мужчин и 54,5% женщин). В общей популяции исследования отказавшихся от курения было заметно больше: продолжали курить 48,6% пациентов (49,3% мужчин и 45,4% женщин). Реже, чем у нас в стране, отказывались от курения после исходной госпитализации только во Франции — там продолжали курить 70,7% пациентов; напротив, наиболее успешно отказ от курения проходил у испанских участников: там не отказались от курения только 27% ранее куривших пациентов.
Мотивация российских пациентов к отказу от курения в будущем примерно соответствовала среднеевропейскому уровню: о наличии намерения отказаться от этой привычки в ближайшие 6 мес в России сообщили 55,4% пациентов, в общей популяции исследования — 50,9%; статистически значимых различий между мужчинами и женщинами по этому показателю не было. По количеству желающих отказаться от курения в Европе лидировала Румыния (71%), самым низким этот показатель был в Словении (13%). Однако в целом в отношении намерения отказаться от курения пациенты разделились примерно поровну: 50% готовы к отказу от курения, другие 50% — нет.
Анализ конкретных мероприятий по борьбе с курением показал, что в российских центрах 81,9% курильщиков (по их словам) получили от врача устный совет отказаться от курения, у 51,6% этот совет был даже зафиксирован письменно, однако лишь 1 (1,1%) пациент получил конкретное направление на участие в специализированной программе помощи по отказу от курения. В общей популяции исследования 88,5% пациентов также получили устные рекомендации, даже несколько меньшее число пациентов (42,6%) сообщили, что совет был дан в письменной форме, однако специализированная помощь предлагалась существенно чаще (18,6% пациентов). Мы также значительно отставали от остальных стран по частоте назначения медикаментозной терапии по отказу от курения: препараты никотинзаместительной терапии (НЗТ) были назначены только 3 (3,2%) пациентам, варениклин не был рекомендован ни одному из пациентов. При этом в европейских странах совет принимать НЗТ получили 22,9% курящих, варениклин был рекомендован 6,2%, и еще 4,7% курильщикам был назначен незарегистрированный в России бупропион.
Из куривших на момент интервью наших пациентов 22,1% сообщили, что после исходного клинического события они пытались полностью отказаться от курения, 35,3% пациентов пытались сократить число выкуриваемых сигарет и 7 (8,1%) пациентов самостоятельно обратились к специалистам по отказу от курения. В общей популяции исследования соответствующие цифры составляли 10,7%, 66,7 и 7,2%. Несмотря на низкую частоту медикаментозных рекомендаций от врачей по отказу от курения, лишь 4,7% наших пациентов самостоятельно принимали НЗТ и 4,7% — варениклин. В общей популяции исследования частота фармакотерапии никотиновой зависимости оказалась в среднем недостаточной (НЗТ — 14,4%, бупропион — 1,7% и варениклин — 3,1%), при этом отмечались существенные различия между странами. Так, варениклин получал каждый четвертый (25%) курильщик в Бельгии, 17,8% — в Швеции и 15,8% — в Испании. НЗТ чаще всего использовалась пациентами в Ирландии (51,6%), Германии (35,4%), Швеции (32,6%), Франции (31,5%) и Великобритании (26,5%).
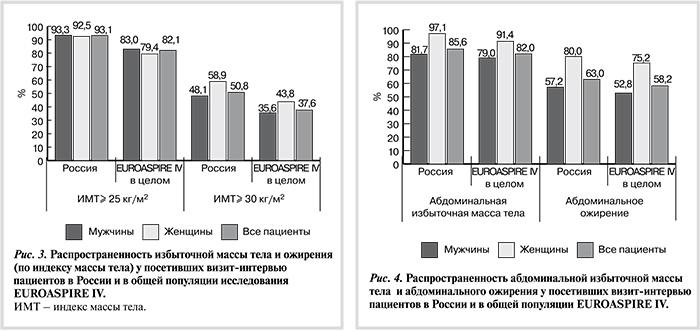
В России было существенно больше пациентов с избыточной массой тела и ожирением, чем в общей популяции исследования, особенно это касалось женщин (рис. 3). Средний индекс массы тела (ИМТ) у пациентов российской когорты составил 30,6±4,8 кг/м2 (30,1±4,4 кг/м2 у мужчин и 32,2±5,4 кг/м2 у женщин), а в общей популяции исследования — 29,1±4,7 кг/м2 (28,9±4,3 кг/м2 у мужчин и 29,6±5,5 кг/м2 у женщин). Надлежащую массу тела имели менее 10% наших пациентов, в Европе в целом таких больных было в 2,5 раза больше. По числу пациентов с ИБС с избыточной массой тела (ИМТ≥25 кг/м2) мы оказались на первом месте в Европе, второе место разделили Словения и Ирландия (по 88%), далее Чехия (85,5%), Кипр и Германия (85%). Самыми стройными оказались пациенты из Франции, Швеции и Сербии — в этих странах каждый четвертый пациент (24%) имел надлежащую массу тела. При анализе распространенности ожирения (ИМТ≥30 кг/м2) наблюдалась сходная картина: лидировали наши пациенты (50,8%), далее Словения (49,4%) и Румыния (46%), а меньше всего таких пациентов было в Сербии (25,8%).
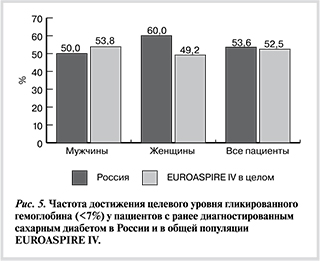
Поскольку копятся доказательства того, что региональное распределение жировой ткани имеет большее значение для риска развития ССЗ, чем общая масса тела, представляет особый интерес анализ показателей ОТ, по которым наши пациенты не так сильно отличались от общей популяции исследования (усредненные показатели окружности талии 102,2±11,9 и 101,4±12,7 см соответственно). По распространенности среди пациентов ИБС абдоминального ожирения (ОТ≥102 см у мужчин и ≥84 см у женщин) лидировали Кипр (73%), Румыния (72%), Словения (71,5%), Чехия (69,1%), и на пятой позиции Россия (63%). Важно отметить, что и в России, и в других европейских странах абдоминальное ожирение было в 1,2—2 раза более характерно для женщин (рис. 4).
Абсолютное большинство (93,9%) российских пациентов с ожирением сообщили, что с момента исходного клинического события врачи им указывали на то, что их масса тела избыточна. Это один из самых высоких показателей в Европе, чаще такую информацию от медицинских работников получали только пациенты из Испании (94,4%), для сравнения в Турции таких пациентов было всего 61,7%(среднеевропейский показатель — 80,6%).
При этом 77% российских пациентов с ожирением отметили, что врачи указывали им на нездоровый характер питания (63,5% в Европе в целом).
Каждый второй (50%) российский пациент с ИБС и ожирением в течение 1 мес до визита-интервью предпринимал попытки снизить массу тела (показатель примерно соответствовал среднеевропейскому уровню — 49,8%).
Снизить массу тела в ближайшие полгода планировали 67,5% наших пациентов с ожирением. Это чуть больше, чем в среднем по Европе (61,9%). Наиболее часто такие намерения высказывали пациенты из Словении (86%), реже всего — жители Финляндии (25%).
Таким образом, обращает на себя внимание высокая распространенность нарушений жирового обмена в общей популяции исследования и особенно среди российских пациентов, при этом в большинстве случаев пациенты были информированы врачами о наличии у них избыточной массы тела/ожирения и имели достаточно высокий уровень мотивации к снижению массы тела. Отсутствие действенных результатов по снижению массы тела, очевидно, обусловлено, с одной стороны, низкой доступностью диетологического консультирования, а с другой, объективными трудностями коррекции массы тела при ожирении [17].
Каждый пятый (20,1%) российский пациент знал о наличии у него СД, диагностированного ранее (в том числе 17,4% мужчин и 28,3% женщин). Это несколько меньше, чем в Европе в целом, где СД был ранее диагностирован у 26,8% пациентов (25,7% мужчин и 30,1% женщин). Больше всего пациентов с известным анамнезом СД было в Греции (41,5%), меньше всего — в Ирландии (15,1%).
Из российских пациентов с СД 69% сообщили, что придерживаются диеты и/или мероприятий по коррекции образа жизни, 76,2% получали пероральные сахароснижающие средства, 14,3% — инсулин. В целом в европейских странах было существенно больше (31,9%) пациентов, получавших инсулин, при этом диету соблюдали 66,2%, а пероральные сахароснижающие препараты — 72,5% пациентов.
У 23,4% наших пациентов с ранее диагностированным СД имелись диабетическая ретинопатия, у 12,2% — нефропатия, 36,3% — невропатия, в общей популяции исследования частота этих осложнений была несколько ниже и составляла 7,9%, 8,8 и 14,8% соответственно.
Самоконтроль гликемии проводили 88,1% наших пациентов с ИБС и диагностированным СД, причем женщины несколько чаще мужчин (93,3% против 88,1%); в общей популяции исследования самоконтролю гликемии были привержены 73,6% пациентов с СД без существенных различий по полу. Очевидно, бо'льшая приверженность самоконтролю гликемии обусловила несколько более низкие средние уровни в крови глюкозы и HbA1c у российских пациентов. Усредненный уровень глюкозы в российской когорте составил 8,37±3,03 ммоль/л (и у мужчин, и у женщин 8,78±3,08), а в общей популяции исследования — 8,51±2,80 ммоль/л, также без существенных различий по полу.
Средний уровень HbA1c у российских пациентов с СД 7,08±1,29% (7,07±1,25% и у мужчин, и у женщин), в Европе в целом 7,20±1,41% также без различий между мужчинами и женщинами. Тем не менее число пациентов с целевым уровнем HbA1c (<7%) в российских центрах и в общей популяции исследования было примерно одинаковым (рис. 5), при этом несколько лучшие показатели компенсации по сравнению со среднеевропейскими отмечались только у российских женщин. Наиболее высокой частота компенсации СД по критерию HbA1c была в Финляндии (72%), наиболее низкой — в Турции (27%).
При обследовании, проведенном во время визита-интервью, СД (гликемия натощак ≥7 ммоль/л) был впервые выявлен у 6,7% российских пациентов (6,2% мужчин и 8,3% женщин); в общей популяции таких случаев было почти в 2 раза больше — 12,9% (без статистически значимых различий между мужчинами и женщинами). Диагностический для СД уровень HbA1c (≥6,5%) был установлен у 4% наших пациентов, ранее не подозревавших наличия у себя СД; в общей популяции исследования такие находки встречались чуть чаще: у 5,6% участников (6,0% мужчин и 4,2% женщин). Пероральный тест на толерантность к глюкозе проводился у пациентов без СД в анамнезе и уровня глюкозы в крови натощак ≥11,1 ммоль/л. В российских центрах исследование было проведено у 80,4% пациентов с такими характеристиками, в Европе в целом — у 78,8%, в обоих случаях без значимых различий частоты его выполнения у мужчин и у женщин. На основании проведенного теста у 8% наших пациентов был впервые диагностирован СД, у 12,4% — нарушенная гликемия натощак, у 20,3% — нарушение толерантности к углеводам. В общей популяции исследования эти состояния были обнаружены в 17,%, 14,1 и 21,8% случаев соответственно.
Таким образом, у 1/3 российских пациентов ИБС имелся СД: у 20,1% был диагностирован ранее и у 8% выявлен во время визита-интервью при включении в исследование EUROASPIRE IV по данным теста на толерантность к глюкозе.
Средний уровень систолического артериального давления (САД) составил у российских пациентов 127,4±17,9 мм рт.ст. (128,1±18,3 у мужчин и 127,0±17,1 у женщин), диастолического артериального давления (ДАД) — 76,3±11,7 мм рт.ст. (77,2±11,7 у мужчин и 73,9±11,5 у женщин).
В общей популяции исследования цифры были несколько выше: САД 134,4±19,1 мм рт.ст. (134,2±18,9 у мужчин и 135,0±19,6 мм рт.ст. у женщин), ДАД 78,9±11,1 мм рт.ст. (79,1±11,0 у мужчин, 78,4±11,2 мм рт.ст. у женщин).
Отсутствие контроля давления (САД≥140 мм рт.ст. и/или ДАД≥90 мм рт.ст.) на момент визита-интервью у российских участников отмечалось заметно реже, чем в общей популяции исследования EUROASPIRE IV (23,9% против 38,5%; у мужчин 25,1% против 38,2% и у женщин 20,6% против 39,5%). Меньшее число пациентов с неконтролируемой АГ было только в Греции (15,7%) и Ирландии (22,9%), а наиболее неблагоприятная картина в этом отношении зафиксирована в Литве (55,8%).
Антигипертензивные препараты, назначенные специально с целью коррекции АД, получали абсолютное большинство пациентов: 80,1% (80,3% мужчин и 95,3% женщин) в России и 78,1% (76,2% мужчин и 84,1% женщин) в общей популяции. Среди пациентов, которые в течение 2 нед до визита-интервью принимали лекарства для снижения АД, целевой уровень АД был достигнут у каждого второго пациента в общей популяции исследования (53,5%; 53,1% мужчин и 53,7% женщин) и 73,4% пациентов в российской когорте (71,8% мужчин и 77,2% женщин). Это был самый лучший показатель в Европе. Реже всего давление контролировалось у жителей Литвы (38,9%).
Кроме того, в российских центрах отмечалась значительно более благоприятная ситуация, чем в остальных странах в отношении частоты недиагностированной АГ. Среди пациентов без АГ в анамнезе при визите-интервью АД≥140/90 мм рт.ст. было выявлено лишь у 8,2% (8,7% мужчин, 0% женщин), в то время как в общей популяции исследования — у 26,5% (26,7% мужчин и 25,8% женщин).
В отличие от АД уровень липидов у наших пациентов был выше, чем в общей популяции исследования: общий холестерин (ХС) 4,91±1,45 ммоль/л (4,80±1,24 у мужчин и 5,23±1,92 у женщин) против 4,41±1,12 ммоль/л (4,32±1,06 у мужчин и 4,71±1,24 у женщин), ХС ЛНП 2,90±1,07 ммоль/л (2,87±1,04 у мужчин и 2,98±1,17 у женщин) против 2,51±0,92 (2,46±0,87 у мужчин и 2,69±1,03 у женщин).
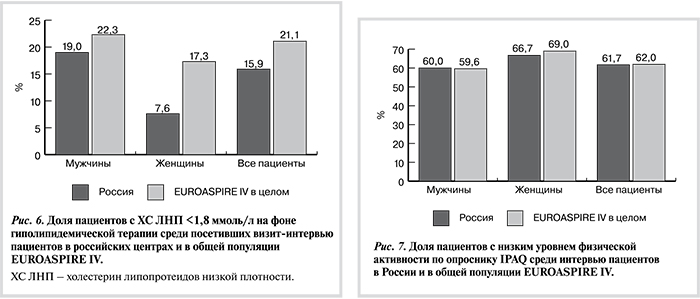
Доля российских пациентов с уровнем общего ХС≥4,0 ммоль/л составила 71,3% (69,3% мужчин и 77,4% женщин), в общей популяции исследования таких пациентов было заметно меньше — 59,8% (56,4% мужчин и 70,6% женщин). ХС ЛВП превышал целевой для пациентов ИБС уровень (≥1,8 ммоль/л) у 87,4% наших пациентов (85,6% мужчин и 92,9% женщин) и у 80,5% пациентов в Европе в целом (79,2% мужчин и 84,4% женщин). Гиполипидемические препараты получали 74,9% российских пациентов (73,1% мужчин и 80,2% женщин), в Европе в целом они назначались чаще — 86,6% (87,3% мужчин и 84,5% женщин). Частота достижения целевого уровня ХС ЛНПсреди получавших гиполипидемические препараты пациентов с ИБС (рис. 6) была очень низкой в общей популяции исследования и особенно в России. Возможно, причиной этого было относительно недавнее понижение целевого уровня ЛНП при ИБС (с <2,5 до <1,8 ммоль/л) [18]. Частота достижения этого жесткого целевого уровня была наиболее высокой в Испании (41%) и наиболее низкой — в Литве (5%).
Что касается физической активности, то 67,1% российских пациентов с ИБС в ходе визита-интервью охарактеризовали свою физическую активность вне работы как незначительную, 16,2% — как умеренную, 10,9% — как интенсивную и 5,8% — как никакую; в общей популяции исследования — 51,7%, 20,5, 19,5 и 8,2% соответственно.
По данным Опросника Година, уровень физической активности во внерабочее время у российских пациентов и в общей популяции исследования были сопоставимы: 21 (21—46) и 23 (15—45) МЕТ в неделю.
Рекомендованный ВОЗ уровень физической активности (>30 мин 5 раз и более в неделю) имели, по их словам, 67,8% российских пациентов (67,7% мужчин и 68,3% женщин) и 42,9% пациентов в европейских странах в целом (44,7% мужчин и 37,2% женщин). Наши пациенты, по-видимому, считали свою физическую активность достаточной и продемонстрировали низкую мотивацию к повышению физической активности. Так, 60,9% пациентов указали, что не занимаются и не хотят заниматься физической культурой, направленной на повышение тренированности (в общей популяции исследования таких ответов было только 41,5%).
По данным опросника IPAQ, уровень физической активности наших пациентов был выше, чем общей популяции: 3252 (1548—6158) против 2586 (1182—4572). Частота низкого уровня физической активности, по данным опросника IPAQ (рис. 7), у наших пациентов была примерно сопоставима со среднеевропейским уровнем. Больше всего пациентов с низким уровнем физической активности было в Турции (86,4%), а меньше всего в Германии (38,2%).
Обсуждая эти результаты, нельзя не отметить, что 2 из трех участвовавших в исследовании EUROASPIRE IV российских клинических центров представляли собой медицинские учреждения с высоким уровнем оказания медицинской помощи, и вполне вероятно, что в целом по стране частота достижения целевых уровней ФР будет ниже. Этот недостаток является общим для всей программы EUROASPIRE [14], где в каждой из стран как минимум одним из участвовавших в исследовании клинических центров была университетская клиника. В связи с этим некоторое искажение реальной картины в лучшую сторону, по-видимому, присуще всему исследованию.
Заключение
Итак, по итогам российской части исследования EUROASPIRE IV можно сделать вывод о наличии у нас значительных нереализованных возможностей по коррекции традиционных факторов риска у пациентов с ишемической болезнью сердца, которые перенесли острый инфаркт миокарда, острый коронарный синдром, чрескожное коронарное вмешательство и аортокоронарное шунтирование. Это же относится и к некоторым другим странам Европы. Между Россией и общей популяцией исследования существуют определенные различия, причем в некоторых областях (в частности, контроле АД), российские центры достигли даже лучших результатов, чем европейские страны в целом. Напротив, среди российских пациентов отмечалась худшая ситуация в отношении частоты курения, медицинской помощи по лечению табачной зависимости, отказу от курения, распространенности избыточной массы тела и ожирения, контроля уровня липидов крови.



