В экономически развитых странах в последние десятилетия ишемическая болезнь сердца (ИБС) является главной причиной смертности [1]. Среди такой группы заболеваний, как ИБС, цереброваскулярные заболевания и инфаркт миокарда (ИМ), по данным Росстата за 2015 г., в России лидируют ИБС — 29,1% (278 395 человек) и цереброваскулярные болезни — 16,9% (161 658 человек). Общее число умерших за первый квартал составило 507 тыс., это на 23,5 тыс. больше, чем в первом квартале 2014 г. Смертность от болезней кровообращения сделала самый большой вклад в увеличение общего числа смертей: в расчете на 100 тыс. населения на нее приходится максимальная доля — 718 человек (в 2014 г. — 687 человек).
ИБС часто развивается у трудоспособных лиц, значительно ограничивая их социальную и трудовую активность. В настоящее время общепризнанными механизмами развития ИБС являются нарушения липидного обмена, артериальная гипертензия (АГ), малоподвижный образ жизни, ожирение.
Гипоксия — несоответствие энергопотребности клетки энергопродукции в системе митохондрий. Образование энергии в клетке может нарушаться происходить по разным причинам: нарушения транспорта кислорода, нарушения кровообращения и микроциркуляции, расстройства внешнего дыхания и др. Дефицит энергии составляет основу гипоксии и приводит к метаболическим и функциональным нарушениям в разных органах и тканях. Непосредственной причиной гипоксии служит снижение количества кислорода в клетке. В результате угнетается митохондриальное окисление. В первую очередь происходит снижение активности NAD-зависимых оксидаз цикла трикарбоновых кислот (Кребса), при этом активность FAD-зависимой сукцинатоксидазы сохраняется, но позже ее активность снижается в условиях нарастающей гипоксии. В результате этих процессов развивается прогрессирующий дефицит молекул АТФ, которые служат источником энергии клетки. В условиях недостатка АТФ активируются процессы гликолиза как компенсаторная реакция для возмещения энергодефицита. Однако гликолиз приводит к быстрому накоплению лактата с последующим развитием ацидоза.
Гипоксия приводит к повреждению липидного слоя клетки, повреждается клеточная мембрана. Наступает распад фосфолипидов, торможение их синтеза, что приводит к повышению концентрации ненасыщенных жирных кислот (ЖК). Из-за нарушения барьерной функции клеточной мембраны в цитоплазме накапливается Са2+. Митохондрии захватывают Са2+, чтобы тормозить процессы его накопления, но при этом увеличивается расход АТФ. Таким образом, гипоксия нарушает энергетический обмен и стимулирует свободнорадикальное окисление и перекисное окисление липидов (ПОЛ), а активация этих механизмов усугубляет энергодефицит.
В норме кардиомиоциты получают АТФ за счет расщепления ацетил-КоА в цикле трикарбоновых кислот, и основными источниками энергии являются глюкоза и свободные жирные кислоты (СЖК). Около 80—90% ацетил-КоА образуется за счет окисления СЖК, а остальные 10—20% — за счет декарбоксилирования пировиноградной кислоты. В свою очередь примерно половина пировиноградной кислоты в клетке образуется за счет гликолиза, а вторая половина — из лактата, поступающего в клетку из крови. Катаболизм СЖК по сравнению с гликолизом требует большего количества кислорода для синтеза эквивалентного количества АТФ [1, 2].
В условиях гипоксии поступающего кислорода не хватает для окисления ЖК. В результате в митохондриях накапливаются недоокисленные активированные формы ЖК (ацилкарнитин, ацил-КоА), что приводит к нарушению транспорта АТФ в цитозоль и повреждает мембраны клеток.
Нарушенные процессы митохондриального окислительного фосфорилирования стимулируют восстановление кислорода с образованием свободных радикалов, а также оксидантов нерадикальной природы. Формируется окислительный стресс (ОС) [3].
ОС является дисбалансом между продуктами свободнорадикального окисления (СРО) и ПОЛ и способностью организма к удалению этих веществ, обладающих высокой химической активностью. ОС формируется при усилении выработки продуктов СРО и ПОЛ и истощении антиоксидантных защитных механизмов [4, 5]. В условиях хронического нарушения коронарного кровообращения ОС выступает как один из основных механизмов повреждения клетки. При хронической ишемии энергетическое снабжение сердца становится недостаточным, а компенсаторные механизмы компенсации истощаются [6].
В последние годы большое внимание уделяется изучению состояния эндотелия сосудов. Дисфункция эндотелия — основной патогенетический фактор микроангиопатии, хотя атеросклероз и АГ также оказывают негативное воздействие на сосуды. Нарушение функции эндотелия ведет к развитию ишемических нарушений сердца, нарушений гомеостаза, липидного обмена по типу гиперхолестеринемии, появлению гипергликемии. Известно, что АГ, ожирение, дислипидемия во многом реализуются именно через дисфункцию эндотелия. Она в большинстве случаев сопровождается ОС [7].
В настоящее время в лечении больных ИБС наряду с антиангинальной, антиагрегационной и гиполипидемической терапией важное место занимают препараты метаболического ряда, применяемые с целью нормализации метаболизма в кардиомиоцитах [8, 9].
В течение полувека и более для метаболической терапии использовалась глюкозо-инсулино-калиевая смесь (ГИК), применение которой приводит к увеличению потребления глюкозы и уменьшению синтеза СЖК.
Метаболическая терапия направлена на улучшение усвоения кислорода миокардом в условиях ишемии. В настоящее время список препаратов метаболического действия значительно расширен. Механизмы обеспечения данного эффекта следующие: торможение окисления СЖК (триметазидин); усиление поступления глюкозы в миокард (раствор глюкоза-натрий-инсулин); стимуляция окисления глюкозы (L-карнитин); восполнение запасов макроэргов (фосфокреатин); улучшение трансмиокардиального транспорта NAD+/NADH (аминокислоты); открытие К+-АТФ-каналов (никорандил).
Использование антигипоксантов достигает следующих целей: повышение эффективности использования митохондриями кислорода при стабилизации мембран митохондрий, поддержание активности сукцинатоксидазного звена цикла трикарбоновых кислот, экономия использования кислорода, увеличение образования АТФ без увеличения продукции лактата и др [10].
В 2005 г. С.В. Оковитым и А.В. Смирновым была предложена классификация антигипоксантов:
- Ингибиторы окисления жирных кислот.
- Сукцинатсодержащие и сукцинатобразующие средства.
- Естественные компоненты дыхательной цепи.
- Искусственные редокс-системы.
- Макроэргические соединения.
Ингибиторы окисления ЖК. К этой группе относят парциальные ингибиторы окисления ЖК (ранолазин, триметазидин, мельдоний) и непрямые ингибиторы окисления ЖК (карнитин).
Триметазидин МВ (тримектал МВ). Действие препарата связано с изменениями не параметров гемодинамики, а в метаболизме.
Триметазидин блокирует 3-кетоацилтиолазу — один из ключевых ферментов окисления ЖК, чем достигается снижение интенсивности их окисления в митохондриях, при этом небольшое количество кислорода, которое поступает в клетку, расходуется рационально — на аэробный путь окисления глюкозы с выработкой АТФ. Окисление глюкозы требует меньшего количества молекул кислорода по сравнению с окислением ЖК. Следовательно, повышается энергетическая устойчивость клетки к ишемии, АТФ снова образуется, снижается количество токсичных для клетки веществ [11].
При приеме препарата увеличиваются окисление пирувата и продукция АТФ, снижается концентрация АМФ и АДФ, блокируется накопление лактата, а значит и развитие ацидоза, подавляется СРО. Принципиальной особенностью триметазидина является прямое воздействие на ишемизированный миокард (кардиотропный эффект), которое приводит к более рациональному использованию поступающего кислорода [12, 13]. Триметазидин увеличивает количество молекул АТФ на 33%.
В рандомизированном клиническом исследовании TEMS у больных ИБС применение триметазидина способствовало уменьшению частоты и продолжительности эпизодов ишемии миокарда, отмечалось повышение толерантности к физической нагрузке.
В настоящее время установлено, что триметазидин весьма эффективен в случаях, когда ИБС сочетается с другими патологическими состояниями (у больных сахарным диабетом, АГ, с терминальной хронической почечной недостаточностью). При этом следует помнить, что триметазидин не используется при купировании приступов стенокардии.
Кроме того, триметазидин используется при хориоретинальных сосудистых нарушениях, головокружениях сосудистого происхождения, кохлеовестибулярных нарушениях ишемической природы (шум в ушах, нарушение слуха). С 2014 г. триметазидин отнесен к допинговым средствам, так как при приеме в больших дозах накапливается в скелетных мышцах, что необходимо учитывать при назначении спортсменам.
Ранолазин (ранекса) также является ингибитором окисления ЖК.
Препарат оказывает антиишемический эффект вследствие ограничения использования в качестве энергетического субстрата СЖК и увеличения использования глюкозы. Это приводит к образованию большего количества АТФ на единицу потребленного кислорода. Кроме того, ранолазин воздействует на поздний натриевый ток.
Подобно триметазидину препарат ингибирует β-окисление ЖК, однако точный механизм действия препарата не установлен. Предполагают, что он блокирует 3-кетоацил-КоА-тиолазу. В эксперименте показано, что ранолазин блокирует медленно инактивируемые натриевые каналы, в связи с чем обсуждают потенциальные возможности применения препарата при систолической дисфункции ЛЖ и ХСН.
Ранолазин обычно используют в комбинированной терапии у больных ИБС вместе с антиангинальными препаратами [14].
Мельдоний (милдронат) обратимо ограничивает скорость биосинтеза карнитина из его предшественника γ-бутиробетаина. Вследствие этого нарушается транспорт длинноцепочечных ЖК через мембраны митохондрий. Это означает, что мельдоний не способен полностью блокировать окисление всех ЖК. Частичная блокада окисления ЖК запускает альтернативный путь производства энергии — окисление глюкозы, которая эффективнее (на 12%) использует кислород для синтеза АТФ.
Мельдоний при стабильной стенокардии уменьшает частоту приступов стенокардии, повышает толерантность больных к физической нагрузке и снижает употребление нитропрепаратов короткого действия [15, 16].
Карнитин (витамин В11) играет важную роль в переносе длинноцепочечных ЖК через внутреннюю мембрану митохондрий, а также ключевую роль в образовании ацетил-КоА.
Антигипоксическое действие карнитина является дозозависимым и проявляется при применении высоких доз препарата, в то время как низкие дозы оказывают лишь витаминное действие.
Сукцинатсодержащие и сукцинатобразующие средства. Сукцинатсодержащие средства. К этой группе препаратов относят вещества, поддерживающие при гипоксии активность сукцинатоксидазного звена. Это FAD-зависимое звено цикла трикарбоновых кислот, которое в условиях гипоксии угнетается позже, чем NAD-зависимые оксидазы. Энергопродукция в клетке поддерживается благодаря наличию в митохондриях субстрата окисления в данном звене сукцината (янтарной кислоты).
Янтарная кислота реализует свои эффекты через рецепторы, расположенные на цитоплазматической мембране клеток и сопряженные с G-белками (G/Go и Gq). Эти рецепторы расположены в почках (эпителий проксимальных канальцев, клетки юкстагломерулярного аппарата), в печени, селезенке, сосудах. При активации этих рецепторов сукцинатом увеличивается реабсорбция фосфата и глюкозы, стимулируется глюконеогенез, повышается артериальное давление [17]. Одним из представителей этого класса является реамберин. Препарат обладает дезинтоксикационными и антиоксидантными (за счет активации ферментативного звена антиоксидантной системы) свойствами.
Реамберин используют при перитоните с синдромом полиорганной недостаточности, тяжелых травмах, острых нарушениях мозгового кровообращения. Выявлена эффективность препарата при инфекционных заболеваниях (грипп и ОРВИ, пневмонии, острые кишечные инфекции) [18].
Использование препарата у больных при аортокоронарном шунтировании с пластикой левого желудочка (ЛЖ) или протезированием клапанов позволяет снизить частоту развития осложнений в раннем послеоперационном периоде (в том числе повторных ИМ, инсультов, энцефалопатии).
Еще один представитель этой группы — цитофлавин. Препарат сочетает в себе янтарную кислоту с рибофлавином, чем достигается активность сукцинатдегидрогеназы и проявляется непрямое антиоксидантное действие (за счет восстановления окисленного глутатиона). В основном цитофлавин используется при различных повреждениях центральной нервной системы (ишемический инсульт, токсическая, гипоксическая и дисциркуляторная энцефалопатия), а также у больных, находящихся в критическом состоянии [19, 20].
Мексидол является комбинированным сукцинатсодержащим препаратом, представляющим собой комплекс сукцината с антиоксидантом эмоксипином. Обладает относительно слабой антигипоксической активностью, но усиливает транспорт сукцината через мембраны.
Основные клинические испытания были проведены по изучению его эффективности при ИМ, ИБС, остром нарушении мозгового кровообращения, дисциркуляторной энцефалопатии.
Сукцинатобразующие средства. Оксибутират натрия способен превращаться в сукцинат, с чем связано антигипоксическое действие. Активирует обменные процессы в тканях мозга, сердца, сетчатке глаза, повышает их устойчивость к гипоксии. Улучшает сократительную способность миокарда, микроциркуляцию, клубочковую фильтрацию (стабилизирует функцию почек в условиях кровопотери).
Оксибутират натрия обладает элементами ноотропной активности; характерным является его выраженное антигипоксическое действие; он повышает устойчивость организма, в том числе тканей мозга, сердца, а также сетчатки глаза к недостаточности кислорода. Препарат оказывает седативное и центральное миорелаксантное действие, в больших дозах вызывает сон и состояние наркоза. Применяется в неврологии, а также анестезиологии и офтальмологии. Благоприятное действие оксибутирата натрия при гипоксии обусловлено тем, что он активирует энергетически более выгодный пентозный путь обмена глюкозы с ориентацией его на путь прямого окисления и образования пентоз, входящих в состав АТФ.
Естественные компоненты дыхательной цепи. Представителями этого класса являются убихиноны — жирорастворимые коферменты, которые являются естественными компонентами дыхательной цепи митохондрий клеток. Цитохром С и убихинон (кофермент Q10) переносят электроны в дыхательной цепи и принимают участие в окислительном фосфорилировании. Максимальное содержание убихинона в органах с наибольшими энергетическими потребностями (в сердце и печени). Убихинон принимает активное участие в процессах активизации и регуляции ферментных систем человеческого организма.
Цитохром С эффективен в комбинированной терапии критических состояний. Эффективность препарата изучалась при асфиксии новорожденных, отравлении снотворными средствами, окисью углерода, различных повреждениях миокарда, нарушениях мозгового и периферического кровообращения. Средняя доза препарата составляет 10—15 мг внутривенно, внутримышечно или внутрь (1—2 раза в день).
Убихинон у больных с ИБС и стенокардией I—II функционального класса (ФК) улучшает клиническое течение заболевания, снижает частоту приступов, повышает толерантность к физической нагрузке. Препарат малоэффективен у больных с резким снижением толерантности к физической нагрузке.
При ХСН использование убихинона в комбинированной терапии позволяет увеличить сократимость ЛЖ и улучшить функцию эндотелия. Достоверное положительное влияние препарат оказывает на ФК у больных с ХСН и число госпитализаций. Положительные эффекты препарата проявляются преимущественно при использовании высоких (300 мг/сут) доз препарата [21].
Искусственные редокс-системы. Эти препараты устраняют излишки электронов из звеньев дыхательной цепи, тем самым восстанавливается ее функция. К препаратам этой группы относят олифен (гипоксен). Препарат используется при тяжелых травмах, шоке, кровопотере, обширных хирургических вмешательствах, деструктивном панкреатите, способствует более быстрой стабилизации гемодинамики в послеоперационном периоде. У больных ИБС он уменьшает ишемические проявления, снижает свертываемость крови и общее потребление кислорода.
Макроэргические соединения. Антигипоксантом этого класса является креатинфосфат (неотон). В миокарде и в скелетной мышце креатинфосфат используется для ресинтеза АТФ, необходимой для образования энергии. Действие креатинфосфата состоит в фосфорилировании АДФ и увеличении тем самым количества АТФ в клетке.
Основными показаниями к применению креатинфосфата служат острый период ИМ и интраоперационная ишемия миокарда или конечностей. Важно, что однократная инфузия препарата не влияет на клинический статус и состояние сократительной функции ЛЖ.
В настоящее время в качестве цитопротектора с учетом имеющихся исследований кардиологических больных наиболее убедительно зарекомендовал себя триметазидин [22]. Метаболическая терапия у пациентов с ишемией миокарда и ХСН эффективно улучшает качество жизни, сократимость миокарда и уменьшает частоту ангинозных приступов, хотя доказательная база по влиянию на долгосрочный прогноз у больных недостаточна [23, 24]. Цитопротекция может быть рекомендована в качестве дополнительной курсовой терапии пациентам с ИБС и ХСН моложе 70 лет для улучшения клинической картины заболеваний [25].
В настоящее широко используется генерический препарат триметазидин МВ (тримектал МВ, «Вертекс»), обладающий биоэквивалентностью по отношению к оригинальному препарату, доказанной эффективностью, безопасностью, оптимальным соотношением стоимости и эффективности [26].
Клиническая фармакокинетика и эффективность препарата триметазидин МВ. Препарат принимают внутрь, во время еды. Рекомендуемая доза составляет 35 мг 2 раза в сутки утром и вечером во время еды. Продолжительность курса терапии определяется индивидуально. После приема внутрь препарат быстро и практически полностью абсорбируется из желудочно-кишечного тракта. Биодоступность составляет 90%, время достижения максимальной концентрации (Сmах) в плазме крови 3 ч, связывание с белками плазмы 16%. Легко проникает через гистогематические барьеры. Период полувыведения составляет 7 ч. Выводится из организма почками (около 60% в неизмененном виде).
Мы наблюдали 74 больных в возрасте от 54 до 75 лет с клиническими признаками стенокардии II ФК по Канадской классификации. При проведении исследования пациенты были разделены на 2 сопоставимые группы: в контрольной — 34 больных на фоне стандартной терапии (статины, антиагреганты, β-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента – АПФ); в основной группе — 40 больных, которым был добавлен триметазидин МВ в дозе 35 мг 2 раза в день.
Положительная динамика клинического состояния пациентов и тяжести ХСН наблюдалась в обеих группах. По всем параметрам различия между группами через 3 мес от начала терапии достигли статистической значимости. Так, в основной группе на фоне приема триметазидина МВ через 3 мес терапии произошло достоверное уменьшение ФК ХСН (р<0,05): у 11 (27,5%) сохранялся исходный ФК ХСН, у 7 (17,5%) ФК уменьшился с I до 0, у 17 (42,5%) — со II до I, а у 5 (12,5%) — с III до II.
В контрольной группе динамики ФК ХСН не было отмечено у 17 (50%) пациентов, уменьшение ФК ХСН с III до II достигнуто у 5 (14%). У 12 (35%) пациентов произошло уменьшение со II до I ФК. Таким образом, у пациентов, принимавших триметазидин МВ в составе комбинированной терапии, выявлено более значительное снижение ФК ХСН и повышение толерантности к физической нагрузке, чем в контрольной группе. Толерантность к физической нагрузке определялась при велоэргометрической пробе. Основным клиническим эффектом триметазидина МВ, свидетельствующим об улучшении показателей гемодинамики, было достоверное по сравнению с исходным уменьшение частоты приступов стенокардии, количества употребляемых таблеток нитроглицерина.
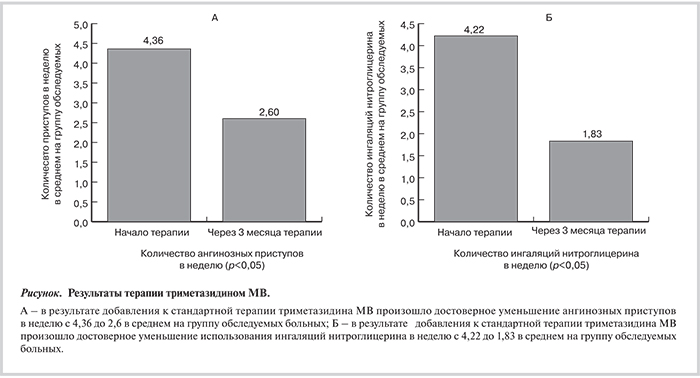
При анализе полученных данных отмечено, что у больных, получавших триметазидин МВ, получено достоверное уменьшение количества ангинозных приступов в неделю с 4,36±0,5 до 2,61±0,4 (р<0,05; см. рисунок А), количества используемых ингаляций нитроглицерина в неделю с 4,22±1,03 до 1,83±0,95 (р<0,05; см. рисунок Б). Отчетливый клинический эффект был отмечен у 76% больных этой группы.
В большинстве случаев больные отмечали улучшение самочувствия в конце 2-й недели лечения, что проявлялось уменьшением частоты ангинозных болей, повышением толерантности к физическим нагрузкам, уменьшением слабости. Достигнутый антиангинальный эффект сохранялся на протяжении всего курса лечения. Случаев развития толерантности к препарату отмечено не было. Переносимость препарата хорошая. Динамические наблюдения с применением эхокардиографии в группе больных, принимавших триметазидин МВ, показали достоверное увеличение ударного индекса с 42,21±12,32 до 43,64±1,96 (р<0,05), фракции выброса с 52,26±2,18 до 56,12±1,99% (р<0,05), сердечного индекса с 2,94±0,1 до 3,13±0,18 (р<0,05) и уменьшение индекса конечного систолического объема с 26,75±3,36 до 24,8±2,8 мм (р<0,05). При эхокардиографии выявили следующие основные положительные эффекты триметазидина МВ: достоверно уменьшился индекс конечного систолического объема ЛЖ, статистически значимо увеличились ударный и сердечный индексы, фракция выброса.
Противопоказания к назначению триметазидина: почечная недостаточность (клиренс креатинина меньше 15 мл/мин); выраженные нарушения функции печени; беременность; период лактации (грудного вскармливания); детский и подростковый возраст до 18 лет (эффективность и безопасность не установлены); повышенная чувствительность к компонентам препарата.
Побочные эффекты триметазидина. Со стороны пищеварительной системы: редко гастралгия, тошнота, рвота; также возможны аллергические реакции (прежде всего кожный зуд); редко головная боль, ощущение сильного сердцебиения.
Прием препарата возможен пожизненно, так как нет накопительного эффекта.
Заключение
Таким образом, необходимо и оправдано более широкое использование миокардиального цитопротектора триметазидина МВ (тримектала МВ, качественного отечественного генерического препарата триметазидина МВ) в кардиологической и терапевтической практике, что определяется его высокой эффективностью как препарата, оказывающего выраженный кардиоцитопротективный эффект, и фармакоэкономической составляющей (оптимальное соотношение стоимости и эффективности).



