Приверженность пациента к терапии является залогом успешного лечения заболевания и уменьшения частоты развития осложнений. Под приверженностью к терапии понимают степень соответствия поведения больного рекомендациям, полученным от врача в отношении приема препаратов, соблюдения диеты и изменения образа жизни. Термин «приверженность» пришел на смену термину «комплаентность», под которой понимали сложный поведенческий процесс, значительно подверженный влиянию окружающей пациента среды, деятельности врачей и организации системы здравоохранения. Эволюция понятий символизировала переход к принципиально другому пониманию взаимоотношений между пациентом и лечащим врачом, так как термин «приверженность к терапии» подразумевает сотрудничество между пациентом и специалистом, а не пассивное следование инструкциям врача. Наиболее остро вопрос приверженности встает при назначении терапии на неопределенно долгий срок, что особенно актуально для пациентов с сердечно-сосудистыми заболеваниями в отношении антигипертензивной, гиполипидемической и, безусловно, антикоагулянтной терапии (АКТ). Постоянная АКТ — необходимый компонент лечения пациентов с неклапанной фибрилляцией предсердий (ФП) [1, 2]. Низкая приверженность к АКТ ассоциирована с ростом числа как тромбоэмболических, так и геморрагических осложнений. В связи с этим активно обсуждаются оптимальные схемы и режимы дозирования новых антикоагулянтов (НОАК) — неантагонистов витамина К.
Приверженность к АКТ: проблемы варфарина. Традиционно приверженность пациента к назначенному лечению складывается из трех элементов: начала лечения, его осуществления и дальнейшего удержания пациента или же прекращения терапии. Основными компонентами приверженности являются постоянство в терапии (persistence) — то, как долго пациент придерживается предписанного режима приема; и исполнение (execution) — то, как четко пациент выполняет рекомендованный режим [3].
Низкая приверженность к лечению может проявляться по-разному: пропусками вечерних доз, пропусками вечерних и утренних доз, «каникулами» в приеме лекарств или преждевременным прекращением терапии [4]. Наиболее ярко проблемы низкой приверженности проявляются для препаратов с узким терапевтическим окном, к которым относятся и непрямые антикоагулянты — антагонисты витамина К, имеющие широкий спектр показаний, в том числе для неопределенно долгого применения [1, 5]. Обычно пациенты с неохотой соглашаются на прием варфарина, опасаясь кровотечений, и часто прекращают его в связи со сложностью удержания целевого международного нормализованного отношения (МНО) и связанными с этим побочными эффектами. Согласно анализу Базы данных общей практики в Великобритании (41 910 пациентов с ФП), 30% пациентов, получавших варфарин, прекратили прием препарата в течение первого года терапии [6]. В исследовании T. Gomes и соавт. (популяционное исследование 125 195 пациентов с ФП) показано, что прием варфарина в 1-й месяц может быть ассоциирован с наибольшей частотой кровотечений (отношение риска — ОР 11,8 при 95% доверительном интервале — ДИ от 11,1 до 12,4) по сравнению с ОР 3,4 (при 95% ДИ от 3,4 до 3,5; р<0,001) через 5 лет [7]. В то же время проведенное L. Azoulay и соавт. исследование случай—контроль (70 766 пациентов с впервые выявленной ФП) показало увеличение риска развития инсульта в течение 1-го месяца терапии варфарином на 71% (ОР 1,71 при 95% ДИ от 1,39 до 2,12) по сравнению с ОР 0,55 (при 95% ДИ от 0,49 до 0,61) через 90 дней [8]. В исследованиях ROCKET-AF [9] и ARISTOTLE [10] наибольшее количество тромбоэмболических осложнений регистрировалось в конце периода наблюдения в фазу перехода к антагонистам витамина К [11].
Известно, что при нерегулярном приеме варфарина МНО ниже целевого ассоциированно с повышением риска тромбозов, а МНО выше целевого при приеме лишних доз — с риском кровотечений. В исследовании IN-RANGE приверженность к приему варфарина оценивалась методом электронного мониторинга с использованием электронной системы MEMS, в которой регистрировалось время открытия каждой упаковки с препаратом [12]. Прием варфарина достаточно часто ассоциировался с низкой приверженностью к лечению: среди 136 пациентов, наблюдавшихся в среднем в течение 32 нед, 92% пропустили прием хотя бы одной дозы или приняли одну лишнюю таблетку; 36% пропустили прием более 20% препарата, а 4% приняли более 10% лишних доз. Низкая приверженность отразилась на контроле коагуляции: пропуск 1—2 доз в неделю (20—30% от общего количества) ассоциировался с почти двукратным увеличением частоты регистрации нецелевого МНО, а при приеме лишних таблеток МНО значительно возрастало [13]. Анализ баз данных NAMCS и NHAMCS показал, что наибольшее количество (33%) экстренных госпитализаций по поводу осложнений лекарственной терапии у пожилых пациентов США связаны с передозировкой варфарина [14].
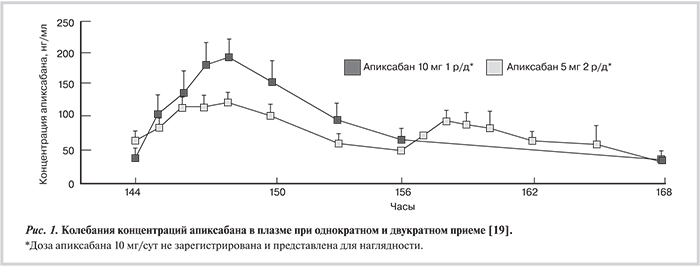
Обоснование выбора режима дозирования новых пероральных антикоагулянтов (НОАК): двукратный или однократный прием? Клинико-фармакологические аспекты выбора режима терапии НОАК. Определяющими факторами при выборе кратности приема НОАК в течение суток должны быть длительность антикоагулянтного действия препарата, широта терапевтического действия (оптимальный баланс эффективности и безопасности) и результаты исследований II фазы при сравнении разных режимов приема и подборе доз, выполненных для всех НОАК [15]. Фармакодинамические эффекты препаратов из группы НОАК тесно связаны с их концентрацией в плазме, и оптимальный дозовый режим подбирается с учетом периода полувыведения [16—20]. Период полувыведения НОАК зависит от возраста пациента и функции почек, но в среднем составляет для дабигатрана 12—17 ч, для ривароксабана 5—9 ч у молодых и 11—13 ч у пожилых лиц, для апиксабана 12 ч [21, 22]. В целом все НОАК обладают сходными фармакокинетическими параметрами, но кратность приема препаратов различается: апиксабан и дабигатран назначают 2 раза в сутки, а ривароксабан и не зарегистрированный пока в Российской Федерации эдоксабан — 1 раз. Это обусловлено тем, что при применении антикоагулянтов фармакокинетические показатели не совпадают с параметрами антикоагулянтного эффекта [15]. При однократном применении соотношение пик/спад составляет около 4,5 для дабигатрана [22], около 10 для ривароксабана [17, 18], около 10 для апиксабана [19] и 10—30 для эдоксабана [20]. Чем выше соотношение, тем больше суточные колебания концентрации препарата в плазме, которые клинически выражаются в повышении риска кровотечений на пике действия и повышении риска тромбоэмболических осложнений на спаде. Наиболее наглядно это продемонстрировано в отношении апиксабана с помощью методов фармакокинетического моделирования результатов исследований III фазы (рис. 1). Видно, что двукратный прием обеспечивает снижение пиковой концентрации, уменьшая риск кровотечений, и повышение минимальных концентраций, увеличивая эффективность. Аналогичные результаты продемонстрированы в фармакокинетическом моделировании результатов исследования APROPOS (выбор дозы и режима апиксабана для профилактики венозных тромбоэмболий после протезирования коленного сустава) [23].
Таким образом, в настоящее время большинство врачей и исследователей склоняются к мнению, что двукратный прием НОАК, период полувыведения которых обычно не превышает 12 ч, обеспечивает наилучшую защиту и оптимальную безопасность в течение суток.
Терапевтические преимущества двукратного режима дозирования НОАК. Несмотря на кажущуюся возможность упростить режим дозирования и повысить приверженность пациента к лечению, однократное назначение препарата для достижения необходимых фармакодинамических и клинических результатов требует практически идеального соблюдения режима приема, тогда как назначение препарата 2 раза в сутки оставляет больше возможностей для варьирования времени приема препарата и случайно пропущенных доз.
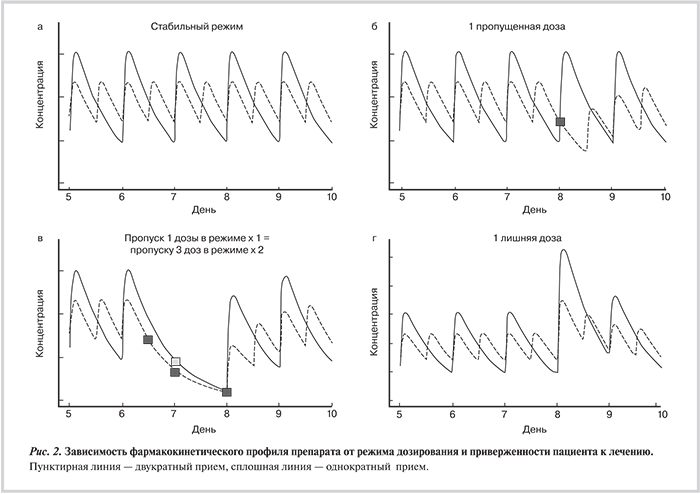
На рис. 2 показано изменение фармакокинетического профиля типичного препарата с периодом полувыведения 12 ч при различных режимах дозирования (1 или 2 раза в сутки) и различных нарушениях приверженности. На рис. 2, а (повторное дозирование при идеальной приверженности) видно, что при одинаковых фармакокинетических характеристиках, соотношение подъем/спад значительно меньше при двукратном режиме дозирования. На рис. 2, б показан фармакокинетический профиль при двукратном режиме дозирования и одном пропуске дозы препарата. Итоговая концентрация совпадает с наименьшей точкой графика однократного приема; это позволяет предположить, что пропуск одной дозы при двукратном приеме не является терапевтически критичным. На рис. 2, в показано, что пропуск одной дозы при однократном режиме эквивалентен пропуску 3 доз при двукратном режиме. На рис. 2, г показано, что повышение пиковой концентрации при приеме лишней дозы меньше при двукратном приеме [11].
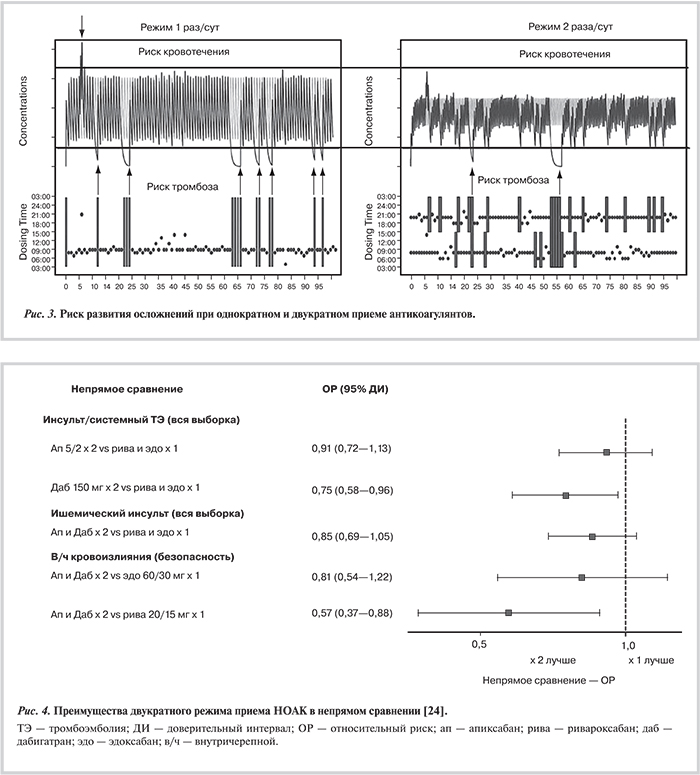
Таким образом, двукратный режим приема антикоагулянтов более безопасен при неадекватной приверженности к лечению. В гипотетической фармакокинетической модели изменения концентраций антикоагулянтов при однократном и двукратном дозировании показано, что в течение 100 дней 15 пропусков в режиме однократного приема эквивалентны 30 пропускам в режиме двукратного приема (рис. 3) [11].
В мета-анализ, проведенный A. Clemens и соавт. с целью определения оптимального режима дозирования НОАК, были включены 4 исследования III фазы, посвященные профилактике тромбоэмболических осложнений с использованием НОАК [24]: RE-LY (дабигатран двукратно, 18 113 пациентов), ROCKET-AF (ривароксабан однократно, 14 264 пациентов), ARISTOTLE (апиксабан двукратно, 18 201 пациент) и DU-176b (эдоксабан однократно по сравнению с варфарином, 21 105 пациентов) [10, 13, 25—27]. В результате показано, что, во-первых, двукратное назначение препаратов более эффективно предотвращает инсульты и системные тромбоэмболические осложнения по сравнению с однократным и более безопасно в отношении риска развития внутричерепных кровоизлияний (табл. 1, рис. 4). Во-вторых, все НОАК продемонстрировали снижение общей смертности на 10% по сравнению с варфарином.

Преимущества двукратного режима дозирования подтверждаются результатами исследований III фазы для НОАК. Так, апиксабан (ARISTOTLE) и дабигатран (RE-LY) более эффективно предотвращали тромбоэмболические осложнения по сравнению с варфарином (табл. 2) [13, 25, 26]. При этом ривароксабан и эдоксабан при однократном приеме предотвращали тромбоэмболические осложнения не хуже варфарина, обладая таким же или превосходящим профилем безопасности [16, 27]. Таким образом, двукратный прием антикоагулянтов — неантагонистов витамина К группы НОАК (в частности, апиксабана), обеспечивает наилучший профиль эффективности и безопасности у пациентов с ФП.
Двукратный прием НОАК: значение апиксабана. Апиксабан одобрен для лечения тромбоза глубоких вен нижних конечностей и тромбоэмболии легочной артерии, профилактики рецидивирующих венозных тромбоэмболий у взрослых, профилактики инсульта и системных эмболий у пациентов с неклапанной ФП, профилактики венозных тромбоэмболий после протезирующих операций на бедре и колене. Двойное слепое исследование AVERROES показало, что у пациентов с ФП, которым не показан прием варфарина, апиксабан снижает риск развития инсульта и системных тромбоэмболий эффективнее, чем ацетилсалициловая кислота [28]. Апиксабан ассоциировался с 55% снижением частоты развития инсультов и системных эмболий в отсутствие повышения частоты больших или внутричерепных кровотечений. В связи с явными значительными преимуществами апиксабана исследование было остановлено досрочно. В исследовании ARISTOTLE апиксабан более эффективно предотвращал инсульты или системные эмболии у пациентов с ФП по сравнению с варфарином (частота первичной конечной точки 1,27% в год и 1,6% в год соответственно (ОР 0,79 при 95% ДИ от 0,66 до 0,95; р=0,01), реже вызывал кровотечения — 2,13% в год по сравнению с 3,09% в год (ОР 0,69 при 95% ДИ от 0,60 до 0,80; р<0,001) и ассоциировался с меньшей смертностью — 3,52% по сравнению с 3,94% (ОР 0,89 при 95% ДИ от 0,80 до 0,99; р=0,047) [13]. В исследовании AMPLIFY было показано, что в лечении острых венозных тромбоэмболий апиксабан оказался не менее эффективным, чем стандартная схема лечения (эноксапарин с переходом на варфарин): 2,3% и 2,7% соответственно (ОР 0,84 при 95% ДИ от 0,60 до 1,18; р<0,001). При этом применение апиксабана ассоциировалось с меньшим риском кровотечений (0,6% по сравнению с 1,8%; ОР 0,31 при 95% ДИ от 0,17 до 0,55; р<0,001) [29].
Как показано выше, наиболее приемлемым является двукратный прием, который в случае апиксабана обеспечивает оптимальный баланс эффективности и безопасности даже при неидеальной приверженности к лечению, отражая приоритет клинических исходов, а не удобство применения. Необходимость принимать препарат дважды в день может быть ассоциирована с более низкой приверженностью к лечению. Это утверждение подвергается сомнению в обзоре 76 исследований, не выявившем достоверных различий в приверженности к лечению при сравнении однократного и двукратного режимов дозирования (79±14 и 69±15% соответственно; р>0,05) [30]. Х. Song с соавт. также опубликовали данные, демонстрирующие отсутствие существенных различий при однократном и двукратном применении лекарственных средств [31]. К тому же в настоящее время разработаны различные подходы, позволяющие улучшить приверженность к лечению, часто более эффективные, чем формальная попытка повысить приверженность путем сокращения кратности суточного приема препарата [11].
Повышение приверженности к НОАК в клинической практике. Известно 5 факторов, влияющих на приверженность пациентов к длительной терапии: система здравоохранения; социально-экономические факторы; факторы, связанные с состоянием здоровья; с лечением и с самим пациентом. Система здравоохранения и врачи вносят значительный вклад в повышение приверженности пациентов путем мониторинга и обеспечения правильного приема пациентом препаратов [3]. Недавно опубликованный обзор по анализу вмешательств, направленных на повышение приверженности к терапии, показал, что наиболее значимым фактором являлся электронный мониторинг приема препаратов с обратной связью (на 8,8% эффективней, чем вмешательства без него; р<0,01) [32]. Анализируя прием препарата каждым пациентом, врач может обсудить с пациентом причину недостаточной приверженности к лечению в определенные моменты времени и предложить решения для предотвращения подобных ситуаций в будущем. Такие вмешательства по улучшению приверженности содержат в себе элемент обучения за счет повышения уровня знаний пациента о его заболевании и о важности приверженности к терапии и мотивации за счет повышения ответственности пациента [4]. Другие возможные способы повышения приверженности суммированы в табл. 2 [11].
Европейская Ассоциация ритма сердца предложила алгоритм структурированного наблюдения пациента, получающего НОАК. Алгоритм включает обязательные визиты в определенные периоды времени (например, на старте терапии, через 1, 3 и 6 мес и т.д.). В эти дни пациент должен приходить к своему лечащему врачу (кардиологу, врачу общей практики) или медсестре, которые должны оценить приверженность пациента к лечению, обеспечить обратную связь, а при необходимости обучение и мотивацию [16]. Более того, в отношении пациентов с ФП выдвинуто предложение по разработке междисциплинарных экспертных программ для структурирования ежедневной врачебной практики [33]. Важную роль в подобных программах будут играть специально обученные медсестры, которые могут являться центральными координаторами всего процесса, так как они имеют больше времени для общения с пациентом. Клиники, специализирующиеся на назначении антагонистов витамина К, в будущем могут пересмотреть свою работу с учетом указанного подхода [34]. Подобные программы должны задействовать электронный и отдаленный мониторинг приверженности по аналогии с отдаленным наблюдением пациентов с имплантированными устройствами [35].
Неоптимальная приверженность к лечению может быть обусловлена тем, что пациент не понимает необходимость следования определенным требованиям. Эту часть проблемы можно устранить с помощью обучения пациентов. Практически все мероприятия по повышению приверженности содержат в себе элемент обучения как во время визитов в клинику, так и при телефонных контактах. Так, в рандомизированном клиническом исследовании TREAT сравнивались стратегии обучения пациентов, получающих варфарин, со стандартным подходом (n=97). Показано, что повышение информированности пациента о заболевании повышает процент времени поддержания целевого МНО в течение первых 6 мес терапии (76,2% по сравнению с 71,3%; р=0,035) [36].
Первым крупным проспективным рандомизированным клиническим исследованием по оценке влияния образовательных программ на приверженность и постоянство приема НОАК, проводимым в настоящее время, является AEGEAN. Его цель — сравнение приверженности к апиксабану при стандартном подходе (583 пациента) и при использовании дополнительной образовательной программы пациента с дальнейшим виртуальным контролем (579 пациентов) у пациентов с неклапанной ФП в течение 48 нед. Первичной конечной точкой является приверженность к лечению в течение 24 нед, вторичной — постоянство терапии к 24-й неделе. Специальная образовательная программа включает информационные брошюры, напоминающие устройства (брелки со звонком, напоминания в мобильных телефонах, приложения для смартфонов) и доступ к виртуальной клинике, сотрудниками которой является персонал антикоагуляционных клиник. Приверженность оценивается с помощью карманного электронного устройства Helping Hand, однако результаты измерений не используются для обратной связи в ходе исследования. На конгрессе ЕОК (Лондон, 2015) были доложены результаты первых 24 нед терапии. В обеих группах показана очень высокая приверженность к терапии (88,5% в контрольной группе и 88,3% в группе обучения; р=0,89). Устойчивость в лечении составила 90,5% и 91,1%, соответственно (р=0,76). Таким образом, продемонстрирована высокая приверженность и постоянство приема апиксабана в целом, хотя использование специальных образовательных программ не имело преимуществ по сравнению со стандартным подходом [37].
В комментариях к первым результатам подчеркивается, что приверженность к лечению в течение 6 мес всегда значительно выше, чем при более длительном приеме препаратов. Кроме того, пациенты, участвующие в исследовании по изучению приверженности, всегда более привержены к терапии, чем пациенты в реальной практике. Таким образом, промежуточный вывод о том, что образовательные программы не способны значительно повлиять на приверженность к терапии НОАК, следует трактовать с осторожностью. Общая продолжительность исследования AEGEAN должна составить 48 нед и набор еще продолжается [38].
Заключение
Непрямые антикоагулянты — препараты с достаточно широким спектром показаний, часто назначаемые на неопределенно долгий срок, это делает проблему приверженности к ним особенно актуальной. Низкая приверженность к приему непрямых антикоагулянтов повышает риск как тромбоэмболических, так и геморрагических осложнений. Все новые антикоагулянты (НОАК) обладают сходными фармакокинетическими параметрами, но отличаются кратностью применения у пациентов с фибрилляцией предсердий. Двукратный режим назначения НОАК обеспечивает наилучшую эффективность и безопасность антикоагулянтной терапии. Промежуточный результат исследования AEGEAN демонстрирует высокую приверженность и постоянство в терапии апиксабаном, назначаемом дважды в день.



