Задачи клинических рекомендаций — обобщать, оценивать и своевременно обновлять все имеющиеся доказательства, помогая врачам в выборе оптимальных стратегий ведения отдельного пациента (с определенным заболеванием) с учетом их влияния на исход лечения, а также соотношения риск-польза конкретного способа диагностики или терапии [1, 2]. Последние рекомендации Европейского кардиологического общества (ЕКО), в которых рассматриваются стратегии пероральной антитромботической терапии, опубликованы в 2011 г. применительно к ведению пациентов с нестабильной стенокардией (НС) или инфарктом миокарда без подъема сегмента ST (ИМбпST) [1], а затем — в 2012 г. применительно к ведению пациентов c инфарктом миокарда с подъемом сегмента ST (ИМпST) [2]. В обоих документах утверждалось превосходство новейших антитромботических препаратов, а именно прасугрела и тикагрелора над клопидогрелом. Как в тех, так и в других европейских рекомендациях применение клопидогрела рекомендуется только в случаях, когда прасугрел или тикагрелор «не имеются в наличии или противопоказаны» [1, 2]. В сжатом виде актуальные рекомендации ЕКО по острым коронарным синдромам (ОКС) приведены в табл. 1.
 В отличие от европейских коллег, рабочая группа по выработке рекомендаций Американской коллегии кардиологов (АКК) и Американской ассоциации сердца (ААС) представила более сбалансированный, рациональный и обоснованный взгляд, не провозглашая превосходства какого-либо одного из антагонистов рецепторов P2Y12 и принимая во внимание весь массив доказательств, а не опираясь на единичные исследования в поддержку более новых препаратов [3—5]. Основные положения текущих рекомендаций АКК/ААС, изданных в США в 2012—2013 гг., кратко представлены в табл. 2 и 3.
В отличие от европейских коллег, рабочая группа по выработке рекомендаций Американской коллегии кардиологов (АКК) и Американской ассоциации сердца (ААС) представила более сбалансированный, рациональный и обоснованный взгляд, не провозглашая превосходства какого-либо одного из антагонистов рецепторов P2Y12 и принимая во внимание весь массив доказательств, а не опираясь на единичные исследования в поддержку более новых препаратов [3—5]. Основные положения текущих рекомендаций АКК/ААС, изданных в США в 2012—2013 гг., кратко представлены в табл. 2 и 3.
Различия в рекомендациях, с одной стороны, очевидны, с другой стороны, трудны для понимания, поскольку у членов как европейской, так и американской рабочих групп был и есть полный доступ к одним и тем же открытым данным. Важно отметить существенный разрыв между рекомендациями общества и каждодневной практикой. Это особенно справедливо с учетом низкой частоты применения прасугрела и, особенно, тикагрелора в клинической практике по всему миру и в Европе в частности. Несколько вопросов заслуживают краткого обсуждения и приведены ниже.
Мы попробуем заполнить некоторые пробелы и постараемся прояснить, почему клиническое использование двух новейших антитромботических препаратов (прасугрела и тикагрелора) является не столь частым. Кроме того, мы рассмотрим доказательства, приведшие к различиям в рекомендациях по ОКС.
Выборка доказательств
Существует огромное несоответствие между обширной базой доказательств, относящихся к клопидогрелу, и сравнительным превосходством по «эффективности» прасугрела (TRITON) или тикагрелора (PLATO) над клопидогрелом, выведенным на базе подгрупп единичных исследований [6, 7]. Даже с учетом очевидных ограничений, имеющихся в более ранних исследованиях клопидогрела в условиях ОКС, таких как CURE [8], CREDO [9], COMMIT [10] и CURRENT [11], имеются согласованные подтверждения клинической пользы клопидогрела при лечении пациентов с ОКС.
Нетрудно заявить о превосходстве антитромботических препаратов нового поколения, однако, чтобы преодолеть критическую массу данных по клопидогрелу с целью изменения текущих практик по назначению лечения, требуется гораздо больше доказательств, чем «официальные» публикации исследований TRITON [6] или PLATO [7]. Представляется, что члены рабочей группы ЕКО ограничили доказательства исключительно первичными публикациями в «The New England Journal of Medicine» (NEJM) [6, 7] и бесчисленными вторичными ретроспективными (post hoc) анализами подгрупп тех же самых исследований.
Было бы более сбалансированным, надежным и практичным рассмотреть обзоры Управления по контролю за качеством пищевых продуктов и лекарственных препаратов США (Food and Drug Administration — FDA) как по прасугрелу [12], так и по тикагрелору [13]. Эти подробные серии документов по обоим препаратам (прасугрелу, тикагрелору), как и более ранние документы по клопидогрелу, находились в общественном доступе на момент выхода рекомендаций и/или их обновлений.
 Поскольку в европейских рекомендациях как по ИМпST, так и по ИМбпST [1, 2] обычно не дается ссылок на эти значимые доказательства, опубликованные государственными учреждениями (в США), представляется, что коллектив авторов и рецензенты не приняли во внимание эти важнейшие данные. Нет сомнений в том, что даже краткий взгляд на обзоры FDA [12, 13] вызывает ряд серьезных вопросов к рекомендациям ЕКО по ОКС вследствие ряда крупных недочетов, не упомянутых в первичных публикациях в журнале NEJM [6, 7]. Вот лишь некоторые из них: изменение и употребление «более свободного» определения инфаркта миокарда (ИМ) в исследовании TRITON [12, 14], а также увеличивающийся со временем риск кровотечения и развития рака после применения прасугрела [12, 15]; несоответствие между приемлемыми показателями нефатального ИМ и инсульта и выраженной частотой сосудистой смерти с необычным отсроченным временем наступления предполагаемой пользы от тикагрелора в PLATO [13, 16].
Поскольку в европейских рекомендациях как по ИМпST, так и по ИМбпST [1, 2] обычно не дается ссылок на эти значимые доказательства, опубликованные государственными учреждениями (в США), представляется, что коллектив авторов и рецензенты не приняли во внимание эти важнейшие данные. Нет сомнений в том, что даже краткий взгляд на обзоры FDA [12, 13] вызывает ряд серьезных вопросов к рекомендациям ЕКО по ОКС вследствие ряда крупных недочетов, не упомянутых в первичных публикациях в журнале NEJM [6, 7]. Вот лишь некоторые из них: изменение и употребление «более свободного» определения инфаркта миокарда (ИМ) в исследовании TRITON [12, 14], а также увеличивающийся со временем риск кровотечения и развития рака после применения прасугрела [12, 15]; несоответствие между приемлемыми показателями нефатального ИМ и инсульта и выраженной частотой сосудистой смерти с необычным отсроченным временем наступления предполагаемой пользы от тикагрелора в PLATO [13, 16].
Кроме того, оба исследования подверглись дополнительному критическому рассмотрению из-за стандартных стратегий вынесения решений, где выраженное предпочтение отдавалось препаратам нового поколения, а исходы исследований искусственным образом менялись с нейтральных на значимые [17, 18]. Наконец, эксперты из FDA США отреагировали на более высокую частоту досрочного прекращения приема препарата после терапии тикагрелором, что проигнорировали их европейские коллеги.
 Действительно, при составлении рекомендаций ЕКО было бы более рациональным опираться на анализы Европейского медицинского агентства по лекарственным средствам (European Medicines Agency, EMEA), однако мы не располагаем информацией о том, находятся ли эти подробные обзоры в широком доступе (www.ema.europa.eu). Напротив, отчеты FDA могут быть с легкостью бесплатно загружены с официального веб-сайта Управления (www.fda.gov).
Действительно, при составлении рекомендаций ЕКО было бы более рациональным опираться на анализы Европейского медицинского агентства по лекарственным средствам (European Medicines Agency, EMEA), однако мы не располагаем информацией о том, находятся ли эти подробные обзоры в широком доступе (www.ema.europa.eu). Напротив, отчеты FDA могут быть с легкостью бесплатно загружены с официального веб-сайта Управления (www.fda.gov).
Возможно, нет необходимости анализировать опубликованные государственным органом США доказательства для всех без исключения клинических случаев, подпадающих под изменение рекомендаций. Тем не менее в случае, когда более новые антитромботические препараты (прасугрел и тикагрелор) рекомендуются как имеющие превосходство над клопидогрелом, обязательной целью рабочей группы должно быть стремление охватить данные помимо тех, что упомянуты в первичных публикациях, и упорно искать более непредвзятые свидетельства, включая факты, изложенные только в государственных материалах. Это особенно справедливо в отношении рекомендаций по тикагрелору, поскольку многие страны, участвовавшие в исследовании PLATO, проходили аудит непосредственно со стороны организатора исследования (self-monitored by study sponsor) [16]. Вызывает озабоченность тот факт, что благоприятные исходы при терапии тикагрелором по сравнению с клопидогрелом в тех учреждениях и странах, которые контролировались организатором исследования, не согласуются с отрицательными результатами по тикагрелору по сравнению с клопидогрелом в нескольких странах, таких как США, или нейтральными результатами в других странах, таких как Российская Федерация, где контроль осуществлялся сторонними исследовательскими организациями, работающими по контракту [16].
Несмотря на то что при составлении рекомендаций рабочая группа ЕКО оставила без должного внимания факты, отраженные в обзорах государственных органов США, существуют многочисленные рандомизированные исследования, косвенно подвергающие сомнению концепцию о том, что длительное применение более сильнодействующих антитромботических лекарственных средств приводит к лучшим сосудистым клиническим исходам. Действительно, недавно полученные результаты исследований GRAVITAS [19], TRIGGER-PCI [20], ARCTIC [21] и ACCOUST [22] не показали такой взаимосвязи, также не подтвердив чрезмерно оптимистичные рекомендации ЕКО по ОКС.
ИМ с подъемом ST
 С технической точки зрения в рекомендациях ЕКО преимущество прасугрела и тикагрелора (Класс I, УД: B для обоих препаратов) над клопидогрелом (Класс I, УД: С) утверждалось [2] на основании малочисленных когорт с ИМпST и ретроспективных (post-hoc) вторичных анализов TRITON [6] и PLATO [7], предполагающих преимущество обоих новых препаратов в снижении летальности. Ради объективности следует отметить, что не существует специально разработанных исследований прасугрела или тикагрелора в условиях ИМ либо ИМпST в отличие от клопидогрела, по которому в нашем распоряжении имеется крупнейшее за всю историю исследование с участием 45 852 пациентов с ИМ, а именно исследование COMMIT.
С технической точки зрения в рекомендациях ЕКО преимущество прасугрела и тикагрелора (Класс I, УД: B для обоих препаратов) над клопидогрелом (Класс I, УД: С) утверждалось [2] на основании малочисленных когорт с ИМпST и ретроспективных (post-hoc) вторичных анализов TRITON [6] и PLATO [7], предполагающих преимущество обоих новых препаратов в снижении летальности. Ради объективности следует отметить, что не существует специально разработанных исследований прасугрела или тикагрелора в условиях ИМ либо ИМпST в отличие от клопидогрела, по которому в нашем распоряжении имеется крупнейшее за всю историю исследование с участием 45 852 пациентов с ИМ, а именно исследование COMMIT.
В нем обнаружено весьма значительное преимущество в снижении летальности (спасшее к 28-му дню наблюдения 119 жизней) при использовании клопидогрела в дозе 75 мг (без нагрузочной дозы), добавленной к фибринолитическому препарату при сочетанном применении невысоких доз ацетилсалициловой кислоты (АСК) при ведении пациентов с острым ИМ [10] (рис. 1).
Кроме того, обсуждаемые Рекомендации ЕКО не ограничиваются условиями чрескожного коронарного вмешательства (ЧКВ) и предлагают рекомендации по фибринолитическим препаратам (таблица 14 Рекомендаций ЕКО) в дополнение к специальному разделу (3.5.4), посвященному тромболитической терапии [2]. Исследование COMMIT было специально разработано для пациентов с ИМ, при этом более чем у 86% пациентов критерием включения в исследование был ИМпST.
Однако данные рекомендации понизили ценность этого исследования, а клопидогрел рассматривался при анализе исключительно как дополнение к фибринолизу; при этом не признавалось то влияние, которое оказало исследование COMMIT на установление общей пользы от применения клопидогрела в лечении пациентов с острым ИМ. Все прочие недавно проведенные исследования с использованием клопидогрела, тикагрелора, особенно прасугрела, включают малочисленную когорту пациентов с ИМпST, как показано в табл. 4.

Неясно, почему результаты исследования CURRENT должным образом повлияли на более ранние рекомендации ЕКО по ИМбпST [1], определяя приоритетность доказательств в зависимости от нагрузочной дозы клопидогрела, тогда как данные CURRENT были проигнорированы в более поздних рекомендациях по ИМпST [2], особенно с учетом того, что когорта пациентов с ИМпST в исследовании CURRENT была крупнее, чем в TRITON (более подробную информацию см. в табл. 1, 2). Более того, двойная доза клопидогрела в исследовании CURRENT ассоциировалась со снижением частоты развития первичного исхода с 5,2 до 4,7% и уменьшением относительного риска (ОР=0,9) по сравнению со стандартным режимом у 7327 пациентов с ИМпST [11].
Сравнение вторичных публикаций по смертности от ИМпST в исследовании TRITON [23] или PLATO [24] и сопоставление их с имеющимися в наличии данными FDA [12, 13], по сути, поднимает больше вопросов, чем дает окончательных заключений (подробную информацию см. на рис. 2—4). Во-первых, полностью различаются методики выбора времени для определения пользы от прасугрела (немедленная; см. рис. 2) и тикагрелора (отсроченная; см. рис. 3).
В исследовании TRITON польза является ранней и ожидаемо наблюдается меньше, чем период последующего контроля больных, воспроизводя результаты исследований ISIS-2 [25] и OASIS-6 [26]. Необходимо также отметить исчезновение преимущества прасугрела в показателях смертности ближе к концу периода последующего наблюдения, когда в TRITON появились признаки отсроченного кровотечения и рака [12].
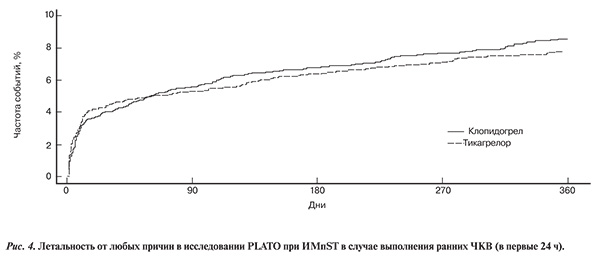
 Напротив, в исследовании PLATO не регистрировалось преимущества в когорте раннего ЧКВ (ранее 24 ч, см. рис. 4). На самом деле пациенты, получавшие тикагрелор, чувствовали себя хуже, представляя собой «парадокс летальности на тикагрелоре при раннем ЧКВ», как указано в документах [13].
Напротив, в исследовании PLATO не регистрировалось преимущества в когорте раннего ЧКВ (ранее 24 ч, см. рис. 4). На самом деле пациенты, получавшие тикагрелор, чувствовали себя хуже, представляя собой «парадокс летальности на тикагрелоре при раннем ЧКВ», как указано в документах [13].
Возможно, тикагрелор является высокоэффективным препаратом, однако летальность при ИМпST в исследовании PLATO оказалась выше, чем в исследовании TRITON, и не объясняет этот сомнительный феномен. В действительности, неясно, почему пациенты с ИМпST в когорте клопидогрела в исследовании PLATO умирали на 30% чаще (6,1% против 4,31%), чем подобные им больные в исследовании TRITON, несмотря на интенсивную предварительную нагрузку клопидогрелом в исследовании PLATO (46% больных получили предзагрузку до рандомизации), тогда как это было специально запрещено в исследовании TRITON c прасугрелом [12, 13, 23, 24]. Кроме того, трудно понять, почему тикагрелор после регистрации промотируется как препарат «спасающий жизнь», если он вызвал на 34% больше смертей (4,9% против 3,28%), чем прасугрел в таких же когортах пациентов с ИМпST [23, 24]. К сожалению, мы не имеем прямых сравнений тикагрелора и прасугрела, однако значительное сходство в категории больных и в планах их ведения в обсуждаемых исследованиях оставляет нам право на подобные вопросы.
НС/ИМбпST
В отличие от рекомендаций, представленных в США, действующие рекомендации ЕКО дают прасугрелу и тикагрелору статус преимущества над клопидогрелом [1]. Несмотря на одинаковый класс и уровень доказательности (Класс I, УД: B), клопидогрел следует использовать с нагрузочной дозой 300 мг (Класс I, УД: A) либо 600 мг (Класс I, УД: B) только в случае невозможности применения тикагрелора и прасугрела [1]. Эта клиническая рекомендация также основана на подгруппе единственного исследования с каждым из новых препаратов.
Касательно когорты с ИМбпST в исследовании TRITON ниже представлены соответствующие кривые смертности (рис. 5), согласно документам FDA [12]. Учитывая расхождения в определении ИМ (отмеченные FDA) и спорные методики вынесения решений, небольшое, но стабильное преимущество клопидогрела над прасугрелом в показателях смертности у пациентов TRITON с ИМбпST служит явным сигналом, является убедительным и не подкрепляет текущие рекомендации ЕКО.
По поводу тикагрелора в табл. 5 приводятся мнения клинических рецензентов FDA (рецензии относятся ко всем группам больных, в том числе к подгруппам НС/ИМбпST).
Таким образом, через 2 года от начала рассмотрения документов FDA тикагрелор получил в 2011 г. разрешение для клинического использования в США с обязательствами компании-производителя провести новое исследование, включающее значительную долю пациентов — жителей США, исключив в новом исследовании влияние высоких доз ацетилсалициловой кислоты, как представленной причины «неуспеха» тикагрелора на территории США.

К слову, за пределами США в настоящее время проводится проспективное рандомизированное двойное слепое исследование III фазы, в которое включены не менее 800 пациентов из Японии и Азии, чтобы оценить безопасность и эффективность тикагрелора при ОКС [27]. Пациенты должны быть рандомизированы к тикагрелору в дозе 90 мг 2 раза в сутки либо к клопидогрелу в дозе 75 мг в сутки в дополнение к АСК. Первичные исходы в исследовании — время до первого крупного кровотечения до 12 мес и время до первой регистрации совокупной конечной точки, состоящей из смерти от сосудистых причин, ИМ или инсульта до 12 мес. Это исследование должно было завершиться в июле 2012 г., однако результаты не были опубликованы до апреля 2013 г.
Еще одно краткосрочное исследование по оценке тикагрелора (A 30 Day Study to Evaluate Efficacy and Safety of Pre-hospital vs In-hospital Initiation of Ticagrelor Therapy in STEMI Patients Planned for Percutaneous Coronary Intervention (PCI) (ATLANTIC)) должно завершиться в августе 2013 г. [28]. Это проспективное рандомизированное двойное слепое исследование IV фазы должно включить не менее 1770 пациентов, в том числе на территории США, чтобы определить эффективность и безопасность догоспитального начала приема тикагрелора по сравнению со стационарным у больных ИМпST, для которых запланирована инвазивная тактика лечения, включающая ЧКВ. Пациенты получат тикагрелор в нагрузочной дозе 180 мг либо до поступления в стационар, либо уже в стационаре с последующей поддерживающей дозой 90 мг 2 раза в сутки в течение 30 дней. Первичными критериями являются достижение кровотока степени TIMI III в инфаркт-связанной артерии при исходной ангиографии и снижение сегмента ST не менее 70% до начала чрескожного вмешательства.
Заключение
В отличие от рекомендаций, вышедших в США [3—5], текущие рекомендации ЕКО по ОКС [1, 2] в части, касающейся предпочтительного применения новейших пероральных антитромботических препаратов (тикагрелора и прасугрела), а не клопидогрела, являются чрезмерно оптимистичными и не вполне основанными на доказательствах. Рекомендации имеют бóльший вес, когда им следуют большинство врачей. Если же основная часть профессионального сообщества игнорирует рекомендации, это обычно означает либо то, что они ошибочны, поскольку не отражают факты, либо то, что на принятие решений оказывают воздействие другие условия «из реальной жизни».

Однако ежедневная клиническая практика подсказывает, что клопидогрел по-прежнему остается незыблемым краеугольным камнем антитромботического лечения больных с острыми коронарными синдромами, занимая более 90% рынка пероральных антитромботических стратегий, что заставляет усомниться в практической ценности и репутации рекомендаций ЕКО. Важно, что несмотря на попытки маркетинга, ситуация не изменится без еще одного крупного, четко определенного исследования.
Особая благодарность д-ру С. Стейнхублу (CREDO) и д-ру Д. Бхатту (CHARISMA) за разъяснение исследовательских данных.



