Фибрилляция предсердий (ФП) — самое распространенное нарушение ритма сердца среди населения [1]. Она служит одним из наиболее важных факторов риска смерти от инсульта и других сердечно-сосудистых катастроф. Помимо влияния на прогноз пароксизмальная ФП значительно снижает качество жизни не только во время пароксизма, но и в период между приступами.
Исследования как иностранных, так и отечественных авторов [2] выявили такой феномен, как утрата сократительной функции предсердий непосредственно после восстановления синусового ритма у пациентов с ФП. При этом сократительная функция предсердий у пациентов с пароксизмальной формой ФП на фоне синусового остается малоизученной.
Целью настоящего исследования было изучение сократительной функции предсердий у больных с пароксизмальной формой ФП по сравнению с пациентами без наджелудочковых аритмий.
Материал и методы
Работа спланирована как клиническое исследование случай—контроль с последовательным включением пациентов. Из 70 больных, включенных в исследование, 35, с артериальной гипертензией (АГ) и пароксизмальной формой ФП, были включены в группу ФП; 35 больных с АГ, сопоставимых по возрасту и полу, но без указаний на наличие нарушений ритма, были объединены в группу контроля.
Все пациенты получали лечение антигипертензивными препаратами по поводу АГ, имели клиническое поражение органов-мишеней. Подъемы артериального давления (АД) были неоднократно зафиксированы как при непосредственном измерении, так и при проведении суточного мониторирования АД (СМАД).
Диагноз «ФП, пароксизмальная форма» устанавливали по данным анализа электрокардиограммы (ЭКГ) при наличии доказательств того, что пароксизмы продолжались не более 48 ч. Больных с персистирующей формой ФП исключали из исследования.
ФП и другие нарушения ритма были исключены у пациентов в группе контроля как по данным анамнеза, так и с помощью холтеровского мониторирования (ХМ) ЭКГ.
Критериями включения в группу ФП служили пароксизмальная форма ФП, зарегистрированные на ЭКГ пароксизмы длительностью не более 48 ч; подтвержденная АГ (по данным СМАД или на основании длительного приема антигипертензивных препаратов).
Критериями включения в контрольную группу служили подтвержденная АГ (по данным СМАД или на основании длительного приема антигипертензивных препаратов); отсутствие указаний на наличие нарушений ритма, включая отсутствие жалоб на частые сердцебиения или перебои в работе сердца, отсутствие нарушений ритма при анализе ЭКГ в 12 отведениях и ХМ ЭКГ.
В группе ФП анализировали клинические данные у 15 (42,9%) мужчин и 20 (57,1%) женщин, в контрольной группе — у 16 (45,7%) и 19 (54,3%) соответственно. Средний возраст пациентов в группе ФП на момент включения в исследование составил 62,2±10,2 года, в контрольной группе — 60,7±11,2 года (p>0,05). Сопутствующая патология отражена в табл. 1.
Развитие пароксизма ФП не сопровождалось клинической симптоматикой у 5 (14,3%) больных (I класс по EHRA — European Heart Rhythm Association), II класс по EHRA был диагностирован у 7 (20%) пациентов. У 15 (42,9%) больных отмечался III класс по EHRA. К IV классу были отнесены 8 (22,9%) пациентов, у которых главными жалобами на фоне пароксизма выступали одышка и резкая слабость.
В ходе настоящей работы проводился опрос всех больных с ФП относительно срока давности последнего пароксизма ФП. У 8 (22,9%) больных последний приступ ФП отмечался в течение 1—3 дней до момента обследования, у 12 (34,3%) — от 4 до 7 дней, у 9 (25,7%) пациентов — от 1 до 2 нед до момента госпитализации, у 3 (8,6%) лиц — около 1 мес назад.

Основным методом, с помощью которого проводилась оценка сократительной функции предсердий, служила эхокардиография (ЭхоКГ). Ее проводили на фоне синусового ритма; исследование включало следующее: 1) стандартные измерения (определение размеров полостей сердца, оценку систолической и диастолической функции левого желудочка — ЛЖ); 2) оценку сократительной функции предсердий в В-режиме с помощью импульсно-волнового, тканевого допплеровского исследования, а также оценку времени проведения по предсердиям; 3) оценку объемной фракции фиброза в предсердиях и желудочках с использованием программного обеспечения Image J (NIH, 2009).
Кроме того, анализировали следующие показатели:
- скорости пиков трансмитрального диастолического потока;
- пики S, D и Ar кровотока в легочных венах;
- отношение Е/Е′;
- объем левого предсердия (ЛП) в систолу и диастолу по методу дисков из апикальной четырехкамерной позиции с последующим расчетом фракции выброса (ФВ) ЛП;
- скорость пика А трансмитрального диастолического кровотока, скорость, интеграл скорость—время (VTI) и продолжительность пиков A′ фиброзных колец трикуспидального и митрального клапанов;
- время проведения электрического импульса по ЛП (измеряли как время от начала зубца Р до начала систолы предсердий — пика А′ при синхронной записи эхокардио-граммы и ЭКГ).
Фракцию фиброза миокарда оценивали по следующей методике. Сохраняли эхокардиографические изображения, записанные в диастолу из парастернальной позиции по длинной оси и апикальной четырехкамерной позиции, на которых отчетливо были видны перикард, межжелудочковая перегородка (МЖП), полость и задняя стенка ЛЖ, ЛП. При записи всех изображений, чтобы избежать последующих ошибок в расчетах, использовали один и тот же режим ЭхоКГ — стандартные настройки аппарата Acuson «Cardiac Difficult» (серошкальные изображения, частота датчика 3,5 МГц) с автоматической подстройкой яркости.
Изображения записывали в формате jpeg и переносили для последующего анализа в компьютер, где анализировали с помощью программного обеспечения Image J 1.4 (NIH, 2009), созданного для количественного и качественного анализа медицинских и биологических изображений. Путем автоматической настройки порога по методу максимальной энтропии изображения переводили в однобитовые. На однобитовых изображениях самым «ярким» оставался перикард ввиду его наибольшей эхогенности и максимального содержания соединительнотканных волокон. Фракцию фиброза в перикарде принимали за 100%. Напротив, заполненная кровью полость ЛЖ оставалась «черной», фракцию фиброза в ней принимали за 0.
 На этом фоне в толще МЖП и межпредсердной перегородки (МПП) отмечалось наличие ярких, гиперэхогенных включений, наиболее вероятно, обусловленных фиброзом миокарда.
На этом фоне в толще МЖП и межпредсердной перегородки (МПП) отмечалось наличие ярких, гиперэхогенных включений, наиболее вероятно, обусловленных фиброзом миокарда.
С целью оценки объемной фракции фиброза в предсердиях была разработана оригинальная методика, основанная на использовании эхокардиографических изображений МПП из апикальной четырехкамерной позиции. По сути МПП — единственная структура, представленная четко ограниченной тканью собственно предсердий. В отношении других стенок предсердий с применением ЭхоКГ практически невозможно отграничить их от соседних анатомических образований (перикарда, ЛЖ, клапанов), что резко снижает точность оценки. При оценке фракции фиброза в предсердиях за максимально эхогенное образование принимали створки митрального клапана (в связи с неудовлетворительной визуализацией перикарда из четырехкамерной позиции).
С помощью программы Image J проводили количественную оценку фракции «100% ярких» пикселей в толще МЖП (базальный отдел) и МПП (вся перегородка), процентное отношение которых к площади перегородок и принимали за показатель фракции фиброза.
Анализ данных проводили с использованием программы Statistica 7.0, были вычислены описательные статистики, критерий χ2 и корреляции между переменными, построены таблицы сопряженности. Сравнение выборок было реализовано методами непараметрической статистики, дисперсионного анализа, для сравнения независимых переменных использовались критерии χ2, Манна—Уитни и Стьюдента, если распределение величин отвечало закону нормального распределения. Для определения того, является ли распределение нормальным, использовали критерий Колмогорова—Смирнова. За уровень значимости статистических показателей принято р<0,05. Данные в таблицах и в тексте представлены как среднее значение ± стандартное отклонение, распространенность отдельных нарушений показана в виде абсолютного числа и % пациентов в группе.
Результаты
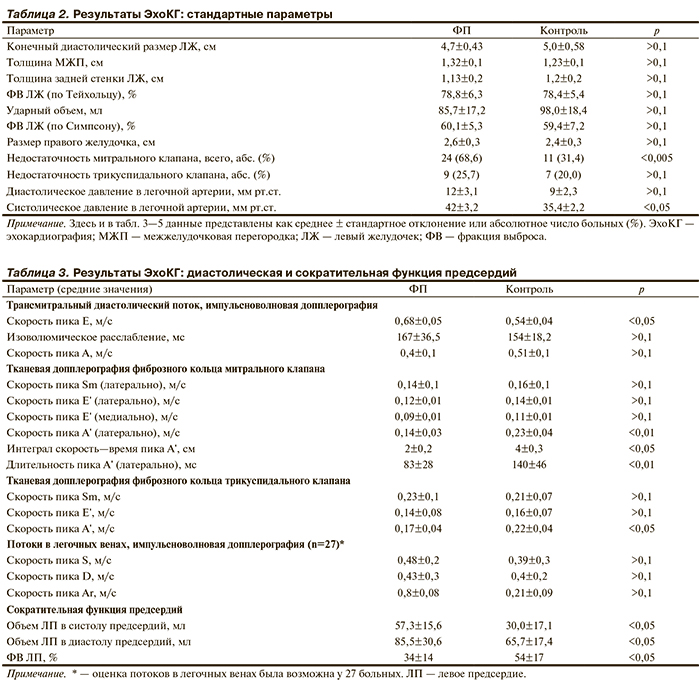
Результаты оценки стандартных параметров ЭхоКГ приведены в табл. 2.
В группе ФП по сравнению с группой контроля отмечалась выраженная дилатация ЛП: средний переднезадний размер ЛП составлял 4,7±0,4 см, верхненижний — 6,1±0,6 см, медиально-латеральный — 5,2±0,4 см; в группе контроля соответствующие размеры достигали 3,8±0,4; 5,7±0,5 и 4,4±0,5 см.
Средний объем ЛП в группе ФП достигал 85,5±30,6 мл, тогда как в группе контроля — 65,7±17,4 мл (р<0,05; при норме менее 45 мл). В отношении размеров правого предсердия (ПП) наблюдалась сходная тенденция к дилатации в группе ФП (средние размеры 5,8±3,7 см против 5,3±3,3 см в контрольной группе).
Важной представлялась оценка сократительной функции предсердий в подгруппе с относительно небольшими объемами ЛП (менее 55 мл), в которую распределились 7 (20%) больных.
Сократительная функция предсердий тесно связана с диастолической функцией желудочков, поэтому результаты оценки этих параметров представлены в единой табл. 3.
У больных с ФП отмечалось выраженное снижение сократительной функции предсердий на фоне синусового ритма, как по данным оценки ФВ ЛП (В-режим, метод дисков), так и с использованием потокового и тканевого допплеровского исследования.
ФВ ЛП составила в контрольной группе 54±17%, а в группе ФП — 34±14% (р<0,05; при нижней границе нормы 45%). Сниженная сократительная функция ЛП имелась у 27 (77,1%) больных с ФП. В подгруппе больных с объемом ЛП менее 55 мл (n=7) снижение ФВ ЛП отмечалось у 3 пациентов.
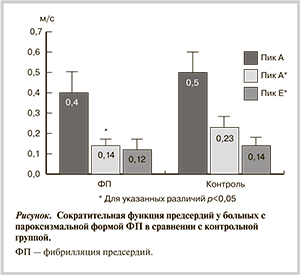
При оценке трансмитрального диастолического потока сократительную функцию ЛП отражает скорость пика А. В нашем исследовании в группе больных с ФП этот параметр оказался несколько меньше (0,4±0,1 м/с против 0,51±0,1 м/с), однако различия не достигли статистической значимости.
По данным анализа более чувствительных тканевых допплерографических параметров, в группе ФП выявлялось выраженное снижение сократительной функции как ЛП, так и ПП. Скорость пика A′ — пика тканевого допплеровского исследования, соответствующего пику А и отражающего движение стенки предсердий во время их систолы, оказалась у пациентов с ФП достоверно более низкой, чем в группе контроля. Скорость пика А′, оцениваемого латерально на уровне фиброзного кольца митрального клапана («прицельная» оценка сократительной функции ЛП), составила в группе контроля 0,23±0,04 м/с, тогда как в группе ФП — 0,14±0,03 м/с, р<0,01 (см. рисунок). У больных с ФП отмечается выраженное статистически значимое снижение скорости пика А′, в то время как пик А снижен лишь незначительно и статистически незначимо. Для сравнения на рисунке также приведен пик Е′ (нет различий).
Продолжительность и интеграл VTI пика А′ в группе ФП оказались достоверно более низкими, чем в группе контроля (83±28 мс против 140±46 мс, р<0,01; и 2±0,2 см против 4±0,3 см, p<0,05 соответственно), что отражало снижение сократительной функции ЛП. Можно обсуждать вопрос о том, что систола предсердий у больных с пароксизмальной формой ФП оказывается не только слабее, но и короче, чем в контрольной группе.
Сократительная функция ПП оказалась нарушенной в меньшей мере: при оценке на уровне фиброзного кольца трикуспидального клапана скорость пика А′ составила в группе контроля 0,22±0,04 м/с, а в группе ФП — 0,17±0,04 (p=0,04).
Помимо изучения сократительной функции предсердий важной практической задачей представляется оценка давления в полости ЛП, с повышением которого связана одышка. Проблема оценки давления в полости ЛП с помощью ЭхоКГ в некоторой степени является обратной по отношению к проблеме точной оценки сократительной функции ЛП. C целью уменьшения влияния повышенного конечного диастолического давления в полости ЛЖ и снижения сократительной функции ЛП в ходе работы был впервые предпринят анализ нового параметра А/А′. В группе ФП отмечено достоверное увеличение параметра А/А′ до 2,7±0,2 (в группе контроля — 1,9±0,1; р<0,01), что можно трактовать как повышение давления в полости ЛП, не связанное со снижением его сократительной функции.
Наиболее высокое отношение А/А′ (в среднем 4,3) отмечалось у больных с пресистолическим ритмом галопа S4 (n=11), у которых даже при наличии атриомегалии и сниженной сократительной функции ЛП сохранялся высокий пик А трансмитрального диастолического потока (в среднем пик A=0,55 м/с). Эти данные раскрывают гемодинамический механизм формирования VI тона.
Зависимость сократительной функции ЛП от степени атриомегалии. При проведении корреляционного анализа выявлена статистически значимая отрицательная корреляция между объемом ЛП и такими показателями, как ФВ ЛП (r=–0,39; p<0,05) и величина пика А′ (r=–0,47; p<0,05). Наиболее четко эта зависимость прослеживалась у пациентов с объемом ЛП более 65 мл. Эти данные свидетельствуют в пользу того, что снижение сократительной функции предсердий идет одновременно с нарастанием степени атриомегалии.
Сократительная функция ЛП у пациентов с ФП без выраженной дилатации ЛП. Анализ сократительной функции ЛП с применением тканевого допплеровского исследования у пациентов с ФП с объемом ЛП менее 55 мл (n=7) продемонстрировал ее снижение, сопоставимое с таковым у пациентов с дилатацией ЛП. Средние значения пика А′ в этой подгруппе составили 0,16±0,02 м/с, А/А′ — 2,5±0,2 (р>0,1 при сравнении со значениями в подгруппе с дилатацией предсердий). Таким образом, в отношении оценки сократительной функции предсердий показатели тканевого допплеровского исследования являются более чувствительными, чем оценка ФВ ЛП.
Связь продолжительности пароксизма ФП и степени снижения сократительной функции ЛП. Большинство включенных в исследование пациентов отмечали развитие пароксизма в течение последних 2 нед до момента госпитализации. При проведении корреляционного анализа статистически значимой зависимости между снижением сократительной функции ЛП (с учетом как ФВ ЛП, так и допплерографических показателей) и длительностью пароксизма выявлено не было (r=–0,22; p>0,1).
Оценка диастолической функции ЛЖ и ее связь с сократительной функцией ЛП. В отношении диастолической функции единственным статистически значимым различием между группами была скорость пика Е трансмитрального диастолического потока, которая оказалась несколько выше в группе ФП (0,68±0,05 м/с против 0,54±0,04 м/с; р<0,05), что не оказало достоверного влияния на отношение Е/Е′. По всей видимости, у больных с ФП отмечается компенсаторное увеличение скорости пика Е на фоне снижения пика А для обеспечения достаточного наполнения ЛЖ в диастолу.
Следует отметить несколько важных особенностей оценки диастолической функции в исследуемой популяции. Во-первых, скорости пика Е′ (и, соответственно, показателя Е/Е′), измеренные на уровне фиброзного кольца латерально, были достоверно более высокими (0,14—0,16 м/с), чем измеренные медиально (0,09—0,11 м/с). Во-вторых, скорости пиков E′ и A′, измеренных на уровне фиброзного кольца трикуспидального клапана, были более высокими, что может свидетельствовать о большей сохранности функции ПП и меньшей степени диастолической дисфункции правого желудочка. В ходе работы у 2 больных в группе ФП и 3 в контрольной группе на уровне фиброзного кольца трикуспидального клапана мы регистрировали «гигантские» пики E′, превышающие по скорости 0,4 м/с, трактовка которых затруднена. В-третьих, в ходе работы выявлена тесная положительная корреляция (r=0,6; р<0,05) между массой миокарда ЛЖ и показателем E/E′, что позволяло предположить возможность механического, не связанного с истинной диастолической дисфункцией, влияния гипертрофии ЛЖ на рост показателя E/E′. В-четвертых, в группе ФП отмечалось статистически значимое повышение Е/А (1,9±0,2 против 1,6±0,1; р<0,05), вероятно, вследствие уменьшения скорости пика А ввиду снижения сократительной функции ЛП, а не истинного ухудшения диастолической функции ЛЖ.
Общая характеристика диастолической функции ЛЖ представлена в табл. 4.
Неинвазивная оценка времени проведения электрического импульса по предсердиям. В ходе исследования осуществлялся расчет скорости проведения электрического импульса по предсердиям как интервал от зубца Р ЭКГ до максимума предсердного пика А′ тканевого допплеровского исследования (при параллельной записи ЭКГ и импульсноволнового тканевого допплеровского исследования латеральной порции фиброзного кольца митрального клапана).
В группе ФП отмечалось выраженное достоверное снижение скорости проведения электрического импульса по предсердиям до 262±51,4 мс; в группе контроля этот показатель составлял 154±43,9 мс (р=0,04).
Пациенты с признаками замедления проведения по предсердиям на ЭКГ (n=9) имели достоверно более низкую скорость проведения возбуждения и по данным совмещенной записи тканевой допплерографии, и ЭКГ. Средняя скорость проведения электрического импульса в этой подгруппе составила 289±21 мс.
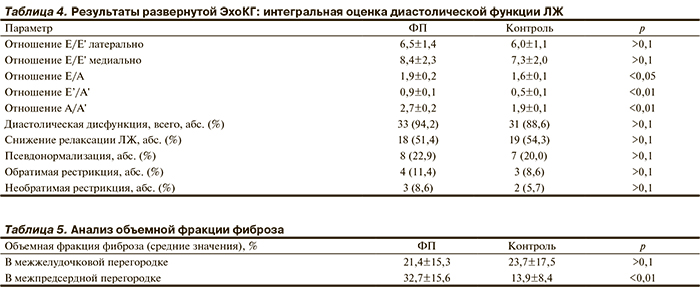
Оценка объемной фракции фиброза в предсердиях и желудочках. В ходе исследования при анализе серошкальных изображений ЭхоКГ в В-режиме по оригинальной методике был проведен расчет объемной фракции фиброза в МПП и МЖП. Результаты приведены в табл. 5.
По показателю объемной фракции фиброза в МЖП группы достоверно не различались: она составила 21,4±15,3% в группе ФП и 23,7±17,5% в контрольной группе. В группе ФП отмечалось выраженное достоверное увеличение фракции фиброза в МПП до 32,7±15,6% по сравнению с 13,9±8,4% в группе контроля (р<0,05). Фракция фиброза у больных в группе ФП положительно коррелировала с длительностью анамнеза ФП (r=0,36; p<0,05), анамнеза артериальной гипертензии (r=0,41; p<0,05) и систолическим артериальным давлением (r=0,32; p<0,05).
Обсуждение
Атриомегалия играет одну из ведущих ролей в патогенезе ФП. После достижения критических размеров ЛП (4,3×4,4×4,7 см) шансы на восстановление синусового ритма резко снижаются [3]. В нашем исследовании выявлено значительное увеличение размеров ЛП, в первую очередь переднезаднего размера, в группе ФП (4,7 см против 3,8 см в группе контроля).
Разброс объемов ЛП в группе ФП был большим: у большинства пациентов объем ЛП колебался от 66 до 100 мл, но при этом выделялась группа лиц (n=7) с объемом ЛП менее 55 мл.
Допплеровское исследование трансмитрального диастолического потока также активно используется с целью определения сократительной функции предсердий. В данном случае проводится оценка скорости пика А. Европейские и российские авторы продемонстрировали снижение скорости пика А у пациентов с ФП, в том числе после восстановления синусового ритма. Здесь необходимо выделить несколько опорных моментов:
- при снижении сократительной функции ЛП скорость пика А снижается;
- при начальной степени диастолической дисфункции скорость пика Е снижается, а скорость пика А компенсаторно возрастает;
- прогрессирование хронической сердечной недостаточности с сохраненной ФВ ведет к повышению давления в ЛП с его дилатацией, что обусловливает снижение скорости пика А (фаза псевдонормализации);
- последующее нарастание степени диастолической дисфункции вплоть до рестрикции вновь будет приводить к росту скорости пика А.
Таким образом, использование такого маркера сократительной функции предсердий, как скорость волны А, ограничено ввиду влияния на него не только силы сокращения ЛП, но и диастолической функции ЛЖ. Другими словами, в случае одновременно сниженной сократительной функции ЛП и мягкой диастолической дисфункции скорость пика А может оставаться нормальной. Возможно, в связи с этим в нашей работе не получено статистически значимых различий скорости пика А между исследуемыми группами.
В ходе исследования отмечено, что в группе больных с ФП и пресистолическим галопом сохраняется высокая скорость пика А (в среднем 0,55 м/с), несмотря на наличие атриомегалии и выраженное снижение сократительной функции предсердий по данным других параметров. Это может свидетельствовать о значительном повышении давления в полости ЛП, приводящем к формированию выраженного градиента давлений между ЛП и ЛЖ. По всей видимости, именно благодаря такому градиенту создается аускультативный феномен пресистолического ритма галопа.
Исследование с использованием тканевого допплеровского метода «проливает свет» и на формирование протодиастолического галопа: у всех 4 пациентов с тоном S3, включенных в нашу работу, отмечалось снижение систолического пика Sm и появление раннего систолического пика, предшествующего Sm, который может быть ответственен за аускультативный феномен S3.
Оценка диастолической функции у больных с пароксизмальной формой ФП представляет собой непростую задачу. С одной стороны, у пациентов этой категории ожидаемо относительное повышение пика Е (при снижении «предсердного» пика А) при относительном повышении пика Е′ (и при параллельном снижении пика А′). С другой стороны, повышение пиков А и А′, которое обычно трактуется как ухудшение диастолической функции (при росте давления в ЛП в отсутствие его декомпенсации) у пациентов с ФП, может свидетельствовать об улучшении сократительной функции ЛП.
Низкая «надежность» такого показателя сократительной функции предсердий, как скорость пика А, во многом связана с тем, что он отражает градиент давления между предсердием и желудочком во время систолы предсердий [4], а не истинную силу сокращения предсердия. Например, «мощное» сокращение предсердия при изначально высоком конечном диастолическом давлении в полости ЛЖ будет приводить к «низкому» пику А, и наоборот. Показатели тканевого допплеровского исследования, отражающие «истинную» скорость движения стенок сердца в систолу и диастолу, лишены этих недостатков. Наиболее часто используемый на практике показатель тканевого допплеровского исследования — пик Е′, его измерение и расчет соотношения Е/Е′ дают исключительно ценную информацию о повышении конечного диастолического давления в ЛЖ.
Скорость пика А′ тканевого допплеровского исследования может быть использована в качестве надежного маркера сократительной функции предсердий [5], при этом измерение пика А′ на уровне фиброзного кольца митрального клапана позволяет судить о силе сокращения ЛП, а измерение этого пика на уровне фиброзного кольца трикуспидального клапана — о функции ПП [6].
Проведенное нами исследование показало выраженное снижение скорости пика А′ у пациентов с ФП, измеренной как латерально на уровне фиброзного кольца митрального клапана – до 0,14 м/с, так и на уровне фиброзного кольца трикуспидального клапана — до 0,17 м/с. В группе контроля скорости пика А′ составляли соответственно 0,23 и 0,22 м/с, что отвечает нормальным значениям. Сократительная функция ЛП по данным этого теста оказалась нарушенной в значительно большей степени, чем функция ПП. Эти результаты хорошо соотносятся с находками других авторов. Необходимо отметить, что в работах, изучавших темпы восстановления сократительной функции предсердий после кардиоверсии, показано еще более выраженное снижение сократительной функции ЛП, особенно в области задней стенки (скорости сокращения 0,02—0,04 м/с).
В ходе данного исследования помимо скорости пика А′ мы проанализировали другие его характеристики: продолжительность и интеграл VTI . Эти параметры, имеющие, по нашему мнению, большое значение, исключительно редко анализируются даже в научных работах. В нашем исследовании у пациентов с ФП показано значительное снижение как VTI (в 2 раза), так и длительности пика А′ (в 1,7 раза), что также отражает степень снижения сократительной функции. Большая амплитуда снижения этих показателей по сравнению со скоростью пика А′ может быть использована для наблюдения за пациентами в динамике.
C целью снятия влияния снижения сократительной функции ЛП на повышение давления в полостях сердца мы предложили использовать новый параметр А/А′, который представляется более адекватным для этой цели с позиции гемодинамики.
В группе ФП отмечено достоверное увеличение А/А′ до 2,7±0,2, при этом в группе контроля это отношение составило 1,9±0,1 (р<0,01). Данные изменения, по всей видимости, демонстрируют некоторое повышение давления в полости ЛП, не связанное со снижением его сократительной функции. Наиболее высоким отношение А/А′ оказалось у пациентов с пресистолическим ритмом галопа (4,3), что свидетельствует в пользу повышения в этой группе давления в полости ЛП.
В рамках настоящей работы мы соотнесли степень дилатации ЛП с нарушением его сократительной функции, что позволило выявить J-образную зависимость между этими показателями. Следует отметить, что у пациентов без атриомегалии с объемом ЛП менее 55 мл при оценке показателей тканевого допплеровского исследования отмечалось снижение сократительной функции ЛП, сравнимое с таковым у пациентов с умеренно выраженной атриомегалией. Наиболее сохранной сократительная функция была у пациентов с объемами ЛП в пределах 45—70 мл. При дальнейшем увеличении объема ЛП параллельно происходило и снижение сократительной функции ЛП, при этом степень атриомегалии лучше всего коррелировала со снижением скорости пика А′ (r=–0,47; p<0,05). В контрольной группе подобных зависимостей не наблюдалось. Таким образом, исследование сократительной функции предсердий позволяет выявить у пациентов с ФП без атриомегалии функциональные нарушения, которые могут вносить важный вклад в патогенез и клиническую симптоматику пароксизмальной формы ФП.
Во многих работах продемонстрировано, что сократительная функция предсердий непосредственно после восстановления синусового ритма с помощью кардиоверсии оказывается сниженной [7]. В связи с этим мы сделали предположение, что степень снижения сократительной функции предсердий будет коррелировать и с продолжительностью пароксизма ФП. Анализ включенных в наше исследование пациентов не выявил подобной зависимости, что может быть объяснено тремя основными факторами. Во-первых, у большинства включенных в исследование пациентов пароксизмы ФП возникали примерно в один промежуток времени — в течение последних 1—2 нед до поступления в клинику. Во-вторых, данные о давности пароксизма фиксировались со слов пациентов, которые не всегда могли указать точную дату развития последнего пароксизма, а кроме того, многие пароксизмы ФП протекают бессимптомно. В-третьих, в исследование не были включены больные, перенесшие процедуру кардиоверсии, у которых ожидаемо состояние «оглушенных» предсердий [8].
Замедление проведения электрического импульса по ткани предсердий, Z-образное проведение, причиной которых является фиброз миокарда предсердий, сегодня представляются в качестве основной патофизиологической основы ФП [9]. До недавнего времени оценка проведения электрического импульса по предсердиям была осуществима только с помощью инвазивных методов (электрофизиологическое исследование), а оценка объемной фракции фиброза в предсердиях — только на биологических моделях, при кардиохирургических вмешательствах или post mortem ввиду технической невозможности проведения биопсии предсердий.
В нашей работе анализ скорости проведения электрического импульса по предсердиям проводился по методике, подробно описанной выше. Ее суть состояла в оценке длительности интервала между появлением на ЭКГ зубца Р и началом систолы предсердий по данным тканевого допплеровского исследования (зубец А′). Указанный метод был протестирован в небольших проспективных исследованиях на популяции больных с ФП. Недавно в проспективном исследовании показано, что снижение скорости проведения по предсердиям более 165 мс увеличивает риск развития ФП [10]. В то же время в популяции больных с пароксизмальной формой ФП этот метод изучен недостаточно. В нашем исследовании продемонстрировано, что у пациентов с пароксизмальной формой ФП отмечается значительное снижение скорости проведения по предсердиям по сравнению с таковым в группе контроля (262±51,4 мс против 154±43,9 мс; р<0,05). Таким образом, средние значения у пациентов в группе ФП вплотную приближались к рубежу в 165 мс. В подгруппе пациентов с признаками замедления проведения по предсердиям на ЭКГ (n=9) продолжительность проведения импульса по предсердиям была наибольшей, в среднем 289±21 мс.
В ходе данной работы впервые, по нашим данным, был проведен анализ объемной фракции фиброза в МПП с помощью ЭхоКГ. Оценка фиброза в предсердиях ограничивалась трудностью дифференцировки ткани предсердий от лежащих рядом структур. Эта сложность была преодолена путем оценки фракции фиброза в МПП по оригинальной методике. Кроме того, одновременно осуществлялся анализ объемной фракции фиброза в МЖП. Результаты работы показали, что средняя объемная фракция фиброза в МЖП достоверно не различается в исследуемых группах (21,4% в группе ФП и 23,7% в контрольной группе), в то время как в МПП у больных с ФП наблюдается выраженное и статистически значимое увеличение объемной фракции фиброза примерно в 3 раза (32,7±15,6% против 13,9±8,4% в контрольной группе; р<0,01).
Объем фракции фиброза в МЖП, превышающий 20%, можно трактовать как аномальный. По всей видимости, наличие фиброза миокарда ЛЖ у наших пациентов связано с длительным анамнезом АГ.
Значительные различия между группами по объемной фракции фиброза в МПП, наиболее вероятно, объясняются именно наличием ФП. В последнее время появляется все больше работ, свидетельствующих о ключевой роли фиброза миокарда предсердий в течении ФП. В частности, недавно показано, что пациенты с выраженным фиброзом миокарда предсердий имеют более высокий риск повторных эпизодов ФП после процедуры радиочастотной абляции [11].
Заключение
У больных с пароксизмальной формой фибрилляции предсердий по сравнению с пациентами без наджелудочковых аритмий на фоне синусового ритма отмечается статистически значимое снижение сократительной функции предсердий, не зависящее от давности пароксизма фибрилляции предсердий. Исследование с применением тканевого допплеровского исследования фиброзных колец митрального и трикуспидального клапанов позволяет выявить группу пациентов с пароксизмальной формой фибрилляции предсердий без выраженной атриомегалии, но со значительным снижением сократительной функции предсердий. Нарастание степени атриомегалии у пациентов с пароксизмальной формой фибрилляции предсердий ассоциировано со снижением сократительной функции предсердий.
Показано, что объемная фракция фиброза в межпредсердной перегородке статистически значимо увеличена у пациентов с пароксизмальной формой фибрилляции предсердий при сходных показателях объемной фракции фиброза в межжелудочковой перегородке.



