Сеть Хиари выявляется в популяции в 2% случаев и представляет собой фиброзно-нитевидную структуру в виде сетки, которая прикрепляется к клапану нижней полой вены (евстахиев клапан) с одной стороны и к различным частям правого предсердия (ПП) — с другой [1]. Наряду с евстахиевым клапаном сеть Хиари может прикрепляться к клапану основного венозного коллектора, впадающего в ПП коронарного синуса (тебезиев клапан), к терминальному гребню, расположенному в зоне устья верхней полой вены, межпредсердной перегородке и стенке предсердия [1].
Обычно сеть Хиари не имеет существенного клинического значения. Однако в литературе периодически появляются описания случаев, в которых сеть Хиари играет определенную функциональную роль. С подобным случаем довелось столкнуться и нам.
Описание клинического наблюдения
Больной М., 68 лет, поступил в отделение нарушений ритма сердца ФГБУ «ЦКБ с поликлиникой» УДП РФ в январе 2014 г. с жалобами на сердцебиение и перебои в работе сердца, общую слабость, головокружение.
 История заболевания. Пациент длительное время наблюдается врачами по поводу ишемической болезни сердца, стенокардии напряжения II функционального класса, экстрасистолической аритмии (частая желудочковая экстрасистолия) и гипертонической болезни II стадии. Последнее время лечился нерегулярно. Периодически принимает эналаприл 5 мг, соталол 40 мг. Ухудшение самочувствия отмечает в течение последних 2—3 дней, когда при измерении артериального давления (АД) отметил учащенный неритмичный пульс и слабость. В день госпитализации имелся эпизод выраженной слабости и головокружения. Была вызвана скорая медицинская помощь. На снятой электрокардиограмме (ЭКГ) зарегистрирован пароксизм мерцательной аритмии (МА), сопровождающийся гипотонией (АД 80/40 мм рт.ст.). Пациент был госпитализирован в отделение нарушений ритма сердца ФГБУ «ЦКБ с поликлиникой» УДП РФ.
История заболевания. Пациент длительное время наблюдается врачами по поводу ишемической болезни сердца, стенокардии напряжения II функционального класса, экстрасистолической аритмии (частая желудочковая экстрасистолия) и гипертонической болезни II стадии. Последнее время лечился нерегулярно. Периодически принимает эналаприл 5 мг, соталол 40 мг. Ухудшение самочувствия отмечает в течение последних 2—3 дней, когда при измерении артериального давления (АД) отметил учащенный неритмичный пульс и слабость. В день госпитализации имелся эпизод выраженной слабости и головокружения. Была вызвана скорая медицинская помощь. На снятой электрокардиограмме (ЭКГ) зарегистрирован пароксизм мерцательной аритмии (МА), сопровождающийся гипотонией (АД 80/40 мм рт.ст.). Пациент был госпитализирован в отделение нарушений ритма сердца ФГБУ «ЦКБ с поликлиникой» УДП РФ.
Из анамнеза известно, что больной страдает рядом сопутствующих заболеваний, таких как хронический бронхит, эмфизема легких, диффузный пневмосклероз, многоузловой эутиреоидный зоб, аденома предстательной железы, хронический простатит.
При поступлении в стационар состояние средней тяжести, периферических отеков нет, температура тела 36,6 °С. Периферические лимфатические узлы не увеличены. При аускультации легких дыхание жесткое, проводится во все отделы, хрипов нет. При аускультации сердца тоны сердца приглушены, аритмичные. Частота сердечных сокращений около 140 уд/мин, дефицита пульса нет. АД 130/85 мм рт.ст. Живот мягкий, при пальпации безболезненный. Печень выступает на 1 см из-под края реберной дуги. Селезенка не пальпируется. Стул в норме. Дизурических явлений нет.
Пациент в сознании, контактен, ориентирован. Острой очаговой неврологической и менингеальной симптоматики нет.
При поступлении в клиническом анализе крови эритроцитоз (эр. 6,03×1012/л при норме до 5,6×1012/л; Hb 168 г/л при норме до 160 г/л), нейтрофилез за счет сегментоядерных форм (н. 6,16×109/л при норме до 5,9×109/л, с. 78% при норме до 72%), лимфоцитопения (лимф. 1,155×109/л при норме от 1,2×109/л; 15% при норме от 19%), тромбоцитопения (тр. 121×109/л при норме от 180×109/л), остальные показатели в пределах нормы. При динамическом наблюдении за 3 нед лечения показатели красной и белой крови нормализовались.
В анализе мочи регистрировалась протеинурия (белок 320 мг/л при норме до 100 мг/л), уробилинурия (17 мкмоль/л), при микроскопии осадка лейкоциты до 15 и эритроциты до 3 в поле зрения.
Биохимический анализ крови: повышены общий билирубин (43,7 мкмоль/л при норме до 21 мкмоль/л) и прямой билирубин (23,1 мкмоль/л при норме до 5,1 мкмоль/л).
Система гемостаза исходно: активированное частичное тромбопластиновое время 27 с, фибриноген 2,8 г/л, международное нормализованное отношение (MHO) 1,1, протромбин 80%. В динамике на фоне антикоагулянтной терапии (гепарин, варфарин): MHO 1,8, фибриноген 7 г/л, протромбин 38%.
Эзофагогастродуоденоскопия: поверхностный гастрит. Хронический дуоденит. Дуоденогастральный рефлюкс желчи.
Рентгенография грудной клетки: легочные поля без свежих очаговых и инфильтративных теней с умеренно выраженным пневмосклерозом. Легочный рисунок прослеживается во всех отделах, но в верхних легочных полях рисунок обеднен, несколько больше справа. Корни легких не расширены, структурны. Сердце с небольшим увеличением левого желудочка, талия сердца сглажена. Обращало внимание склерозирование листков перикарда. Аорта без особенностей.
Ультразвуковое исследование брюшной полости, почек: незначительная гепатомегалия, признаки диффузных изменений печени, картина инфильтрации поджелудочной железы.
На ЭКГ при поступлении регистрировалась МА с частотой сокращения желудочков до 130 в 1 мин.
С учетом неизвестной давности пароксизма МА было принято решение о выполнении чреспищеводной эхокардиографии (ЧПЭхоКГ) для исключения внутрисердечного тромбоза и выработки дальнейшей тактики ведения пациента.
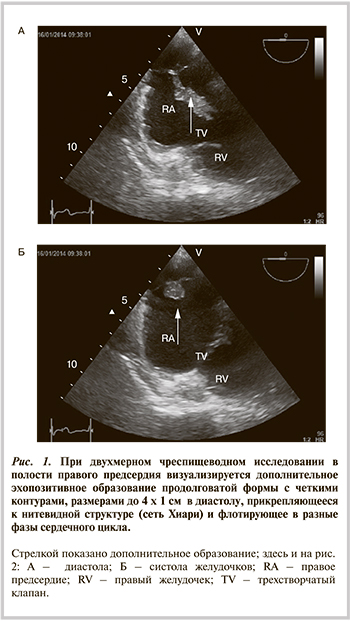
 При ЧПЭхоКГ в ПП отчетливо визуализируется высокоподвижное дополнительное эхопозитивное образование продолговатой формы, флотирующее по ходу тока крови, размерами до 4×1 см. Место прикрепления образования — устье нижней полой вены, где визуализируется нитевидная структура сети Хиари, к которой и прикрепляется выявленное дополнительное образование, не препятствующее кровотоку (рис. 1). В нижней полой вене дополнительных образований не выявлено. В других камерах сердца, в том числе в ушках левого и ПП, дополнительных эхопозитивных образований не выявлено.
При ЧПЭхоКГ в ПП отчетливо визуализируется высокоподвижное дополнительное эхопозитивное образование продолговатой формы, флотирующее по ходу тока крови, размерами до 4×1 см. Место прикрепления образования — устье нижней полой вены, где визуализируется нитевидная структура сети Хиари, к которой и прикрепляется выявленное дополнительное образование, не препятствующее кровотоку (рис. 1). В нижней полой вене дополнительных образований не выявлено. В других камерах сердца, в том числе в ушках левого и ПП, дополнительных эхопозитивных образований не выявлено.
При цветовом допплеровском картировании межпредсердной перегородки выявлено незначительное шунтирование крови слева направо на уровне открытого овального окна.
При осмотре нисходящего отдела грудной аорты отмечается увеличение толщины интимы—медии. Регистрируются гиперэхогенные атеросклеротические бляшки высотой до 3 мм на 9 и 4 часах.
Заключение: дополнительное образование в ПП. Возможный генез образования — тромб? Однако нельзя исключить и опухоль (миксому?). Открытое овальное окно.
При ранее выполненной ЧПЭхоКГ от 21.04.09 (архив ЦКБ) дополнительных образований в ПП не регистрировалось.
В связи с выявленным образованием в ПП пациенту экстренно выполнено цветовое дуплексное сканирование (ЦДС) нижней полой вены, подвздошной вены и вен нижних конечностей. Обнаружены протяженные обтурирующие тромбы левых общей и наружной подвздошных вен, глубоких вен левой нижней конечности (подколенная, поверхностная, общие бедренные вены). Верхний уровень распространения тромботических масс соответствовал устью общей подвздошной вены, где верхушка тромба фиксирована к стенкам общей подвздошной вены на уровне устья. Признаки выраженной клапанной недостаточности глубоких вен левой голени. Протяженные гиперэхогенные тромбы большой подколенной вены левой нижней конечности. Нижняя полая вена, подвздошные вены справа и глубокие подкожные вены правой нижней конечности проходимы.
Диагноз тромбоэмболии легочной артерии (ТЭЛА) был подтвержден при мультиспиральной компьютерной томографии (МСКТ): картина субмассивной двусторонней ТЭЛА. В ПП на фоне недостаточного контрастирования создается впечатление о наличии участков сниженной плотности общими размерами 26×11 мм, вероятно, тромботические массы.
Консультация сердечно-сосудистого хирурга: показаний к оперативному лечению на данный момент нет. Ввиду отсутствия дыхательной недостаточности после перенесенной ТЭЛА показаний к проведению тромболизиса нет. Рекомендовано: эластическая компрессия нижних конечностей до верхней трети бедра, возвышенное положение нижних конечностей, продолжение инфузий гепарина, прием варфарина под контролем MHO, детралекса 500 мг 2 раза в день в течение 2 мес, омепразола 20 мг 2 раза в день. Контроль ЦДС подвздошных вен и вен нижних конечностей через 7—10 дней.
Таким образом, пациент поступил в связи с пароксизмом МА неизвестной давности, сопровождавшимся выраженной слабостью и гипотонией до 80/40 мм рт.ст. Учитывая неизвестную длительность пароксизма, с целью исключения тромбоза камер сердца пациенту проведена ЧПЭхоКГ, при которой обнаружено высокоподвижное образование ПП (тромбоз? миксома?). При дополнительном проведении МСКТ выявлено образование ПП, предположительно тромб, также признаки субмассивной двусторонней ТЭЛА. При ЦДС вен нижних конечностей обнаружен тромбоз левой общей и наружной подвздошных вен и глубоких вен левой нижней конечности. На момент осмотра сосудистым хирургом показаний к оперативному лечению и тромболизису нет.
Учитывая выявленный тромбоз ПП, от активной антиаритмической терапии, направленной на восстановление синусового ритма, было решено воздержаться. С целью контроля частоты сокращений желудочков назначены β-адреноблокаторы и сердечные гликозиды. Проводилась антикоагулянтная терапия: гепарин 24 000 ед/сут через перфузатор с последующим переходом на подкожное введение эноксапарина 40 мг 2 раза в сутки, варфарин под контролем MHO.
На фоне терапии состояние пациента оставалось стабильным. По кардиомонитору регистрировалась нормосистолическая форма фибрилляции предсердий с частотой сокращения желудочков 70—80 в 1 мин; АД 110/70 мм рт.ст.
При контрольной ЧПЭхоКГ через 13 дней в камерах сердца, в том числе в ПП, тромбов не выявлено. При контрольном ЦДС вен нижних конечностей сохранялся тромбоз глубоких вен голеней без признаков ухудшения (рис. 2). Учитывая удовлетворительную переносимость аритмии, нормосистолию, отсутствие явлений сердечной недостаточности, стабильные параметры гемодинамики, от активной антиаритмической терапии, направленной на восстановление синусового ритма, решено воздержаться. С целью коррекции частоты сокращения желудочков назначена комбинация сердечных гликозидов и β-адреноблокаторов. С учетом ТЭЛА, наличия тромбоза вен голени и бедра продолжена антикоагулянтная терапия.
Таким образом, у больного с пароксизмом МА был выявлен тромбоз сети Хиари ПП; обтурирующий тромбоз левых общей и наружной подвздошных вен, глубоких вен левой нижней конечности; субмассивная двусторонняя ТЭЛА. На фоне проведенной терапии регистрировалась выраженная положительная динамика в виде отсутствия тромбоза сети Хиари ПП. Пациент был выписан в удовлетворительном состоянии под наблюдение врачей поликлиники.
Через 2 мес после выписки самочувствие пациента удовлетворительное, жалоб, в том числе и на одышку, не предъявляет. По результатам ЦДС регистрируется положительная динамика тромбоза вен левой нижней конечности.
Обсуждение
В представленном случае диагностика бессимптомной ТЭЛА, обусловленной тромбозом глубоких вен нижних конечностей, стала возможной при МСКТ грудной клетки и ЦДС нижних конечностей. Это было осуществлено только после выявления при ЧПЭхоКГ дополнительного эхопозитивного образования, фиксированного на нитевидной структуре, которая представляла собой сеть Хиари в полости ПП.
Бессимптомный характер течения ТЭЛА мог быть обусловлен постепенной эмболией легочной артерии небольшими фрагментами тромба из глубоких вен нижних конечностей. Тромб бόльших размеров в правом предсердии, обнаруженный при ЧПЭхоКГ, вероятно, фиксировался в сети Хиари, которая таким путем предотвратила клинически проявляющееся развитие ТЭЛА у представленного больного. Это предполагаемый, но вполне вероятный механизм развития ТЭЛА, если исходить из тех объективных данных, которые были получены при инструментальном обследовании.
Как уже отмечалось, сеть Хиари обычно не имеет существенного клинического значения. Однако в литературе можно найти описания случаев, в которых сеть Хиари играет определенную роль. Уже в ранних работах патологов высказано предположение о двоякой роли сети Хиари, которая может, с одной стороны, способствовать формированию тромбов, а с другой – выступать в качестве ловушки для тромбоэмболов, предохраняя больного от фатальной ТЭЛА [2, 3]. H. Chiari в одном из 11 представленных случаев наблюдал множественные тромбы в описанной им сети в ПП, а также в правой и левой легочных ветвях. Позднее W.M. Yates представил случай большого эмбола в сети Хиари у больного 39 лет с тромбозом глубоких вен проксимального отдела нижней конечности [3]. Очевидно, первоначально сеть Хиари задержала продвижение эмбола, часть которого после фрагментации в последующем преодолела сеть и привела к эмболии легочной артерии. Похожий случай представлен S.T. Yuen и P. Dickens у 86-летней женщины с фатальным переломом шейки бедренной кости [4]. Сеть Хиари содержала тромб, а в правой легочной артерии был обнаружен эмбол, содержащий материал костного мозга и тромбоциты с фибрином. Авторы предположили, что захваченный сетью Хиари эмбол костного мозга инициировал развитие большего по размерам тромба, который и привел к фатальной ТЭЛА.
Таким образом, в исследованиях патологов неоднократно обсуждался механизм развития ТЭЛА, при котором сеть Хиари могла сыграть роль промежуточного барьера. Этот механизм, по-видимому, имелся у представленного больного, и нам удалось документировать это по результатам инструментальных исследований.



