По данным современных исследований, заболеваемость инфекционным эндокардитом (ИЭ) составляет 3–10 случаев на 100 тыс. человек в год [1, 2].
В течение последних десятилетий увеличилось количество и изменилось соотношение основных факторов риска ИЭ, среди которых основное значение имеют инъекционная наркомания, кардиохирургические операции и инвазивные медицинские манипуляции, что привело к смене ведущего возбудителя, которым в настоящее время, согласно большинству исследований, является Staphylococcus aureus [3].
В настоящее время при ведении пациентов с ИЭ активно используются современные методы визуализации, в том числе мультиспиральная компьютерная томография (МСКТ), магнитно-резонансная томография (МРТ), радиоизотопные методы исследования. При этом ключевую роль среди данных методов исследования в ходе диагностики ИЭ играет эхокардиография, метод проведения которой зависит от конкретной клинической ситуации [4, 5].
Высокие цифры летальности при ИЭ во многом обусловлены развитием потенциальных осложнений, среди которых наиболее часто отмечаются развитие и прогрессирование сердечной недостаточности, тромбоэмболические проявления и развитие инфекционных аневризм [2, 5].
ИСТОРИЧЕСКИЕ АСПЕКТЫ ЭХОКАРДИОГРАФИИ ПРИ ДИАГНОСТИКЕ ИНФЕКЦИОННОГО ЭНДОКАРДИТА
Открытие метода прижизненной визуализации вегетаций на клапанах сердца стало важнейшим этапом в изучении ИЭ. В 1970-х гг. Харви Фейгенбаум собрал серию наблюдений, в которой обращалось внимание на визуализацию вегетаций при эхокардиографии в М-режиме. Позже, в 1980 г., Д. Стюарт с соавт. из университета Дюка сообщили, что у 54% пациентов с ИЭ удалось выявить вегетации при эхокардиографии (ЭхоКГ) [6].
С тех пор ЭхоКГ претерпела модернизацию от одномерного трансторакального ориентировочного метода (ТТЭ) диагностики до высокочувствительного трансэзофагеального метода (ТЭЭ), позволяющего, помимо вегетаций, визуализировать и другие патологические изменения (абсцесс, псевдоаневризма, несостоятельность протеза клапана) [5].
Дэвид Дюрак с соавт. в 1994 г. из университета Дюка систематизировали и обобщили данные об ИЭ, заменив патологоанатомический критерий обнаружения вегетации на эхокардиографический, что легло в основу новой классификации. Авторы выделили определенный, возможный и отвергнутый диагноз ИЭ. При этом определенный диагноз можно было установить при жизни пациента. Университетом Дюка были разработаны критерии диагностики с использованием модификации Дюрака и принципа Томаса Дукетта Джонсона (1899–1954), который предложил разделять критерии на большие и малые [7]. Таким образом, ЭхоКГ и культура крови стали иметь одинаковый вес и на сегодня считаются большими критериями ИЭ, что привело к увеличению чувствительности диагностики.
ВОЗМОЖНОСТИ ЭХОКАРДИОГРАФИИ ПРИ ДИАГНОСТИКЕ ИНФЕКЦИОННОГО ЭНДОКАРДИТА
Разрешающая диагностическая способность трансторакальной двухмерной ЭхоКГ (ТТЭ) с использованием допплеровской техники при ИЭ составляет 80% [8]. Применение трансэзофагеальной эхокардиографии (ТЭЭ) повышает чувствительность метода для диагностики ИЭ до 90–94%, поскольку при этом устраняется преграда для ультразвукового сигнала в виде подкожно-жирового слоя, ребер, воздуха в легких, а также обеспечивается непосредственная близость от исследуемого участка [9, 10].
Согласно современным рекомендациям, ЭхоКГ следует выполнять во всех случаях с подозрением на ИЭ. Тактика исследования (ТТЭ или ТЭЭ) зависит от конкретной клинической ситуации (табл. 1). ТТЭ рекомендуется как средство визуализации первой линии при вероятном ИЭ, а также после завершения антимикробной терапии для оценки кардиальной и морфологической функции клапана. Вместе с тем ТЭЭ рекомендуется проводить у пациентов с сочетанием высокой клинической вероятности ИЭ и отсутствием обнаружения патологических изменений в ходе проведения ТТЭ, а также в случае инфекционного поражения протезированных клапанов [5, 11].

Отрицательный результат ЭхоКГ, особенно на фоне кальцинированного порока сердца, не отвергает диагноз ИЭ. Выявление патологических изменений может быть также затруднено при наличии уже существующих серьезных поражений (пролапс митрального клапана, протезирование клапанов), при их размерах менее 5 мм, а также при ИЭ без вегетаций [4, 5].
Если уровень клинического подозрения высок, а также в случае с изначально негативной диагностикой повторные ТТЭ/ТЭЭ должны проводиться через 7–10 дней и даже раньше при этиологической роли S. aureus [5, 12].
Интраоперационную ЭхоКГ следует проводить во всех случаях ИЭ, требующих оперативного лечения [5].
Наиболее распространенное морфологическое проявление ИЭ – формирование бактериальных вегетаций. Характерным признаком вегетаций является обнаружение грубых, нерегулярных Эхо-сигналов на створках клапанов. Этот признак отличается от дрожания створок, обусловленного регургитантным потоком, возникновением в различные фазы систолы и диастолы (рис. 1) [8].
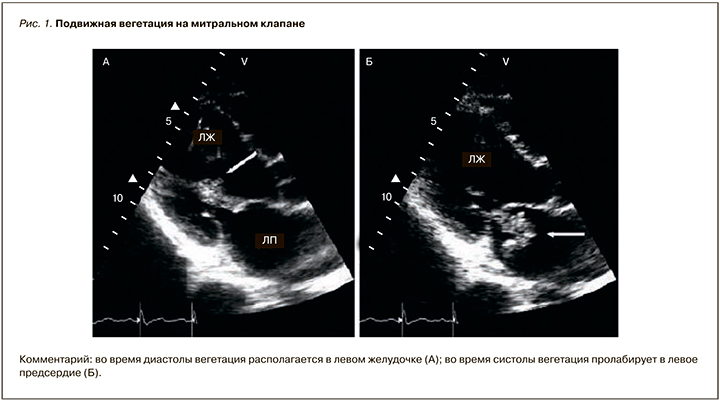
В соответствии с рекомендациями Европейского общества кардиологов 2015 г. четыре признака, которые можно обнаружить при проведении эхокардиографии, являются большими критериями ИЭ: это вегетации, абсцесс, псевдоаневризма и дисфункция протезированного клапана (табл. 2) [5].
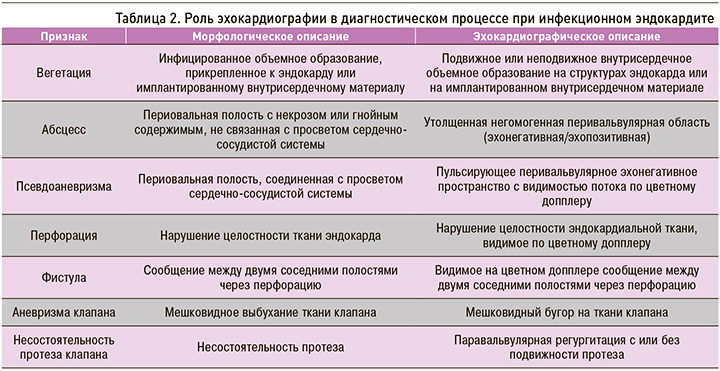
ПРАКТИКА ПРИМЕНЕНИЯ ЭХОКАРДИОГРАФИИ ПРИ ДИАГНОСТИКЕ ИНФЕКЦИОННОГО ЭНДОКАРДИТА В РОССИИ
Согласно существующей практике, в России крайне недостаточно многоцентровых исследований, характеризующих проблемы диагностики и терапии ИЭ. Одним из таких научных проектов стало исследование МАЭСТРО, включившее случаи определенного и вероятного ИЭ из 11 стационаров 9 городов нашей страны.
При проведении этого исследования в 84,2% случаев использовалась только ТТЭ, ТЭЭ – в 3,7%, ТТЭ и ТЭЭ – в 12,1%. В определенной мере такую низкую частоту применения ТЭЭ можно объяснить инвазивным характером этого исследования.
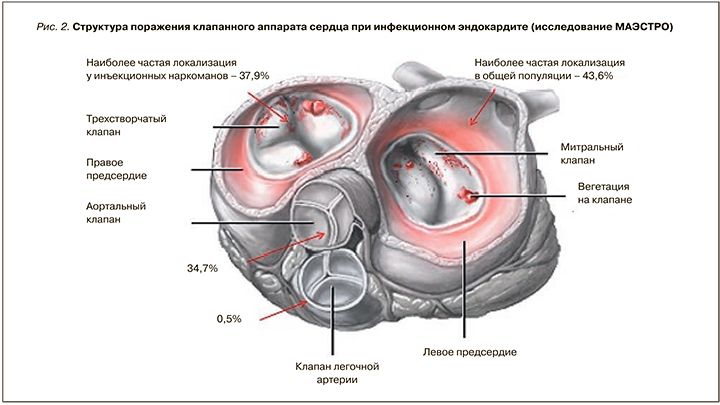
При этом наиболее частой локализацией инфекционного поражения был митральный клапан (43,6%). Следует также отметить достаточно высокие цифры поражения трехстворчатого клапана (34,7%), что можно объяснить высокой частотой инъекционной наркомании и других факторов риска (катетеризация центральных вен, инвазивные манипуляции на крупных сосудах), способствующих повреждению целостности периферических сосудов (рис. 2). Кроме того, согласно полученным результатам, в 15,9% отмечалось сочетанное поражение клапанов, являющееся одной из тенденций современного течения ИЭ [2].
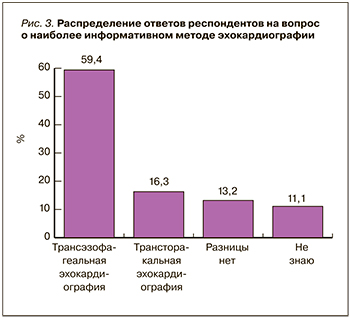 С учетом комплексного характера проблемы ИЭ в рамках проведения исследования МАЭСТРО был проведен опрос 530 врачей различной специальности, сталкивающихся с этим заболеванием. При ответе на вопрос о наиболее информативном методе ЭхоКГ только 59,4% респондентов отметили преимущества ТЭЭ перед ТТЭ (рис. 3) [1]. Значение этого показателя представляется крайне недостаточным в условиях принципиально важной роли трансэзофагеального исследования в описываемых выше случаях.
С учетом комплексного характера проблемы ИЭ в рамках проведения исследования МАЭСТРО был проведен опрос 530 врачей различной специальности, сталкивающихся с этим заболеванием. При ответе на вопрос о наиболее информативном методе ЭхоКГ только 59,4% респондентов отметили преимущества ТЭЭ перед ТТЭ (рис. 3) [1]. Значение этого показателя представляется крайне недостаточным в условиях принципиально важной роли трансэзофагеального исследования в описываемых выше случаях.
ЗАКЛЮЧЕНИЕ
Визуализирующие методы играют ключевую роль в диагностике ИЭ, что закреплено в общепризнанных Duke-критериях. Среди них наиболее значима ЭхоКГ, позволяющая выявить вегетации на клапанах и хордах, миокардиальные абсцессы, перфорации и разрывы створок клапанов, разрывы хорд, а также оценить степень клапанной регургитации.
Наиболее распространенным и чаще всего применяемым методом диагностики ИЭ является ТТЭ. Однако в ряде случаев ее выполнению мешают акустические препятствия на пути ультразвукового луча: ребра, легкие, хорошо развитые мышцы и подкожно-жировой слой, выраженный кальциноз и фиброз параклапанных структур, послеоперационные сращения, акустическая тень от опорного кольца и диска механического протеза. Наименее эффективна ТТЭ в диагностике ИЭ искусственных клапанов, абсцессов сердца и мелких плоскостных вегетаций. В таких случаях большую ценность имеет ТЭЭ.
Следует подчеркнуть, что ЭхоКГ зачастую становится методом, определяющим лечебную тактику. Так, обнаружение абсцесса фиброзного кольца, фистул между камерами сердца, раннего ИЭ протезированного клапана, гемодинамически значимых парапротезных фистул или признаков частичного отрыва протеза служит показанием к хирургическому вмешательству.
В последние годы увечилось количество публикаций, свидетельствующих о потенциальной роли в диагностике инфекционного поражения эндокарда компьютерной томографии и МРТ. Вместе с тем на сегодня эти методы исследования не вошли в рутинную практику, и их применение при ИЭ в основном ограничено диагностикой тромбоэмболических осложнений, а также поиском истинного диагноза при лихорадке неясного генеза.



