Хроническая болезнь почек (ХБП) и терминальная стадия хронической почечной недостаточности (ТХПН) являются глобальными проблемами здравоохранения с растущей распространенностью [1]. По некоторым данным, до 40% случаев ТХПН в первые три десятилетия жизни обусловлены врожденными аномалиями мочевыводящих путей (ВАМВП) [2, 3].
Распространенность ВАМВП колеблется от 4,2 на 10 000 рождений на Тайване до 4,0 на 1000 рождений в России и некоторых азиатских и европейских странах [4–8]. К сложным особенностям ВАМВП относится то, что они могут диагностироваться впервые не только в пренатальном периоде, но и в детском или взрослом возрасте. Хотя большинство из этих состояний имеют благоприятный прогноз, возможность стойкого повреждения почек и потенциально повышенного риска развития ХБП в зрелом возрасте может быть недооценена. ВАМВП у взрослых пациентов также могут играть определенную роль в формировании артериальной гипертензии (АГ) [9]. Вклад ВАМВП в формирование потребности в заместительной почечной терапии у взрослых, в отличие от детей, менее очевиден и, возможно, недооценивается [10].
Цель исследования – оценить распространенность аномалий развития мочевыводящих путей и дисплазии соединительной ткани (ДСТ) среди пациентов с ТХПН на гемодиализе.
МАТЕРИАЛ И МЕТОДЫ
Исследование проводилось на базе отделения терапевтической нефрологии, отделение диализа БУЗОО «Областная клиническая больница» (г. Омск). В исследование включались пациенты с ТХПН, получавшие заместительную почечную терапию (гемодиализ) и подписавшие информированное согласие. В исследование поперечного среза вошли 72 пациента (41 мужчина); медиана возраста на момент включения составила 60 лет (LQ 48,5; UQ 65,0), медиана возраста начала гемодиализа – 57 лет (LQ 44,0; UQ 62,00).
Гемодиализ проводился по стандартной программе (3 раза в неделю по 4–4,5 ч) на аппаратах «искусственная почка» Innova (GAMBRO, Швеция) и Surdial Х (Nipro, Япония) с использованием бикарбонатного диализирующего раствора.
Статистическая обработка результатов проводилась посредством методов описательной статистики: количественные признаки в группе описывались как медиана, нижний и верхний квартили (Ме, LQ; UQ), качественные признаки приводились с указанием абсолютного значения в соотношении с общей численностью группы и/или процентов. Статистическая обработка материалов выполнялась с помощью пакетов программ Statistica 10,0 (StatSoft). Сравнение двух независимых групп проводили с применением U-критерия Манна–Уитни, при сравнении частот качественных признаков независимых выборок использовали критерий χ2 с поправкой Йейтса. За статистически значимый принимали уровень p <0,05.
РЕЗУЛЬТАТЫ
В изучаемой группе пациентов ВАМВП, как основная патология, приведшая к развитию ХБП, имела место у 14 пациентов (19,4%). По распространенности среди причин ТХПН она конкурировала с гломерулонефритом (20/72 случаев, в том числе 2 случая поражения почек при ревматоидном артрите), эссенциальной АГ и сахарным диабетом (16/72 и 14/72 случаев соответственно). Другие варианты почечной патологии встречались значительно реже (мочекаменная болезнь, n=5; тубулоинтерстициальный лекарственный нефрит, n=6; синдром Альпорта, n=1; ренопривное состояние (билатеральный рак почек), n=1; стеноз почечной артерии (субокклюзия правой почечной артерии, стеноз левой почечной артерии), n=1; микроскопический полиангиит, n=1; первичный пиелонефрит, n=1).
Среди ВАМВП регистрировались:
- поликистозная болезнь почек (ПКБ) (n=7);
- первичный пузырно-мочеточниковый рефлюкс (ПМР) (n=4);
- гипоплазия почки (n=2);
- аплазия почки (n=1).
Из 7 пациентов с ПКБ в 5 случаях присутствовали кисты печени, в 1 случае – расширение синусов Вальсальвы и аневризма восходящего отдела аорты. У родственников 1 линии родства 3 пациентов также имелась ПКБ.
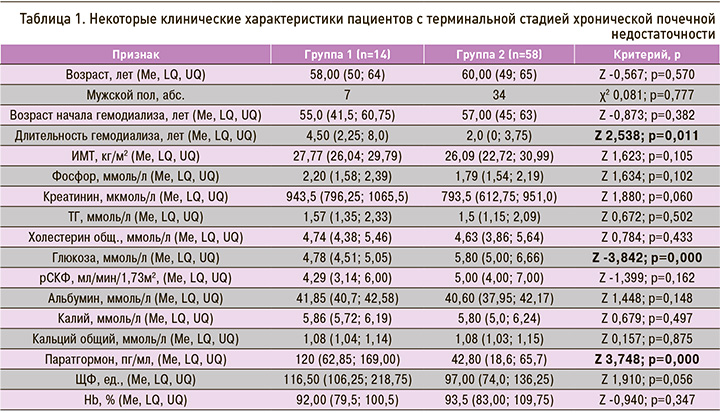
Для дальнейшего анализа были сформированы 2 группы пациентов: группа 1 – пациенты с ВАМВП (n=14) и группа 2 – пациенты без ВАМВП (n=58). Группы не различались по полу и возрасту на момент обследования (табл. 1); не было между ними и различий по возрасту начала гемодиализа, однако длительность диализа была статистически выше в группе 1. По большинству клинико-лабораторных характеристик группы не различались, за исключением статистически значимо более высокого уровня глюкозы и более низкого уровня паратгормона в группе 2.
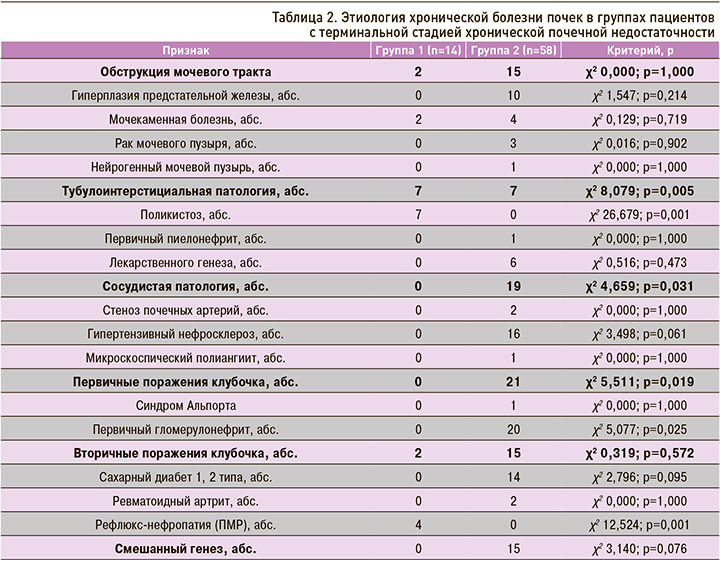
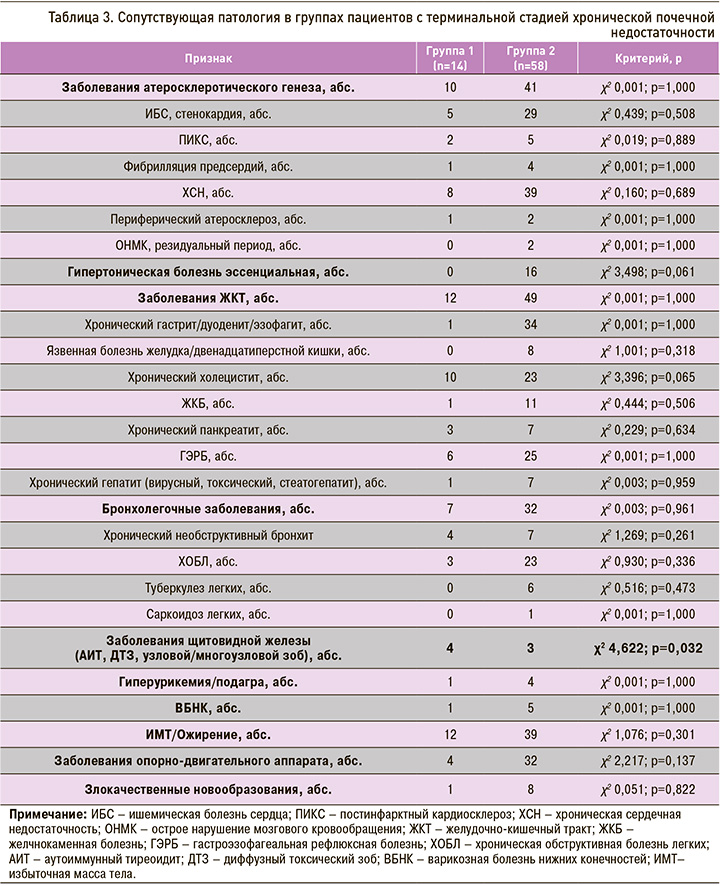
В этиологической структуре ХБП были отмечены различия между группами: в группе 1 в сравнении с группой 2 статистически значимо чаще регистрировалась тубулоинтерстициальная патология, реже первичные гломерулярные поражения и сосудистая патология (табл. 2). При анализе ассоциированной и сопутствующей патологии выявлено, что в группе 1 статистически значимо чаще встречалась патология щитовидной железы (табл. 3). При этом следует отметить, что в группе 1 статистически значимо чаще имелся вторичный пиелонефрит (14/14 и 12/58; χ2 6,365; р=0,012). С одинаковой частотой встречались простые кисты почек (1/14 и 18/58; χ2 2,199; р=0,138). Хроническая анемия как осложнение ХБП регистрировалась с одинаковой частотой (13/14 и 58/58; χ2 0,605; р=0,437).
В общей группе пациентов индекс коморбидности Charlson составил 5,0 (4,0; 7,0). Группа 1 отличалась статистически значимо меньшим индексом коморбидности к несколько более высокому индексу в группе 2 (группа 1 – 4,0 (3,25; 5,0); группа 2 – 5,5 (4,0; 7,0;); Z -1,992; р=0,004). Структура сопутствующей патологии в группах существенно не различалась (см. табл. 3).
В группе 1 статистически значимо чаще встречались малые аномалии развития (МАР) и пороки развития сердечно-сосудистой системы (χ2 5,013; р=0,026), представленные в группе 1 открытым овальным окном (n=2) и аномально прикрепленными хордами левого желудочка (n=1), в группе 2 – аневризмой межпредсердной перегородки с дефектом (n=1) и поликистозом печени, во всех случаях сопутствовавшим поликистозу почек (χ2 17,077; р=0,001). В общей группе (n=72) пациентов средний возраст составлял 60 лет (48,5; 65,0). В среднем и пожилом возрасте диагностика ДСТ сложна вследствие инволюционных изменений, и многие признаки ДСТ утрачивают диагностическое значение. Вследствие этого диагностика ДСТ проводилась с учетом анамнестических данных и архива медицинской документации, отражающих время появления того или иного признака ДСТ. При этом учитывались только признаки, зарегистрированные в период от рождения до 45 лет. Таким образом, ДСТ была установлена у 2 пациентов (2/72). В обоих случаях проявления ДСТ соответствовали маловыраженной форме (диагностические коэффициенты ДСТ составили 18,33 и 21,56 балла). Оба пациента входили в группу 1 (χ2 4,054; р=0,044).
ОБСУЖДЕНИЕ
В обследованной группе пациентов ВАМВП, как основная патология, приведшая к развитию ХБП, имела место примерно у каждого пятого пациента с ТХПН.
Термин ВАМВП (CAKUT – congenital anomalies of the kidneys or lower urinary tract) широко используется для описания пороков развития мочевыделительной системы, которые могут возникать изолированно, в сочетании или в составе других синдромов. Врожденные почечные аномалии могут быть спорадическими или семейными, синдромными или неcиндромными [9].
По данным исследований, от 6 до 50% ВАМВП связаны с пороками развития [4–6, 11–13]. В недавнем исследовании показано, что среди младенцев с ВАМВП у 34% выявляются аномалии других органов и систем, причем в 16% случаев имеются множественные врожденные несиндромные нехромосомные аномалии, из которых наиболее распространенными были дисморфогенетические состояния костно-мышечной, пищеварительной, сердечно-сосудистой и центральной нервной систем [14].
Следует отметить, что в группе пациентов с ВАМВП мы статистически значимо чаще встречали малые аномалии и пороки развития сердечно-сосудистой системы, что согласуется с имеющимися наблюдениями. Врожденные пороки сердца являются наиболее распространенными аномалиями, связанными с ВАМВП, и ведущими пороками развития в целом [15]. С другой стороны, ВАМВП являются одним из наиболее распространенных дефектов, связанных с врожденными пороками сердца [11, 16]. ВАМВП ассоциированы с 23,1% врожденных пороков сердца, что косвенно свидетельствуют о совпадении генетической этиологии врожденных пороков сердца и ВАМВП [17].
ВАМВП могут быть вызваны генетическими, эпигенетическими и экологическими факторами. Пороки развития мочевыводящих путей могут быть семейными, и в некоторых случаях у больных могут быть обнаружены специфические мутации генов, участвующих в развитии мочевого тракта [10]. Генетические исследования показали, что ВАМВП является генетически гетерогенным расстройством, а фенотип зависит от взаимодействия генов и эпигенетических путей [18]. Установлены моногенные мутации в нескольких генах, вовлеченные в развитие ВАМВП, однако эти мутации объясняют только 5–20% заболеваний пациента [3]. Учитывая важную особенность развития мочевыделительной системы, а именно динамическую временную и пространственную интеграцию тканей-предшественников различного эмбрионального происхождения, требующую точного контроля за пролиферацией, апоптозом, миграцией и дифференцировкой всех клеток-предшественников [19], можно предполагать роль ранних морфофункциональных аномалий соединительнотканных структур в генезе ВАМВП. В детской популяции описаны ассоциации ВАМВП с недифференцированной дисплазией соединительной ткани [20]. По некоторым данным, частота аномалий развития верхних мочевых путей при ДСТ сопоставима с распространенностью аномалий сердца при ДСТ [21]. Кроме того, роль почечного интерстиция в развитии ХБП при ВАМВП крайне важна, а при некоторых состояниях (аутосомно-доминантный поликистоз почек) является преобладающей среди механизмов, лежащих в основе прогрессирования патология почек от воспалительного процесса до фиброза. В нашей группе пациентов ДСТ была выявлена в 2 случаях и только среди пациентов с ВАМВП. Известно, что у пациентов с ДСТ вследствие целого спектра диспластикозависимых изменений течение воспалительной патологии почек характеризуется большей тяжестью [22]. Однако значение ДСТ с поражением почек в развитии ХБП, в том числе ТХПН, до сих пор неизвестно. В нашем наблюдении преобладание ДСТ в группе пациентов с ТХПН и ВАМВП как минимум подтверждает известный факт об ассоциациях ДСТ с малыми аномалиями и пороками развития внутренних органов. ДСТ действительно можно рассматривать как маркер нарушений процессов морфогенеза.
ВАМВП включает широкий спектр врожденных дефектов в мочевой системе, начиная от агенезии почек и гипоплазии, структурной дупликации и неправильного позиционирования до дефектов мочеточника и мочевого пузыря. В нашем наблюдении структуре ВАМВП на первом месте по частоте встречаемости была поликистозная болезнь почек, реже встречались первичный пузырно-мочеточниковый рефлюкс, аплазия/гипоплазия почки.
Поликистозная болезнь почек (ПКБ) – это генетически обусловленное заболевание, которое связано с образованием и прогрессированием кист в почках, происходящих из эпителиоцитов канальцев и/или собирательных трубочек, представленное двумя, по сути, разными вариантами – аутосомно-доминантным (АДПКБ) и аутосомно-рецессивным (АРПКБ). Аутосомно-рецессивный поликистоз почек (АРПКП, поликистозная болезнь новорожденных) обычно протекает тяжелее, а встречается значительно реже, чем АДПКП: с частотой 1:10 000–1:20 000 населения [23]. АРПКП обычно диагностируется в детском возрасте, в том числе у новорожденных и характеризуется высокой летальностью уже в детском возрасте. АДПКБ – наиболее распространенное генетически детерминированное поражение почек с частотой встречаемости от 1:400 до 1:1000 новорожденных. Приблизительно 12,5 млн человек на земном шаре страдают АДПКБ, а АРПКБ встречается гораздо реже – от 1:10 000 до 1:20 000 новорожденных, половое и расовое распределение равномерное при обоих типах [23]. АДПКБ является одним из наиболее распространенных наследственных заболеваний у человека, характеризуется генетической гетерогенностью, значительным фенотипическим разнообразием и различным прогнозом. В мире АДПКБ диагностируется у 4–7 млн пациентов, у 7–15% пациентов, получающих заместительную почечную терапию [24]. У большинства пациентов с АДПКБ почечная дисфункция не проявляется до четвертого или пятого десятилетия жизни, около 50% пациентов АДПКБ к 60-летнему возрасту находятся на заместительной почечной терапии [25, 26]. В нашем наблюдении ПКБ была самым частым вариантом ВАМВП. К экстраренальным проявлениям АДПКБ относятся кисты в желчных протоках печени, протоках поджелудочной железы, семенных пузырьках и паутинной оболочке, а также некистозные проявления, такие как внутричерепные аневризмы и долихоэктазии, дилатация корня аорты, пролапс митрального клапана и грыжи брюшной стенки [27]. Из 7 пациентов с ПКБ в 5 случаях присутствовали кисты печени (из них у 3 пациентов среди родственников 1 степени родства также имелась ПКБ), в 1 случае – расширение синусов Вальсальвы и аневризма восходящего отдела аорты, что является характерным клиническим признаком АДПКБ [23].
Первичный ПМР считается одним из наиболее распространенных пороков развития мочевыводящих путей. Этот термин описывает ретроградное движение мочи из мочевого пузыря в верхние мочевые пути, которое не вызвано обструкцией мочевого пузыря (т.е. «первичный» ПМР) и не связано с пороками развития вне почечного тракта (т.е. «несиндромный» ПМР). Точная распространенность ПМР неизвестна, поскольку до сих пор не проводилось цистографическое исследование большого числа бессимптомных пациентов. Однако, по некоторым оценкам, распространенность этой патологии достигает 10% среди детей грудного и раннего возраста [28]. Специфические генетические причины первичных несиндромных форм ПМР до настоящего времени не установлены [18, 29]. Проспективные исследования показывают, что более легкие степени ПМР обычно спонтанно регрессируют в детском возрасте [30]. Тем не менее у некоторых пациентов с ПМР развивается нефросклероз, с патологическими изменениями сходный с обструктивной нефропатией. В нашей группе пациентов врожденный уретерогидронефроз был зарегистрирован в 2 случаях. Как известно, гидронефроз является результатом прямого или косвенного воздействия условий, препятствующих оттоку мочи по мочевыводящим путям, и не является самостоятельным заболеванием. Персистенция гидронефроза может привести к атрофии канальцев, воспалению и фиброзу. Эти патологические изменения в совокупности являются примером «обструктивной нефропатии» и «обструктивной уропатии». Эти термины имеют сходные значения с небольшим акцентом на патологические изменения в почках (обструктивная нефропатия) или с дополнительным указанием на вовлечение нижних мочевых путей (обструктивная уропатия). Врожденная обструктивная нефропатия является наиболее частой причиной хронических заболеваний почек в детской популяции [18]. В нашем наблюдении врожденный уретерогидронефроз имел рефлюксирующий генез и подвергался хирургической коррекции в детском возрасте. Существуют данные, что до 8% терминальных стадий ХБП может быть вызвано ПМР [31, 32]. Кроме того, ПМР часто ассоциируется с инфекцией мочевыводящих путей. В нашем наблюдении пиелонефрит был диагностирован у всех пациентов с ВАМВП.
Гипоплазия почки относится к порокам почек с уменьшенным количеством нефронов вследствие аномалии морфогенеза. Односторонняя гипоплазия имеет частоту 1/1000, в то время как двусторонние случаи встречаются реже (1/4000) [10]. В нашем наблюдении гипоплазия, как и аплазия почек, была односторонней. Если в случае двусторонней гипоплазии развивается ТХПН в среднем или позднем детском возрасте, а также имеется высокая вероятность развития артериальной гипертензии, то односторонняя гипоплазия может не иметь никаких существенных последствий в большинстве случаев [10], однако в части случаев у пациентов развивается вторичный гломерулосклероз [18].
В нашем наблюдении в группе пациентов с ВАМВП статистически значимо чаще регистрировалась тубулоинтерстициальная патология, реже первичные гломерулярные поражения и сосудистая патология, все пациенты имели вторичный пиелонефрит. Несмотря на то что полиморбидная патология характерна для большинства пациентов с ТХПН, индекс коморбидности был статистически значимо ниже в группе пациентов с ВАМВП.
На наш взгляд, особое внимание к ВАМВП определяется тем, что раннее выявление лиц с повышенным риском формирования и прогрессирования ХБП может позволить проводить ранние вмешательства, которые могут снизить частоту развития ТХПН и связанных с ней осложнений. В недавнем популяционном когортном исследовании показано, что анамнез заболеваний почек в детском возрасте (ВАМВП, пиелонефрит, гломерулонефрит) без клинических или лабораторных признаков снижения функции почек в подростковом возрасте был связан со значительно повышенным риском развития терминальных стадий ХБП во взрослом возрасте: риск развития ТХПН в течение 30 лет наблюдения был примерно в четыре раза выше, чем риск среди участников исследования, не имевших такого анамнеза. При этом ассоциации между любым заболеванием почек в детском возрасте (ВАМВП, пиелонефрит и гломерулонефрит) и риском развития ТХПН во взрослом возрасте были сходными по величине (скорректированные коэффициенты риска составили 5,19, 4,03 и 3,85 соответственно).
Таким образом было показано, что как повреждение почек в детском возрасте, так и врожденные структурные аномалии почек имеют долгосрочные последствия [33]. В связи с этим представляется перспективным поиск дополнительных клинических, молекулярно-генетических маркеров риска неблагоприятного прогноза пациентов с ВАМВП. В частности, роль системного дисморфогенеза соединительной ткани в почечном континууме требует дальнейшего изучения.
ЗАКЛЮЧЕНИЕ
В обследованной группе пациентов ВАМВП, как основная патология, приведшая к развитию ТХПН, имела место в 19,4% случаев. В структуре ВАМВП на первом месте по частоте встречаемости была поликистозная болезнь почек, реже встречались первичный пузырно-мочеточниковый рефлюкс, аплазия/гипоплазия почки. Группа пациентов с ВАМВП характеризовалась следующими статистически значимыми отличиями: большей частотой малых аномалий/пороков развития внутренних органов (сердечно-сосудистой системы) и ДСТ, большей частотой тубулоинтерстициальной патологии, меньшей частотой первичных гломерулярных поражений и сосудистой патологии, большей частотой вторичного пиелонефрита, более низким индексом коморбидности Charlson.


