Язвенный колит (ЯК) – хроническое заболевание, характеризующееся иммунным диффузным воспалением слизистой оболочки толстой кишки с обязательным вовлечением в воспалительный процесс прямой кишки [1]. Современные эпидемиологические исследования свидетельствуют о значительном росте заболеваемости ЯК [2, 3]. В экономически развитых странах заболеваемость ЯК составляет до 30 человек на 100 тыс. населения, причем пик приходится на возрастной период от 20 до 40 лет [4]. Это хроническое заболевание связано с нарушением качества жизни, повышением нетрудоспособности и снижением продуктивности.
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью поражения толстой кишки, наличием внекишечных проявлений, длительностью заболевания, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений ЯК [5, 6]. Для поддержания ремиссии больной должен оставаться на противорецидивной терапии [7, 8]. Тем не менее у половины больных ЯК рецидивирует в течение первого года после установления диагноза, ремиссия в течение 3–7 лет сохраняется лишь у 1/4 больных, а ежегодные рецидивы наблюдаются у 1/5 из них. Только у половины больных после первой атаки ЯК ремиссия сохраняется на протяжении 5 лет. Примерно 20% больных переносят колэктомию в течение 10 лет, 30% – в течение 25 лет [9]. В среднем оперативные вмешательства при ЯК выполняются у 10–20% пациентов [6, 10, 11].
Появление генно-инженерных биологических препаратов (ГИБП) значительно повлияло на продолжительность ремиссии, частоту рецидивов и осложнений ЯК. Внедрение их в лечебную практику позволило эффективнее преодолевать гормонорезистентность и гормонозависимость ЯК, увеличить продолжительность безрецидивного периода, снизить риск развития рецидива, уменьшить частоту оперативных вмешательств и значительно улучшить качество жизни больных [12]. Однако традиционными препаратами первой линии при лечении легких и среднетяжелых форм заболевания для купирования атаки и индукции ремиссии, а также для поддержания ремиссии являются препараты 5-аминосалициловой кислоты (5-АСК) [13–15].

Механизм действия аминосалицилатов обусловлен ингибированием медиаторов воспаления (производных арахидоновой кислоты и провоспалительных цитокинов), участвующих в реализации межклеточных взаимодействий и развитии воспаления при воспалительных заболеваниях кишечника (ВЗК). Высокие дозы 5-АСК и сульфасалазина подавляют продукцию простагландинов, а низкие могут ее стимулировать [16], т.к. простагландины при ВЗК играют такую же протективную роль для слизистой оболочки кишечника, как и для слизистой оболочки желудка при язвенной болезни.
 Первым препаратом из группы 5-АСК является сульфасалазин, синтезированный в 1946 г.; он представляет собой 5-АСК, соединенную азотистой связью с сульфаниламидом (сульфапиридином). Терапевтическая доза сульфасалазина назначается до достижения клинико-эндоскопической ремиссии (в течение 4–8 нед), после чего рекомендуется пожизненная поддерживающая терапия для профилактики рецидива. Несмотря на почти 60-летнюю историю, сульфасалазин не утратил своего клинического значения, хотя у него есть существенные недостатки, ограничивающие возможность увеличения доз и длительность приема. Сульфасалазин токсичен и обладает широким спектром побочных реакций, которые встречаются у 15–20% больных. Развитие побочных эффектов связано с сульфаниламидной частью препарата, поскольку сульфапиридин почти полностью всасывается из толстой кишки и метаболизируется в печени.
Первым препаратом из группы 5-АСК является сульфасалазин, синтезированный в 1946 г.; он представляет собой 5-АСК, соединенную азотистой связью с сульфаниламидом (сульфапиридином). Терапевтическая доза сульфасалазина назначается до достижения клинико-эндоскопической ремиссии (в течение 4–8 нед), после чего рекомендуется пожизненная поддерживающая терапия для профилактики рецидива. Несмотря на почти 60-летнюю историю, сульфасалазин не утратил своего клинического значения, хотя у него есть существенные недостатки, ограничивающие возможность увеличения доз и длительность приема. Сульфасалазин токсичен и обладает широким спектром побочных реакций, которые встречаются у 15–20% больных. Развитие побочных эффектов связано с сульфаниламидной частью препарата, поскольку сульфапиридин почти полностью всасывается из толстой кишки и метаболизируется в печени.
Проблема токсичности была решена созданием препаратов 5-АСК без сульфапиридина в молекуле (месалазин, олсалазин, балсалазид). Эти препараты не уступают сульфасалазину по эффективности, а, возможно, и превосходят его, но лишены его побочных эффектов. Наибольшее распространение как за рубежом, так и в России получили месалазины, которые используются для лечения и профилактики рецидивов ЯК и имеют минимум побочных эффектов, связанных с индивидуальной непереносимостью препарата. Однако достижение ремиссии ЯК напрямую зависит от концентрации 5-АСК в слизистой оболочке толстой кишки (СОТК) [17]. При приеме внутрь чистый месалазин быстро и практически полностью метаболизируется эпителиоцитами тонкой кишки до неактивного метаболита – N-ацетил-5-АСК. Для обеспечения в просвете толстой кишки максимального терапевтического эффекта препараты месалазина непрерывно эволюционировали, появлялись новые лекарственные формы, в том числе формы с замедленным высвобождением 5-АСК, что обеспечило постоянный рост эффективности терапии ВЗК. Как за рубежом, так и в России получили месалазины, которые используются для лечения и профилактики рецидивов ЯК и имеют минимум побочных эффектов, связанных с индивидуальной непереносимостью препарата. В настоящее время специализированные фармакологические технологии изготовления лекарственных средств обеспечивают прицельную доставку месалазина к пораженному участку, поддерживая его высокую концентрацию на всем протяжении толстой кишки [18–20]. Для обеспечения данных целей создана MMX®-система доставки месалазина. MMX®-система (мультиматричная) – зарегистрированная торговая марка Cosmo Technologies Limited. С ноября 2011 г. новый препарат месалазина (Мезавант) с ММХ®-технологией доступен в Российской Федерации. Мезавант показан для индукции клинической и эндоскопической ремиссии у пациентов с легким и среднетяжелым течением ЯК как в обострении, так и для поддержания ремиссии заболевания. Мультиматричная система доставки Мезаванта включает: устойчивую к среде желудка рН-зависимую оболочку, которая разрушается в терминальном отделе подвздошной кишки при pH ≥6,8, что позволяет доставить месалазин к пораженному участку без потерь в верхних отделах желудочно-кишечного тракта (ЖКТ); гидрофильную матрицу, которая при взаимодействии с кишечным содержимым формирует вязкую гелеобразную массу, обеспечивающую медленное равномерное высвобождение месалазина, и липофильную матрицу, создающую гидрофобную среду и адгезию месалазина к СОТК, что обеспечивает длительное воздействие месалазина на слизистую оболочку толстой кишки [18–20]. ММХ®-система препарата Мезавант позволяет создать высокую концентрацию месалазина в СОТК за счет прицельной доставки, адгезии и равномерного распределения месалазина на всем протяжении толстой кишки, включая прямую. Результаты исследования демонстрируют, что спустя 330 мин происходит высвобождение вещества в восходящей и/или в поперечной ободочной кишке; через 390 и 450 мин месалазин распределяется по всей кишке вследствие постепенного высвобождения вещества мультиматричной системы [20] (рис. 1).
 Мезавант принимается 1 раз/сут в дозе 1200/2400/3600/4800 мг месалазина, в отличие от других пероральных препаратов месалазина, которые доступны в форме таблеток в дозе по 400 или 500 мг и которые необходимо принимать 3–4 раза/ сут. Обычный режим приема препарата Мезавант – прием 2–4 таблеток 1 раз/сут, что может показать лучшую приверженность пациента лечению при сравнении с другими вариантами. В свою очередь, лучшая приверженность может снижать риск развития рецидива заболевания и уменьшать потребность в хирургических вмешательствах, госпитализации и связанными с этим экономическими затратами на лечение больных ЯК [21].
Мезавант принимается 1 раз/сут в дозе 1200/2400/3600/4800 мг месалазина, в отличие от других пероральных препаратов месалазина, которые доступны в форме таблеток в дозе по 400 или 500 мг и которые необходимо принимать 3–4 раза/ сут. Обычный режим приема препарата Мезавант – прием 2–4 таблеток 1 раз/сут, что может показать лучшую приверженность пациента лечению при сравнении с другими вариантами. В свою очередь, лучшая приверженность может снижать риск развития рецидива заболевания и уменьшать потребность в хирургических вмешательствах, госпитализации и связанными с этим экономическими затратами на лечение больных ЯК [21].
Высокая приверженность лечению ЯК связана с низкой вероятностью рецидивов заболевания, что было показано во многих опубликованных результатах исследований. Пациенты, неприверженные терапии 5-АСК, имеют в 5 раз более высокий риск рецидива [22]. Одним из аспектов, влияющих на высокую приверженность лечению, является частота приема препарата. Например, Kane и соавт. сообщили следующие результаты о приверженности поддерживающей терапии у пациентов ЯК: 39% при двукратном, 27% при трехкратном и 6% при четырехкратном приеме. Более того, авторы изучали взаимодействие между приверженностью лечению и эффективностью терапии и выявили, что приверженные терапии пациенты в 89% случаев сохраняли ремиссию заболевания по сравнению с пациентами, которые не были привержены терапии (39%) [22].
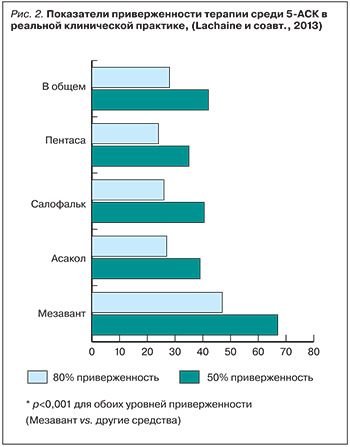
Приверженность терапии 5-АСК представляется основой для достижения лучших результатов лечения у пациентов с ЯК и по-прежнему является определяющим фактором, ассоциированным с рецидивом заболевания. Применение 5-АСК 1 раз/ сут предпочтительно для поддерживающей терапии у пациентов с ЯК [8]. M.A. Kamm и соавт. показали, что поддерживающая терапия Мезавантом в течение 12 мес продемонстрировала отсутствие рецидивов у 9 из 10 пациентов, сохранение заживления СОТК у 8 из 10 пациентов в течение года [23]. Приверженность лечению препаратом Мезавант за 1 год наблюдения была значительно выше по сравнению с приверженностью лечению любым другим препаратом 5-АСК (71,9 против 42,8% для Пентасы до 47,5% для Асакола; р<0,001). Общая приверженность лечению в течение 12 мес для 5-АСК в целом составила 45,5% (рис. 2). Были идентифицрованы факторы, определяющие приверженность лечению. Они включают: пол, возраст, прием кортикостероидов, влияние сопутствующего диагноза иного хронического заболевания. Например, результаты регрессионного анализа показали, что мужчины пожилого возраста (>60), принимающие кортикостероиды, имели более высокую приверженность приему 5-АСК [21].
 Что касается нашего исследования, пациенты принимали Мезавант (месалазин ММХ) 1–2 раза/сут (поддержание ремиссии/обострение), тогда как другие месалазины принимали 3–4 раза/сут для лечения обострения заболевания и 2 раза/сут при поддерживающей терапии. Суточные дозировки месалазина расчитаны на основании Российских клинических рекомендаций.
Что касается нашего исследования, пациенты принимали Мезавант (месалазин ММХ) 1–2 раза/сут (поддержание ремиссии/обострение), тогда как другие месалазины принимали 3–4 раза/сут для лечения обострения заболевания и 2 раза/сут при поддерживающей терапии. Суточные дозировки месалазина расчитаны на основании Российских клинических рекомендаций.
Цель исследования: сравнить эффективность лечения больных ЯК, получающих месалазин ММХ в качестве монотерапии и другие месалазины для системного и местного применения (микроклизмы, суппозитории, ректальная пена).
МАТЕРИАЛЫ И МЕТОДЫ
В отделе патологии кишечника ГБУЗ МКНЦ ДЗМ мы провели сравнительный клинический анализ результатов лечения больных ЯК, получающих месалазин ММХ и другие месалазины для системного и местного применения (микроклизмы, суппозитории, ректальная пена). Диагноз ЯК был подтвержден с помощью колоноскопии, ирригографии, гистологического исследования. Были обследованы 13 больных ЯК, получавших месалазин ММХ (Мезавант) в качестве монотерапии (1-я группа), из них 5 (38,5%) мужчин и 8 (61,5%) женщин. Возраст больных составил от 23 до 54 лет, в среднем 36,5±2,5 года. Эффективность терапии в 1-й группе больных сравнили с 25 пациентами ЯК, получавших месалазины per os (Салофальк, Пентаса, Месакол) и местно в виде микроклизм, суппозиториев или ректальной пены, из 2-й группы – 13 (52,0%) мужчин и 12 (48,0%) женщин. Возраст больных составил от 19 до 58 лет, в среднем 31,6±3,1 года. Курильщиков в изученных группах больных не было.
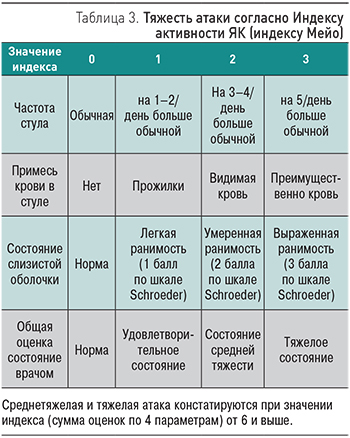
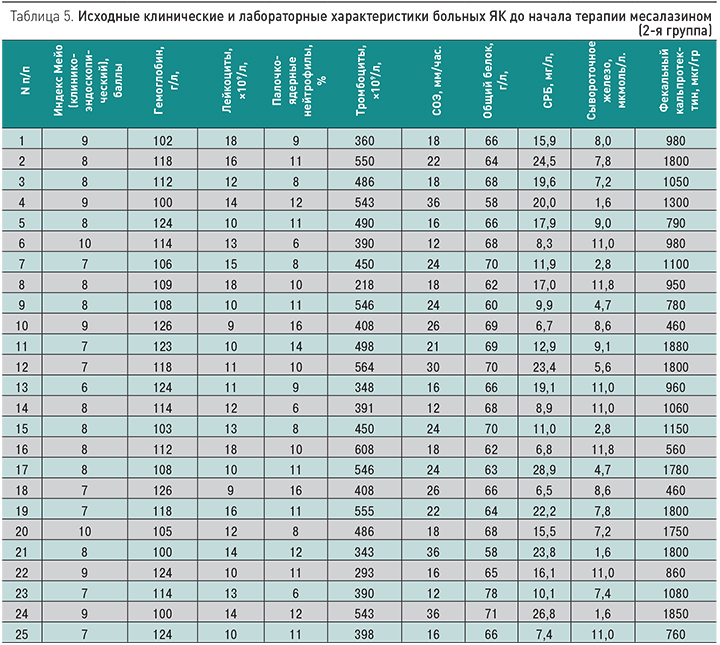
Все больные обеих групп 38 (100,0%), включенные в исследование, имели среднетяжелую степень заболевания, согласно критериям Truelove-Witts: частота стула ≥4 раз/сут; пульс ≤90 уд./мин; температура тела ≤37,5°С; уровень Hb ≥105 г/л; СОЭ ≤30 мм/ч; уровень С-реактивного белка (СРБ) не выше 30 мг/л. Основные демографические, клинические и лабораторные характеристики больных ЯК обеих групп представлены в табл. 1, 2. Лечебные мероприятия включали в себя назначение лекарственных препаратов, психосоциальную поддержку и диетические рекомендации. Выбор вида консервативного лечения определялся тяжестью атаки, протяженностью поражения толстой кишки, наличием внекишечных проявлений, длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений ЯК. Целью терапии является достижение и поддержание ремиссии, профилактика осложнений ЯК, предупреждение хирургических операций при прогрессировании процесса и развития опасных для жизни осложнений [1]. Эффективность терапии оценивали по наличию ответа на терапию месалазинами, потребности в глюкокортикостероидах, частоте рецидива заболевания в течение 52 нед, а также по баллу индекса Мейо (клинико-эндоскопическому) [24] (табл. 3), уровню гемоглобина, лейкоцитов, лейкограмме, тромбоцитов, СОЭ, общего белка, СРБ, сывороточного железа, фекального кальпротектина, с интервалом 12, 26 и 52 нед. Исходные показатели индекса Мейо и основных лабораторных показателей обеих групп пациентов представлены в табл. 4, 5. Время наблюдения за пациентами составило 52 нед. В качестве конечных точек исследования, т.е. показателей эффективности терапии, были использованы: 1) наличие ответа на терапию через 2 нед от начала терапии; 2) достижение и поддержание клинической ремиссии (стойкая ремиссия) на протяжении полугода и года после начала терапии; 3) отсутствие повторных госпитализаций по поводу обострения ЯК и колэктомии в течение года после начала терапии. Клиническую ремиссию констатировали при исчезновении примеси крови в стуле и снижении частоты дефекаций до 3 раз/сут и менее. Все пациенты подписали информированное согласие на участие в исследовании. Статистическая обработка полученных результатов проводилась с использованием пакетов статистической программой IBM SPSS Statistics версии 14.0 и версии 20.0.
 РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Через 2 нед от начала терапии месалазином ММХ 1 пациент (7,7%) не ответил на терапию. В связи с прогрессирующим ухудшением состояния, продолжавшейся кровавой диареей, анемией, лейкоцитозом, повышением уровнем СРБ, СОЭ и прокальцитонина и фекального кальпротектина ему были назначены ГКС по схеме в соответствии с клиническими рекомендациями [1]. Во 2-й группе пациентов, которым была назначена терапия месалазинами, не ответили на терапию 3 пациента (12,0%). 12 (92,3%) из 13 пациентов ответили на терапию месалазином ММХ и продолжили лечение в качестве монотерапии (без микроклизм и суппозиториев). 23 (92,0%) из 25 пациентов 2-й группы ответили на терапию месалазинами и продолжили лечение с применением местных аминосалицилатов (микроклизм и суппозиториев) в сочетании с пероральными 5-АСК в дозах, рекомендуемых национальными рекомендациями по диагностике и лечению взрослых больных ЯК. При полученном ответе на терапию, направленную на купирование обострения ЯК, пролонгировали до 10–12 нед. При достижении ремиссии в 1-й группе проводилась поддерживающая терапия месалазином ММХ 2,4 г/ сут, во 2-й группе – месалазином 1,5–2,0 г/ сут внутрь + месалазин в клизмах по 2 г 2 раза/ нед.
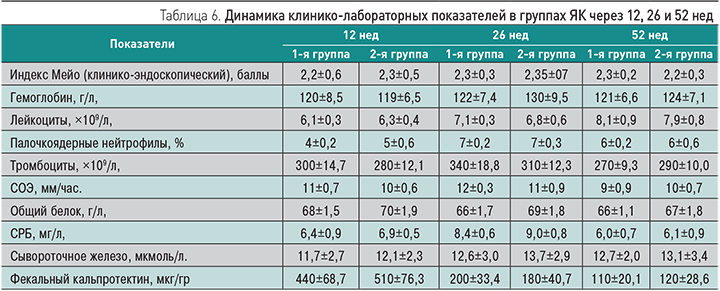
Через 12 недель у 4 (33,3%) из 12 больных 1-й группы, ответивших на терапию месалазином ММХ, достигнута клиническая ремиссия, у 8 (66,7%) клинико-эндоскопическая ремиссия, индекс Мейо в группе в среднем снизился с 7,9±0,98 до 2,2±0,6 балла. У больных ЯК 2-й группы у 14 (60,9%) из 23, ответивших на терапию месалазином ММХ, достигнута клиническая ремиссия, у 9 (39,1%) клинико-эндоскопическая ремиссия, индекс Мейо в группе в среднем снизился с 8,0±0,97 до 2,3±0,5 балла. Динамика основных лабораторных показателей представлена в табл. 6.
Через 26 нед мы провели интегрированный анализ исследования противорецидивной и поддерживающей терапии больных ЯК. Поддерживающая фаза следовала сразу через 12 нед после противорецидивной терапии. Индекс Мейо в группе больных сохранялся в среднем на уровне 2,2–2,3 балла. Увеличилось количество больных с заживлением слизистой оболочки кишки до 6 пациентов ЯК в 1-й и до 11 пациентов – во 2-й группе. Таким образом, клинико-эндоскопическая ремиссия достигнута у 50% больных ЯК как в 1-й, так и во 2-й группе. Основные клинико-лабораторные показатели в среднем оставались в пределах референсных значений (табл. 6).

Через 10 мес от начала терапии месалазином ММХ у 1 больного (8,3%), достигшего клинической ремиссии ЯК, произошел рецидив заболевания: индекс Мейо повысился до 10 баллов, частота стула до 8 раз/сут с примесью крови, гемоглобин снизился до 100 г/л, лейкоциты – 13×109/л, тромбоциты – 555×109/л, СОЭ – 36 мм/час, СРБ – 21 мг/л, сывороточное железо – 8 мкмоль/л, уровень фекального кальпротектина составил >1800 мкг/г. Больному назначена терапия ГКС в рекомендуемых дозах.
Во 2-й группе в период между 7-м и 10-м мес наблюдения рецидив произошел у 2 больных ЯК (8,7%), достигших клинической ремиссии ЯК. Индекс Мейо повысился до 10 и 11 баллов, частота стула до 8–12 раз/сут с примесью крови, гемоглобин снизился до 101 и 88 г/л, лейкоциты – 16×109/л и 11×109/л, тромбоциты – 431×109/л и 380×109/л, СОЭ – 30 и 45 мм/час, СРБ – 14 и 20 мг/л соответственно, уровень фекального кальпротектина составил в обоих случаях >1800 мкгр/гр. Одному больному назначена терапия ГКС в рекомендуемых дозах, второму – терапия ГИБП.
 Таким образом, через год от начала монотерапии месалазином ММХ клиническая ремиссия сохранялась у 5 (41,6%) больных из 12, ответивших на терапию, клинико-эндоскопическая ремиссия – у 6 (50,0%) пациентов с ЯК, у 1 (8,3%) произошел рецидив в течение года наблюдения. Во 2-й группе больных ЯК, получавших местные формы месалазинов (микроклизмы и суппозитории) в сочетании с пероральными месалазинами, клиническая ремиссия сохранялась у 10 (43,5%) больных из 23, ответивших на терапию, клинико-эндоскопическая ремиссия – у 11 (47,8%) пациентов с ЯК, у 2 (8,7%) произошел рецидив в течение года наблюдения. При сравнении продолжительности ремиссии среди пациентов ЯК, получавших месалазин ММХ, и пациентов, получавших местные формы месалазинов (микроклизмы и суппозитории) в сочетании с пероральными месалазинами, статистически достоверной разницы не было (р=0,45) (рис. 3).
Таким образом, через год от начала монотерапии месалазином ММХ клиническая ремиссия сохранялась у 5 (41,6%) больных из 12, ответивших на терапию, клинико-эндоскопическая ремиссия – у 6 (50,0%) пациентов с ЯК, у 1 (8,3%) произошел рецидив в течение года наблюдения. Во 2-й группе больных ЯК, получавших местные формы месалазинов (микроклизмы и суппозитории) в сочетании с пероральными месалазинами, клиническая ремиссия сохранялась у 10 (43,5%) больных из 23, ответивших на терапию, клинико-эндоскопическая ремиссия – у 11 (47,8%) пациентов с ЯК, у 2 (8,7%) произошел рецидив в течение года наблюдения. При сравнении продолжительности ремиссии среди пациентов ЯК, получавших месалазин ММХ, и пациентов, получавших местные формы месалазинов (микроклизмы и суппозитории) в сочетании с пероральными месалазинами, статистически достоверной разницы не было (р=0,45) (рис. 3).
За год наблюдения в обеих группах больных, достигших ремиссии, не было отмечено ни одного случая хирургического вмешательства, а также повторной госпитализации по поводу обострения заболевания. Безопасность и переносимость являются важными аспектами поддерживающей терапии. Приведенный нами анализ также продемонстрировал, что месалазин ММХ хорошо переносится у пациентов с ЯК, непредвиденные нежелательные реакции отсутствовали.
ЗАКЛЮЧЕНИЕ
Месалазин является препаратом первой линии лечения ЯК легкой и средней степени тяжести [26]. Лечение активного ЯК умеренной степени тяжести должно начинаться с перорального месалазина >2 г/день в сочетании с местным месалазином [26]. Результаты нашего исследования показали, что длительный непрерывный прием месалазина ММХ в течение года в качестве монотерапии сопоставим по своей эффективности с месалазинами для системного (per os) и местного применения (микроклизмы, суппозитории). Приверженность терапии по-прежнему является определяющим фактором, ассоциированным с риском рецидива. Применение 5-АСК 1 раз/сут предпочтительно для поддерживающей терапии у пациентов с ЯК [8].
Прием препарата Мезавант продемонстрировал, что он обладает лучшей приверженностью и удержанием на терапии по сравнению с другими препаратами группы 5-АСК [21].
В нашем исследовании в анализируемые группы были включены больные ЯК, которые достигли полной клинико-эндоскопической ремиссии, а также, возможно, и те, у кого не было достигнуто полного заживления слизистой оболочки кишки. Чтобы подтвердить наши выводы о сопоставимости монотерапии месалазином ММХ с месалазинами для системного (per os) и местного (микроклизмы, суппозитории, ректальная пена) применения, необходимо провести рандомизированные контролируемые исследования.



