ВВЕДЕНИЕ
Синдром раздраженного кишечника (СРК) – хроническое функциональное заболевание кишечника, при котором боль в животе связана с дефекацией, изменением частоты и характера стула [1]. Этиология и патогенез этого синдрома изучены недостаточно. В качестве предполагаемых механизмов развития СРК рассматривают нарушение строения и функции слизисто-эпителиального барьера желудочно-кишечного тракта (ЖКТ) вследствие полиморфизма генов, ответственных за синтез его различных компонентов, перенесенные острые кишечные инфекции, антибиотикотерапию, изменения в составе микробиоты, психоэмоциональный стресс и особенности рациона [2]. Изменение микробиоты в сочетании с нарушением функции слизисто-эпителиального барьера вызывает формирование воспалительных изменений в кишечной стенке. Хроническое воспаление нарушает механизм висцеральной чувствительности, что приводит к гиперактивации высших нервных центров (прежде всего лимбической системы) с усилением эфферентной иннервации кишечника. Это, в свою очередь, влечет за собой возникновение спазма гладкой кишечной мускулатуры и развитие симптомов заболевания. Сопутствующие эмоциональные нарушения (тревожность, депрессия, соматизация) способствуют формированию «порочного круга», когда больной акцентируется на соматических симптомах, что еще в большей степени усиливает их [3].
СРК страдают от 10 до 13% населения. Доля лиц, испытывающих симптомы, соответствующие этому синдрому, вероятно, выше, однако лишь 25–30% из них обращаются за медицинской помощью. СРК чаще беспокоит женщин, в большинстве случаев этот диагноз устанавливается в возрасте от 30 до 50 лет. У значительной части пациентов (13–87%) СРК сочетается с функциональной диспепсией [4].
В настоящее время накапливается все больше доказательств относительно как прямого, так и косвенного влияния кишечной микробиоты на развитие СРК. Известно, что 10% пациентов с разными формами СРК имеют в анамнезе эпизод инфекционной диареи (постинфекционный СРК), во время которой происходит изменение нормальной микробиоты кишечника [5]. Также установлена связь между приемом антибиотиков широкого спектра действия и формированием СРК [6]. Микробиота активно взаимодействует с внешними факторами, которые проявляют свое действие при соблюдении пациентами некоторых форм диеты [7].
Указанные факторы приобрели особую актуальность в связи с охватившей мир пандемией COVID-19, которая оказывает значительное влияние на микробный состав кишечной флоры посредством различных прямых и косвенных механизмов, способствуя возрастанию числа пациентов с постинфекционным СРК [8]. В связи с этим представляет интерес оценка возможности применения современных пробиотиков в лечении пациентов с этой разновидностью СРК.
Цель исследования – оценить эффективность включения пробиотических препаратов в терапию пациентов с постинфекционным СРК (ПИ-СРК) после перенесенной инфекции COVID-19.
МАТЕРИАЛ И МЕТОДЫ
Нами были обследованы 64 пациента с ПИ-СРК, развившимся после перенесенной инфекции COVID-19, которые проходили обследование в лечебном учреждении Республики Ингушетия.
Критерии включения: пациенты в возрасте от 25 до 55 лет, соответствовавшие диагностическим критериям СРК и подписавшие форму информированного согласия после полного информирования о цели и процессе исследования.
Критерии исключения:
- воспалительная и органическая патология кишечника, такая как туберкулез этого органа, синдром мальабсорбции, целиакия;
- хирургические операции на брюшной и тазовой области в анамнезе;
- некишечные заболевания пищеварительной системы (хронический панкреатит, опухоли, язвенная болезнь, хронические диффузные заболевания печени);
- другие тяжелые заболевания, включая тяжелые поражения жизненно важных органов (сердце, легкие и почки);
- беременные или кормящие женщины.
Среди пациентов было равное количество мужчин и женщин (по 50%). Средний возраст больных составил 35 ± 5лет, анамнез заболевания – 0,8±0,3 года. Дебют заболевания все пациенты связывали с перенесенной инфекцией COVID- 19, подтвержденной обследованием. Всем больным после завершения курса лечения по поводу COVID-19 проводился двукратный ПЦР-анализ на SARS-CoV-2.
Пациенты были разделены на 2 группы. Основную группу составили 32 человека, которым проводилось лечение СРК в соответствии с последними рекомендациями Российской гастроэнтерологической ассоциации, включая применение спазмолитиков и противодиарейных средств. Дополнительно пациентам этой группы в течение 2 нед назначались пробиотики в стандартной дозировке. В группу контроля вошли 32 пациента, получавшие лечение без добавления пробиотика.
Шкалу тяжести симптомов СРК (IBS-SSS) [4] использовали для оценки степени тяжести абдоминальной боли, частоты болей в животе, степени тяжести вздутия живота, неудовлетворенности работой кишечника и качеством жизни.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации Всемирной медицинской ассоциации. У всех пациентов было получено письменное информированное согласие на участие в исследовании. При заборе и обработке медицинских документов были соблюдены все этические нормы.
Ввод данных в региональном исследовательском центре производился в системе ACCESS MS OFFICE. Статистический анализ результатов осуществлялся с использованием программы SPSS 22.0.
РЕЗУЛЬТАТЫ
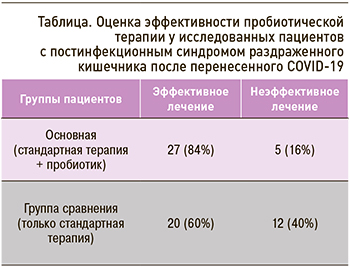
У пациентов основной группы, получавших в рамках комплексной терапии пробиотики, отмечалась более высокая частота избавления от клинических проявлений ПИ-СРК. Эффективность лечения (показатели снижения выраженности симптомов заболевания) составила 84% в основной группе против 60% в группе сравнения (табл.).
До проведения лечения у пациентов двух групп показатели в баллах по тесту IBS-SSS существенно не отличались. После курса терапии в обеих группах исследования отмечалось статически значимое улучшение показателей оценки тяжести кишечных симптомов, при этом самыми низкими показатели были в основной группе по сравнению с группой сравнения.
ОБСУЖДЕНИЕ
СРК является очень распространенным заболеванием с пока еще не ясными механизмами, включающими генетические, физиологические и психологические факторы, которые могут быть прямо или косвенно связаны с изменением состава микробиоты кишечника. Кишечная микробиота вносит вклад в патогенез СРК, влияя на иммунную систему ЖКТ, проницаемость слизистой оболочки кишки, кишечную моторику, висцеральную чувствительность; следовательно, терапия, нацеленная на кишечную микробиоту, в частности применение пробиотиков, может быть многообещающим направлением в лечении пациентов с СРК.
ЗАКЛЮЧЕНИЕ
Таким образом, пробиотики могут рассматриваться как перспективные препараты при лечении пациентов с постковидным ПИ-СРК, способствующими регрессу клинических проявлений заболевания и улучшению показателей качества жизни.


