Кашель – одна из самых частых причин обращения к врачу первичного звена пациентов любого возраста. Он является мультидисциплинарной проблемой, что связано с множеством причин его развития. Среди них болезни органов дыхания, ЛОР-органов, сердечно-сосудистой системы, желудочно-кишечного тракта, курение, прием ряда лекарственных препаратов и др. [1].
Чаще всего кашель вызывают острые респираторные инфекции (ОРИ). Повышение чувствительности ирритативных рецепторов и нарушение мукоцилиарного клиренса в результате вирус-индуцированного воспаления служат причинами кашля, физиологическая роль которого заключается в восстановлении нормальной проходимости дыхательных путей [1–4]. В первые дни ОРИ сухой, надсадный, нарушающий дневную активность и ночной сон кашель требует активного лечения [1, 3, 4].
Лечение кашля после установления его причины должно быть этиотропным и патогенетическим. При ОРИ вирусной этиологии проведение этиотропной терапии затруднено ввиду отсутствия противовирусных препаратов целенаправленного действия. Отхаркивающие, муколитические и противокашлевые препараты являются симптоматическими средствами. Современные подходы к лечению кашля складываются из мероприятий по улучшению дренажной функции бронхов и восстановлению адекватного мукоцилиарного клиренса [3, 5].
Задача врача состоит в выборе лекарственного препарата в зависимости от клинической ситуации в пользу терапии, повышающей эффективность кашля (протуссивной), или предупреждении и устранении кашля (антитуссивной) [1]. Кроме того, необходимо учитывать тот факт, что ключевым фактором патогенеза кашля при ОРИ является воспалительная реакция дыхательных путей.
Являясь защитным рефлексом, кашель может вызывать выраженный дискомфорт и негативно влиять на качество жизни пациента. В этих случаях применяют противокашлевые препараты центрального и периферического действия, которые улучшают самочувствие и уменьшают риск возникновения осложнений кашля [1, 3, 4, 6, 7]. Однако длительность применения препаратов этой группы ограничена ввиду изменения характера кашля и опасности застоя секрета в дыхательных путях и его инфицирования. Для последующей терапии необходима смена препарата на лекарственное средство с протуссивной активностью.
Выходом из подобной ситуации может стать применение комбинированного противокашлевого препарата, выбор которого в настоящее время ограничен. Международные руководства рекомендуют для расширения возможностей терапии кашля при ОРИ создание и проведение клинических исследований новых эффективных и безопасных многокомпонентных, в том числе безрецептурных, лекарственных средств для лечения кашля [8].
Ренгалин (ООО «НПФ «Материа Медика Холдинг») – комплексный препарат для лечения кашля. Активными компонентами его служат антитела в релиз-активной форме к брадикинину (РА АТ к брадикинину), гистамину (РА АТ к гистамину) и морфину (РА АТ к морфину). Фармакологические эффекты препарата обеспечиваются высвобождением особой активности (релиз-активности) в результате технологической обработки исходных антител к молекулам-регуляторам, влияющим на различные звенья кашлевого рефлекса [9]. Ренгалин модифицирует эндогенные молекулы (брадикинин, гистамин и эндогенные опиоиды), изменяя их взаимодействие со своими рецепторами, участвующими в формировании кашля [10–14]. Препарат тормозит центральные звенья кашлевого рефлекса и блокирует передачу болевых импульсов к коре головного мозга, оказывая влияние на кашлевой центр и афферентные нервные волокна дыхательных путей. Ренгалин уменьшает гиперреактивность бронхов, оказывает противовоспалительное, противоотечное, антиаллергическое, спазмолитическое действие, что способствует устранению раздражения слизистой дыхательных путей, а также улучшению дренажной функции бронхов и отхождению мокроты, т.е. оказывает протуссивный эффект. Препарат не вызывает угнетения дыхания, привыкания, лекарственной зависимости, не обладает наркогенным и снотворным действием [12–14].
Ренгалин выпускается в виде таблеток для рассасывания и разрешен к применению у взрослых и детей с 3-летнего возраста. Новая жидкая лекарственная форма была специально разработана как наиболее удобная для дозирования и применения у пациентов различного возраста. В данной публикации представлены результаты завершенного клинического исследования новой жидкой лекарственной формы Ренгалина (раствора для приема внутрь).
Целью настоящего клинического исследования стала оценка безопасности и клинической антитуссивной (противокашлевой) и протуссивной (оптимизирующей кашель) эффективности жидкой лекарственной формы препарата Ренгалин в лечении кашля при ОРИ верхних дыхательных путей у взрослых пациентов.
Материал и методы
Дизайн исследования. Проведено рандомизированное параллельно-групповое двойное слепое плацебо-контролируемое проспективное многоцентровое клиническое исследование III фазы. Перед началом процедур все участники исследования подписывали форму информированного согласия на участие в клиническом исследовании.
В целях сохранения конфиденциальности каждому пациенту при рандомизации присваивался персональный код. Рандомизация проводилась с помощью генератора случайных чисел, исходя из соотношения исследуемых групп 1:1. Участники, соответствующие критериям включения/невключения, были рандомизированы в две группы: пациенты 1 группы принимали Ренгалин по схеме в течение 7 дней, пациенты 2 группы – плацебо по схеме приема Ренгалина. В данном исследовании применялся двойной слепой дизайн. Раствор Ренгалина и плацебо имели одинаковый вид и органолептические свойства. Начиная с четвертого дня пациентам обеих групп при наличии показаний (кашель с отделением вязкой мокроты) врач назначал муколитик амброксол (Лазолван®, Boehringer Ingelheim International (Германия)). Наблюдение за пациентами продолжалось еще в течение 3 дней, общая продолжительность лечения и наблюдения составила до 8 сут. Пациенты трижды осматривались врачом: на 1-й (визит 1), 4-й (визит 2) и 8-й (визит 3) дни. В течение 7 сут пациенты вели дневник, заполняли размещенную в нем «Шкалу тяжести кашля», регистрировали число эпизодов дневного и ночного кашля, описывали характер кашля (сухой/непродуктивный или влажный/продуктивный), результаты измерения температуры тела утром и вечером. Исходно и по завершении терапии проводились лабораторные исследования, регистрировали наличие и характер нежелательных явлений (НЯ) в период терапии, их связь с приемом препарата.
Критерии соответствия. Критериями включения амбулаторных пациентов от 18 лет и старше в исследование были клинические симптомы ОРИ верхних дыхательных путей – острого фарингита, ларингита, ларинготрахеита, трахеита. Выраженность непродуктивного кашля, которую оценивали по сумме дневного и ночного кашля в баллах по специализированной «Шкале тяжести кашля» [1, 15], должна была составлять ≥ 4 баллов (частый, болезненный кашель, оказывающий влияние на повседневную активность либо нарушающий ночной сон) за предшествующие 24 ч, продолжительность кашля – от 12 ч до 3 дней: все это являлось показанием для назначения противокашлевой терапии. Обязательным условием было применение и соблюдение методов контрацепции пациентами репродуктивного возраста обоего пола.
Пациент не включался в исследование, если:
- на момент включения он нуждался в назначении мукоактивных препаратов;
- у него отмечался влажный/продуктивный кашель, ОРИ нижних дыхательных путей, острая дыхательная недостаточность;
- имелось подозрение на бактериальную инфекцию, в том числе пневмонию;
- наблюдалось обострение/декомпенсация хронических заболеваний, включая хронические заболевания органов дыхания.
Кроме того, критериями невключения были наличие в анамнезе хронических заболеваний центральной нервной системы (воспалительных, дегенеративных, полиневропатии, эпилепсии), злокачественных новообразований, сахарного диабета, наследственной непереносимости фруктозы (вследствие наличия в составе исследуемого препарата мальтитола), непереносимости любого из компонентов лекарственных препаратов, используемых в лечении, курение, употребление наркотиков, алкоголя, беременность/кормление грудью/нежелание соблюдать методы контрацепции, психические заболеваний пациента, участие в других клинических исследованиях в течение 3 предшествующих месяцев.
В процессе лечения пациентам разрешался прием препаратов для терапии ОРИ верхних дыхательных путей, а также других лекарственных средств, которые не входили в список запрещенных препаратов. К последним в исследовании были отнесены противокашлевые, антигистаминные, бронхолитические, отхаркивающие средства, глюкокортикостероиды, ингибиторы АПФ, комбинированные лекарства, содержащие Н1-гистаминоблокаторы. При этом за 1 мес до включения в исследование, а также в ходе проведения исследования (с момента подписания информированного согласия и начала скрининга) не разрешалась любая терапия, способная повлиять на выраженность кашля у пациента.
Условия проведения. Проведение рандомизированного клинического исследования было реализовано на базе 12 медицинских организаций (клинических центров), осуществляющих амбулаторно-поликлиническую помощь и расположенных в разных городах России, в том числе в Москве, Санкт-Петербурге, Ярославле, Казани, Смоленске, Челябинске.
Продолжительность исследования. Исследование проводилось в период с ноября 2012 г. по декабрь 2014 г. В связи с недостаточным набором пациентов, запланированным протоколом, исследование было пролонгировано до декабря 2016 г. Таким образом, его продолжительность составила 4 года. В соответствии с планом проводился промежуточный анализ на момент включения 52 пациентов в каждую группу в соответствии с критериями включения/невключения.
Описание медицинского вмешательства. Обследование пациентов включало определение исходной тяжести кашля (по «Шкале тяжести кашля»), осуществлялся сбор жалоб, анамнеза, оценка витальных функций, физикальное обследование, регистрировалась сопутствующая терапия, проводились лабораторные исследования для оценки безопасности проводимой терапии (клинический анализ крови, общий анализ мочи, биохимические маркеры).
Исследуемый препарат (Ренгалин или плацебо) назначался в первые три дня лечения по 2 мерных ложки (10 мл) 3 раза в сутки, затем в последующие 4 дня по 1 мерной ложке (5 мл) 3 раза в день вне приема пищи. Приверженность пациента исследуемой терапии (комплаентность) определялась на основании подсчета возвращенного препарата на заключительном визите по формуле:
N= (Qвыд. – Qвозвр.)/Qдолжн. × 100%,
где N – уровень комплаентности, Qвыд. – объем выданного раствора, Qвозвр. – объем раствора, возвращенного пациентов, Qдолжн. – необходимый объем раствора на курс лечения в соответствии со схемой лечения.
Начиная с четвертого дня пациентам обеих групп при наличии показаний (кашель с отделением вязкой мокроты) врач назначал муколитик амброксол (Лазолван®, сироп 30 мг/5 мл) по 1 чайной ложке (5 мл) 3 раза в сутки независимо от приема пищи.
Пациентам разрешался прием препаратов для терапии ОРИ верхних дыхательных путей, включая жаропонижающие, противовирусные препараты, витамины, сосудосуживающие капли в нос. При необходимости врачи назначали дезинтоксикационную терапию и антибактериальные средства (в случае развития бактериальных осложнений).
Первичными конечными точками исследования служили доли пациентов с улучшением или полным исчезновением кашля на 4 и 7 дни наблюдения. Критерием улучшения считалось снижение баллов по шкале тяжести кашля до 2 баллов днем и 1 балла ночью, критерием выздоровления – полное отсутствие кашля в течение суток. Кроме того, оценивались длительность сухого/непродуктивного кашля и сроки появления первых эпизодов продуктивного кашля, а также общая продолжительность кашля. Вторичными конечными точками были динамика выраженности кашля и катарального синдрома в целом, других синдромов ОРИ (лихорадочного, общеинтоксикационного), частота генерализации респираторной инфекции и бактериальных осложнений, степень удовлетворенности препаратом лечащими врачами.
Анализ в подгруппах в настоящем клиническом исследовании не был запланирован.
Методы регистрации результатов лечения. Для определения выраженности кашля применяли специализированную 6-точечную шкалу оценки его тяжести (0 баллов – отсутствие кашля, 5 баллов – тяжелый кашель) [1, 15]. Пациенты регистрировали в дневнике число эпизодов дневного и ночного кашля, описывали характер кашля (сухой/непродуктивный или влажный/продуктивный), результаты измерения температуры тела утром и вечером. Общая продолжительность кашля определялась как количество дней, потребовавшихся для излечения пациента. Показатель рассчитывался исходя из положения об отсутствии кашля при уровне суммарной оценки дневного и ночного кашля равной 2 баллам. Выраженность других симптомов ОРИ оценивалась по 4-балльной шкале, где 0 – отсутствие симптома, 1 – легкая, 2 – средняя, 3 – тяжелая степень. Оценка эффективности лечения проводилась на основании индекса эффективности шкалы общего клинического впечатления (Clinical Global Impression Scale − Efficiency Index, CGI-EI), отражающего терапевтическую эффективность и частоту побочных эффектов проводимой терапии.
Этическая экспертиза. Исследование проводилось согласно полученному разрешению Минздрава России № 523 от 20.11.2012 и № 463882-20-1 от 05.11.2014 г. на его продление, было одобрено локальными этическими комитетами медицинских центров, на базе которых проводилось исследование.
Статистический анализ, принципы расчета размера выборки. Оценка размера выборки для анализа эффективности проводилась с учетом дизайна Superiority (проверка гипотезы о превосходстве эффективности исследуемого препарата над контрольным). Величина клинически значимого различия «δ» принималась равной 10%. Мощность статистических критериев «P=(1−β)» принималась равной 80%. Вероятность ошибки первого рода «α» допускалась менее 5% (вероятность ошибочного принятия альтернативной гипотезы – менее 0,05).
Методы статистического анализа данных. Обработка данных и все статистические расчеты по данному протоколу производились с использованием статистического пакета SAS-9.4 (Statistical Analysis System, США). При анализе первичных критериев эффективности сформулированы четыре гипотезы, в связи с чем применялись поправки на множественность (поправка Бонферрони), уровень значимости при анализе первичных критериев был установлен равным (0,05/4)=0,0125, для оцениваемых параметров были построены (100–1,25)%=98,75%-ные доверительные интервалы.
Параметрический анализ осуществлялся с помощью критерия χ2 для пропорций и T-критерия Стьюдента для непрерывных величин, непараметрический – с помощью точного критерия Фишера и критерия Краскела–Уоллиса. В результате выполнения проверки на нормальность было установлено, что длительность непродуктивного кашля и общая длительность кашля являются ненормально распределенными величинами. В связи с этим для соответствующих критериев был проведен анализ по методу Каплана–Мейера (z-тест для средних значений и логарифмический ранговый критерий для функций выживаемости). Результаты пациентов, у которых кашель не купировался полностью за время участия в исследовании или же сухой кашель не трансформировался во влажный, включались в анализ как неполные (цензурированные).
Результаты
Характеристика участников исследования. Всего подписали информированное согласие и были включены в исследование 344 пациента, на основании данных которых проводили анализ безопасности. В ходе исследования было выявлено, что 6 пациентов (4 из группы Ренгалина и 2 группы плацебо) были включены в исследование ошибочно, так как не соответствовали критериям включения либо у них присутствовали критерии невключения. Выборку для ITT-анализа эффективности составили 338 пациентов (173 пациента группы Ренгалина и 165 – из группы плацебо). Еще 20 пациентов (n=9 в группе Ренгалина и n=11 в группе плацебо) завершили участие в исследовании досрочно, их данные были исключены из анализа по разным причинам. Таким образом, выборку для PP-анализа составили 318 пациентов, в том числе 164 – группы Ренгалина и 154 – группы плацебо (результаты РР-анализа приведены в квадратных скобках). Движение пациентов в ходе исследования представлено на рис. 1.
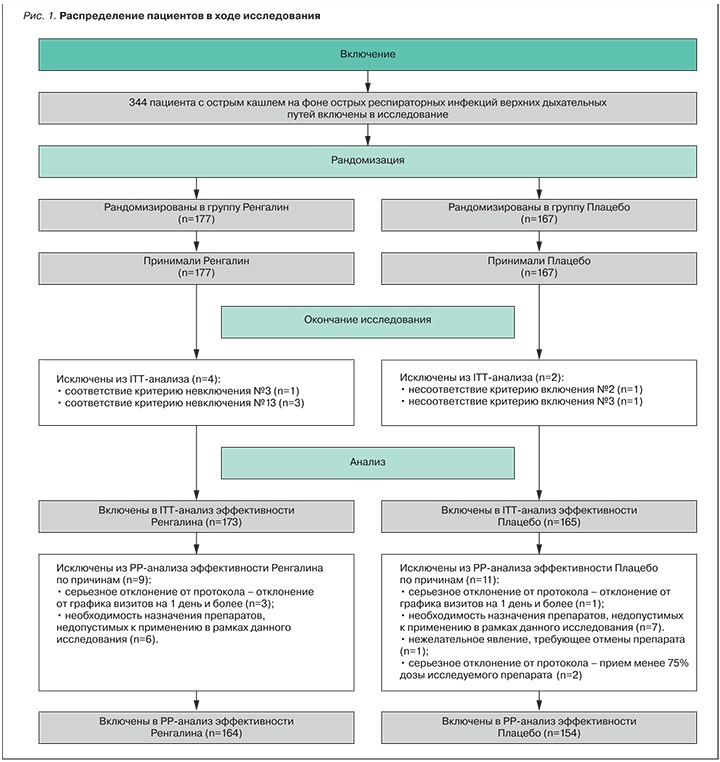
Пациенты обеих групп не имели различий по демографическим и исходным клиническим характеристикам. Демографические данные представлены в табл. 1, исходные клинические характеристики участников исследования – в табл. 2. У всех пациентов ведущим симптомом был сухой (непродуктивный) кашель, снижающий дневную активность и приводящий к нарушению или прерыванию сна, что являлось показанием для назначения противокашлевой терапии. Кроме кашля, наиболее выраженными были другие проявления катарального синдрома (назальная обструкция, ринорея, чихание, боль в горле). Различные сопутствующие заболевания имели 45,1 [45,7]% пациентов группы Ренгалина и 48,5 [50,6]% группы плацебо. Чаще других заболеваний, участники исследования имели патологию сердечно-сосудистой (13,9 и 16,3% в группах Ренгалина и плацебо), костно-мышечной системы (11,0 и 12,1%), болезни желудочно-кишечного тракта (9,8 и 10,3%) и гепатобилиарной системы (6,4 и 2,4%), органа зрения (7,5 и 3,0%). Большинство (около 90%) пациентов получали разрешенные к применению лекарственные средства, включая сосудосуживающие назальные капли и спреи, местные антисептические растворы, анальгетики, противовирусные препараты и иммуномодуляторы. По частоте сопутствующих заболеваний (р=0,821 [р=0,688]) и применения препаратов сопутствующей терапии (р=0,248 [р=0,171]) группы также значимо не различались.
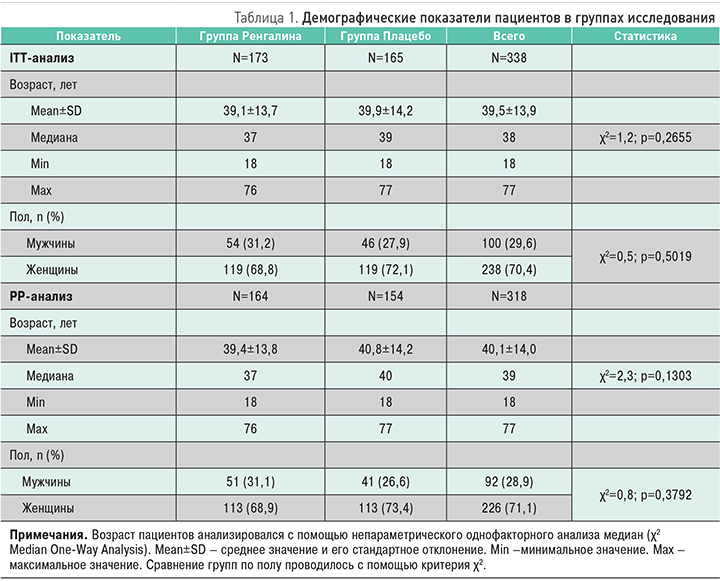
Необходимо отметить, что пациенты обеих групп, исключенные из анализа эффективности, не имели различий по исходным характеристикам выраженности симптомов ОРИ, встречаемости сопутствующих заболеваний и применению сопутствующей терапии.
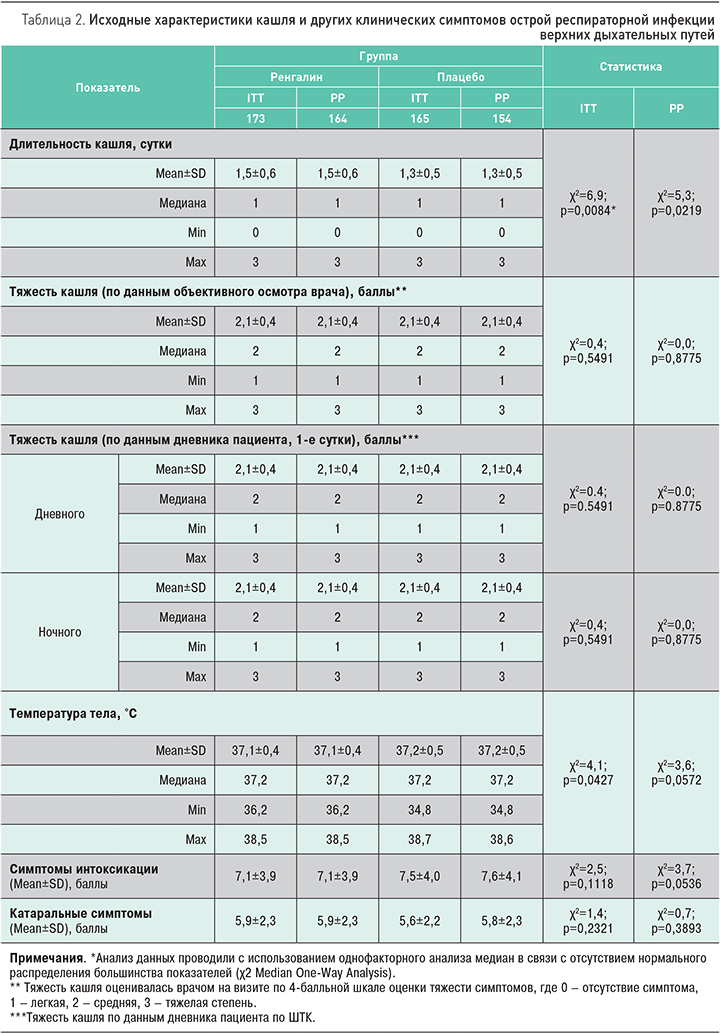
Анализ комплаентности, проведенный по результатам подсчета возвращенного препарата на последнем визите через 7 дней лечения, продемонстрировал высокий уровень приверженности пациентов назначенной терапии: 99,5±5,6 [99,9±4,4]% в группе Ренгалина и 99,0±9,8 [100,4±4,4]% в группе плацебо.
Основные результаты исследования: оценка эффективности. Результаты оценки эффективности по основным критериям представлены в табл. 3 и 4. Лечение Ренгалином увеличивало долю пациентов с улучшением или отсутствием кашля через 3 дня терапии (табл. 3). Доля таких пациентов составила 50[52]% (против 37[38]% в группе плацебо), результаты значимо различались в выборке пациентов, получивших предусмотренную протоколом терапию в полном объеме (р=0,018 [р=0,011]). Анализ полученных данных, проведенный по результатам 7-го дня лечения, также свидетельствовал о преобладании пациентов с улучшением/отсутствием кашля в основной группе, однако результаты оказались незначимыми (р=0,42 [р=0,36]).
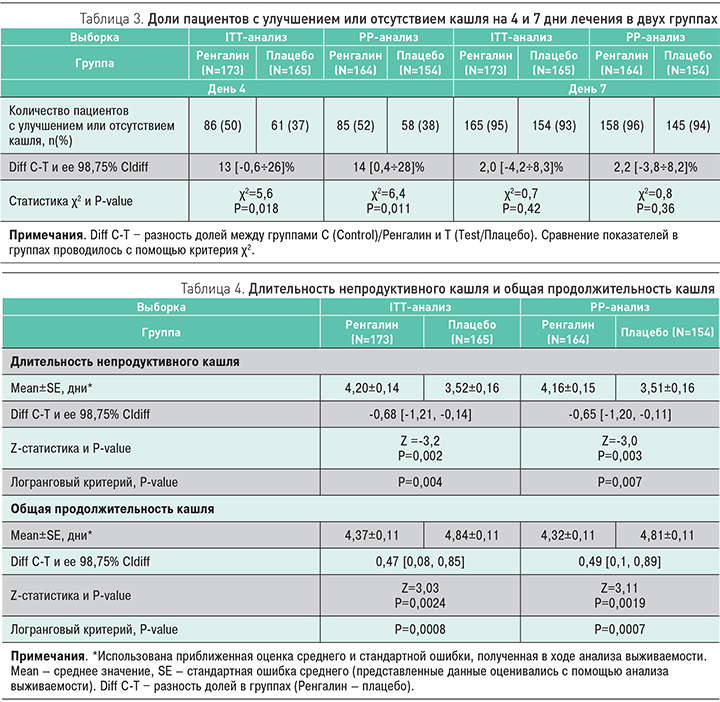
Длительность непродуктивного кашля у пациентов составила 4,20±0,14 [4,16±0,15] дней в группе Ренгалина и 3,52±0,16 [3,51±0,16] дней в группе плацебо (см. табл. 4). Необходимо отметить, что изменение характера кашля с сухого на влажный происходило лишь у 32% пациентов группы Ренгалина, у остальных пациентов, принимающих Ренгалин, кашель излечивался, минуя трансформацию во «влажный». Продолжительность непродуктивного кашля (4,20±0,14 [4,16±0,15]) и общая продолжительность кашля (4,37±0,11 [4,32±0,11]) на фоне лечения Ренгалином практически совпали (р=0,34 [р=0,39]). Вероятно, с этим фактом был связан результат сравнения продолжительности периодов непродуктивного кашля в двух группах.
Итогом терапии Ренгалином стало значимое сокращение общей длительности кашля, о чем свидетельствовали результаты статистического анализа, основанного на z-статистике (р=0,0024 [р=0,0019]), и логранговый критерий функций выживаемости (р=0,0008 [р=0,0007]).
Тяжесть кашля по результатам балльной оценки самих участников исследования прогрессивно снижалась в обеих группах (табл. 5). За 7 дней лечения выраженность дневного кашля уменьшилась до 1,0±0,9 [1,0±0,8] баллов в группе Ренгалина и 1,2±0,9 [1,2±0,9] баллов в группе плацебо, что указывало на наличие единичных (не более двух) эпизодов кашля в течение дня. В результате лечения ночной кашель уменьшился до 0,1±0,4 [0,1±0,4] баллов и 0,3±0,5 [0,3±0,6] баллов в группах Ренгалина и плацебо соответственно, что означало полное отсутствие ночного кашля или однократный эпизод кашля во время ночного сна.
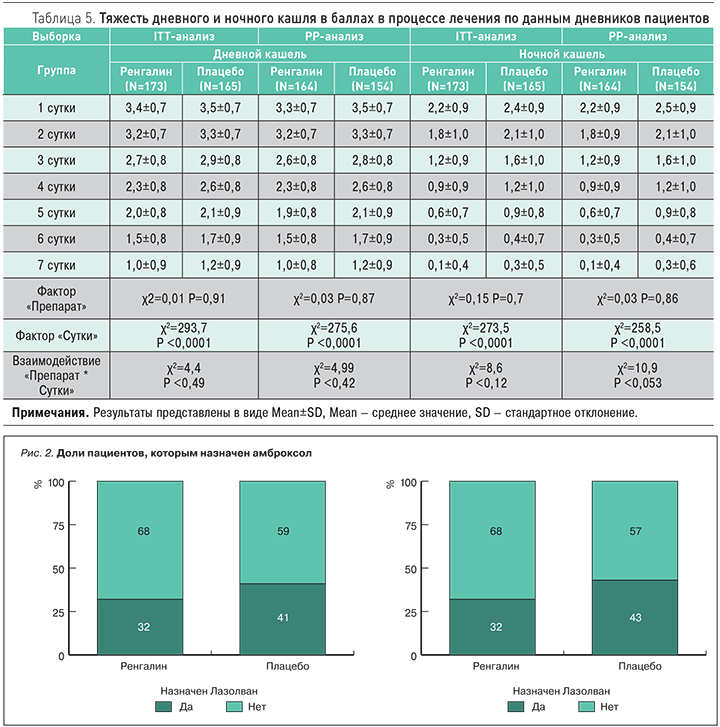
Частота эпизодов кашля в течение 7 дней лечения Ренгалином уменьшилась с 26,9±19 [26,6±19,2] до 4±8,1 [3,4±4,9]; в группе плацебо – с 23,4±15,6 [23,1±13,3] до 4,3±5,2 [4,3±5,3] (табл. 6). Наибольшая эффективность Ренгалина была отмечена в течение ночи, когда кашель существенно нарушал сон пациентов. Значимо меньшее число эпизодов ночного кашля отмечалось в период монотерапии Ренгалином, т.е. на 2 (р=0,038 [0,023]) и 3 (р=0,002 [р=0,001]) сут, а также на 4–7 сут, когда часть пациентов получала комбинацию Ренгалин + амброксол. Среднее значение показателя за весь период лечения снизилось с 3,1±2,8 [3,1±2,8] баллов до 0,1±0,4 [0,1±0,4] баллов у пациентов группы Ренгалина и с 3,2±2,1 [3,2±2,1] до 0,3±0,6 [0,3±0,6] баллов в группе плацебо, дисперсионный анализ подтверждал превосходство Ренгалина (р=0,0011 [р=0,0008]).
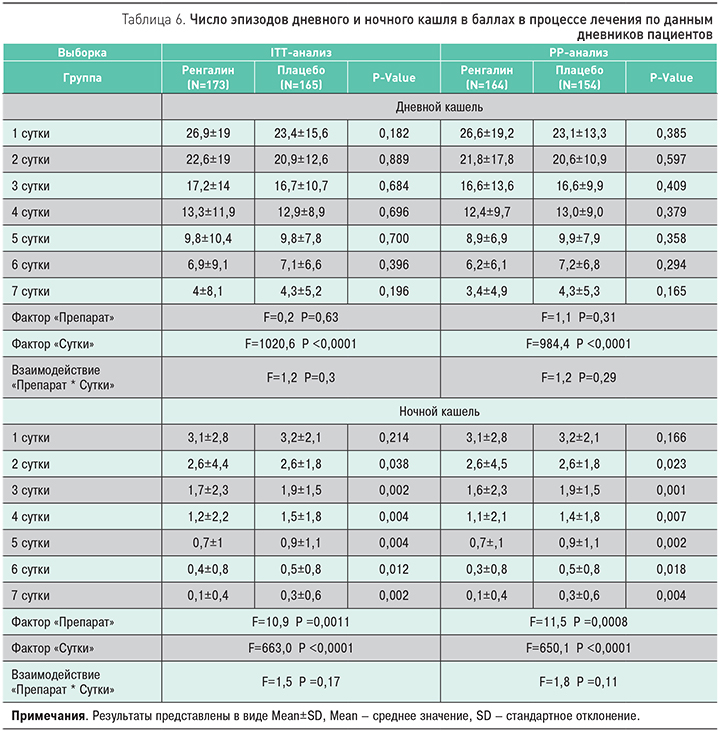
В соответствии с дизайном исследования по окончании трех дней терапии Ренгалином врач назначил муколитик амброксол 32% [32%] пациентов, после 3 дней Плацебо дополнительная муколитическая терапия понадобилась 41% [43%] участников (рис. 2). Результаты РР-анализа показали значимое преимущество исследуемого препарата над плацебо-терапией по данному показателю ([р=0,04]).
Выраженность клинических синдромов ОРИ верхних дыхательных путей прогрессивно снижалась у пациентов двух групп (табл. 7). Если на момент включения в исследование температура тела пациентов была субфебрильной, то на 4 сут – нормальной. Через 3 дня проводимой терапии состояние участников исследования характеризовалось единичными слабо выраженными симптомами интоксикации и другими, помимо кашля, проявлениями катарального синдрома. К моменту завершения курса терапии выраженность респираторной симптоматики была минимальной (0,8±1,1 [0,8±1,0] баллов и 0,9±1,2 [0,9±1,2] баллов в группах Ренгалина и плацебо соответственно). В результате 7 дней лечения интенсивность респираторных жалоб уменьшилась на –5,1±2,5 [–5,2±2,5] баллов в группе Ренгалина и на –4,7±2,3 [4,8±2,3] баллов в группе плацебо.
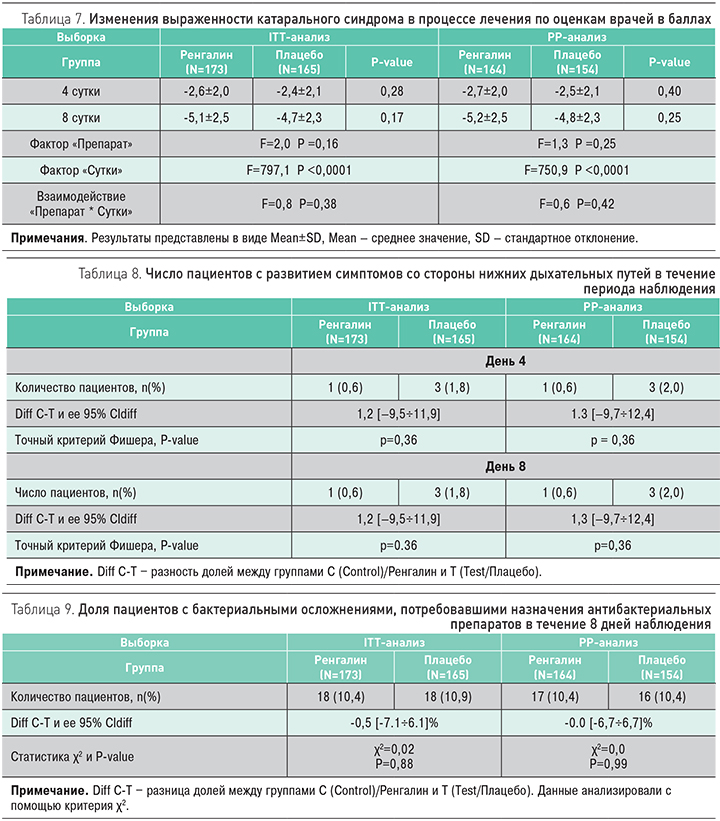
У 4 участников исследования (1 пациента в группе Ренгалина и 3 пациентов в группе плацебо) было выявлено ухудшение течения ОРИ с появлением симптомов со стороны нижних дыхательных путей (диагноз бронхит, зарегистрирован на 4 и 8 дни наблюдения) (табл. 8). Анализ с помощью точного критерия Фишера не выявил значимых различий по данному критерию (р=0,36 [р=0,36] на 4 и 8 дни]).
По частоте возникновения бактериальных осложнений острой респираторной инфекции, потребовавших назначения антибактериальных препаратов (острый синусит, трахеобронхит, увеличение числа лейкоцитов и появление оксалатов в моче и др., в ряде случаев причина не была указана), обе группы пациентов также значимо не различались (р=0,88 [р=0,99]) (табл. 9).
По оценкам врачей, терапевтическая эффективность в группе Ренгалина через 3 дня лечения (день 4) (1,6±0,6 [1,6±0,6] баллов) и всего курса терапии (2,7±0,5 [2,7±0,5] баллов) по шкале CGI-EI была значимо выше по сравнению с результатами в группе плацебо (1,5±0,7 [1,5±0,7] и 2,6±0,6 [2,6±0,6] баллов соответственно; фактор «Препарат» р=0,02 [p=0,02], фактор «Сутки» р <0,0001 [р <0,0001]).
Показатели побочных эффектов в обеих группах были низкими: 2,3 [2,4]% в группе Ренгалина против 1,2 [1,3]% в группе плацебо (р=0,69 [р=0,69]).
Оценка безопасности. Всего в течение периода лечения и наблюдения было зарегистрировано 15 случаев НЯ у 9 (5,1%) пациентов группы Ренгалина и 21 НЯ у 15 (9,0%) участников исследования группы плацебо. Частотный анализ с помощью точного критерия Фишера не выявил значимых различий между числом пациентов с НЯ (p=0,37) и частотой НЯ в двух группах.
По мнению врачей-исследователей, все зарегистрированные в обеих группах НЯ не имели определенной (достоверной) связи с исследуемой терапией; в 7 случаях НЯ в группе Ренгалина связь с исследуемой терапией отсутствовала; в 8 случаях причинно-следственная связь была маловероятной/вероятной или возможной. Среди зарегистрированных были отмечены следующие НЯ, имеющие отношение к тому или иному коду MedDRA1: инфекционное заболевание (1,1% в группе Ренгалина против 5,4% в группе плацебо, р=0,081), гастроинтестинальные расстройства (1,1% в группе Ренгалина и 0,6% в группе плацебо, р=1,0), сердечно-сосудистые расстройства (0,6 и 0% в группах Ренгалина и плацебо, р=1,0), общие расстройства (0,6 и 0% в группах Ренгалина и плацебо, р=1,0), расстройства нервной системы (1,7% в группе Ренгалина против 0% в группе плацебо, р=0,231), отклонения от нормы, выявленные при инструментальных и лабораторных исследованиях (2,8 и 3,6% в группах Ренгалина и плацебо, р=0,921).
Сочетанное использование Ренгалина с противовирусными и иммуномодулирующими препаратами, анальгетиками и антипиретиками, нестероидными противовоспалительными, антибактериальными, блокаторами кальциевых каналов, диуретиками, статинами, антагонистами рецепторов ангиотензина II, деконгестантами, муколитиком амброксолом, витаминами, комбинированными пероральными контрацептивами не приводило к развитию реакций фармакологической несовместимости, антагонистическому или взаимоусиливающему действию.
Обсуждение
Полученные в ходе исследования результаты показали, что жидкая лекарственная форма Ренгалина является эффективным средством лечения кашля у взрослых пациентов с острыми респираторными инфекциями верхних дыхательных путей. Низкая частота нежелательных явлений на фоне приема Ренгалина, значимо не отличающаяся от применения плацебо, свидетельствует о благоприятном профиле безопасности препарата Ренгалин.
Лечение Ренгалином способствовало увеличению числа пациентов с купированием непродуктивного кашля, сокращению общей продолжительности кашля при ОРИ, что значимо превосходило аналогичные показатели в группе плацебо. Необходимо отметить, что длительность непродуктивного кашля в основной группе совпадала с общей продолжительностью кашля и превосходила таковую в группе плацебо. Это, вероятно, было связано с тем, что эпизоды продуктивного (влажного) кашля появились лишь у трети пациентов группы Ренгалина и острый непродуктивный кашель излечивался без появления обильного секрета дыхательных путей. В этом заключалось отличие первых трех дней лечения Ренгалином в виде монотерапии от применения плацебо. У пациентов группы сравнения в ходе лечения появился влажный экссудат (эпизоды продуктивного кашля), и многим из них в силу наличия вязкого экссудата был назначен муколитик амброксол, который еще больше способствовал «переходу» сухого кашля во влажный. Меньший процент пациентов группы Ренгалина, нуждающихся в дополнительном назначении муколитика амброксола, а также редукция кашля, начиная со вторых суток наблюдения, свидетельствовали о купировании сухого кашля у пациентов основной группы, минуя фазу влажного кашля. Таким образом, можно говорить о большей противокашлевой эффективности препарата Ренгалин по сравнению с плацебо.
Прием препарата Ренгалин позволил уменьшить частоту и выраженность кашля, а также обеспечить более быструю динамику катарального синдрома в целом. Результатом терапии стала трансформация сухого кашля в редкий кашель, не беспокоящий больного в течение дня и ночи без образования вязкой мокроты, требовавшей дополнительного назначения муколитической терапии или полное его купирование.
Низкая частота случаев появления симптомов со стороны нижних отделов дыхательных путей при приеме Ренгалина (0,6 против 2,0% в группе плацебо) и отсутствие различий между группами (р=0,36 [р=0,36]) свидетельствовали об отсутствии распространения воспалительного процесса и негативного воздействия на эвакуацию воспалительного экссудата из дыхательных путей.
Полученные в данном исследовании результаты по уменьшению интенсивности и ускорению купирования кашля при острых респираторных инфекциях у взрослых пациентов оказались сопоставимы с результатами ранее проведенного сравнительного исследования Ренгалина с кодеинсодержащим противокашлевым препаратом [16].
Описанные эффекты препарата обусловлены модулирующим влиянием компонентов препарата на функциональную активность рецепторов-мишеней – брадикининовых, гистаминовых и опиатных рецепторов, что обеспечивает воздействие на центральные и периферические звенья кашлевого рефлекса, а также причину кашля − воспаление в респираторном тракте [10, 11]. Особенностью препарата Ренгалин и его терапевтических эффектов является комплексное воздействие на различные звенья патогенеза кашля при ОРИ. В начальном периоде имеет значение балансирующее влияние препарата на опиатные рецепторы для обеспечения противокашлевого и анальгезирующего действия. РА АТ к морфину разрывают рефлекторную дугу кашля, понижают порог возбуждения ирритантных рецепторов, что приводит к противокашлевому эффекту. В последующий период ОРИ, когда преобладает экссудативно-катаральное воспаление, значимо влияние компонентов препарата на брадикининовые и гистаминовые рецепторы. Эффекты двух других компонентов препарата (РА АТ к брадикинину и гистамину) за счет воздействия на различные этапы формирования кашлевого рефлекса способствуют уменьшению отека, воспаления, спазма гладкой мускулатуры дыхательных путей, улучшают легочный клиренс, т.е. оказывают протуссивное или оптимизирующее кашель действие, при этом выраженность кашлевого рефлекса сохраняется на физиологическом уровне. Противовоспалительный, антигистаминный и спазмолитический эффекты способствуют разрешению инфекционно-воспалительного процесса в дыхательных путях. За счет этого происходит торможение образования густой вязкой мокроты и более легкое ее отхождение, предупреждение распространения патологического процесса в нижние отделы респираторного тракта. Фармакологические эффекты препараты позволяют не только сократить сроки купирования кашля, но и способствуют выздоровлению пациентов от ОРИ.
Ограничения исследования. В данное исследование не включали пациентов с рядом сопутствующих заболеваний, таких как хронические болезни легких (хроническая обструктивная болезнь легких, бронхиальная астма, бронхоэктатическая болезнь), медицинскими состояниями, которые ассоциированы с тяжелым течением острой респираторной инфекции. Участникам исследования не проводилась этиологическая и клиническая дифференциальная диагностика ОРИ, что также могло повлиять на динамику тяжести кашля и сроки выздоровления пациентов. Все это ограничивает возможность прогнозирования эффекта от проводимого лечения кашля с помощью исследуемого препарата у данной категории пациентов.
Заключение
На сегодняшний день лекарственные средства для лечения кашля при ОРИ представлены множеством различных препаратов разного происхождения и механизма действия. Лекарственные препараты, применяемые для лечения кашля при ОРИ, как правило, являются симптоматическими средствами и не оказывают влияния на патогенез вирус-индуцированного воспаления в дыхательных путях. Препарат Ренгалин, благодаря своему составу, оказывает комплексное действие (противокашлевое, противовоспалительное, бронхолитическое), что позволяет достигать терапевтической цели при лечении пациентов с кашлем в течение всего периода ОРИ.
Результаты проведенного клинического исследования подтвердили эффективность и безопасность жидкой лекарственной формы препарата Ренгалин в лечении кашля у взрослых пациентов.
Применение Ренгалина способствовало уменьшению тяжести кашля, сокращению его длительности и катарального синдрома в целом, ускорению выздоровления пациентов. Значимое противокашлевое действие в виде снижения числа эпизодов кашля начиналось со вторых суток наблюдения. Лечение Ренгалином в течение трех дней препятствовало развитию выраженной экссудации с образованием вязкой мокроты, что существенно сокращало необходимость дополнительных назначений муколитических препаратов на последующих стадиях течения острого инфекционного процесса в дыхательных путях. Ренгалин не оказывал негативного воздействия на мукоцилиарный клиренс и опосредованные им процессы эвакуации воспалительного экссудата из дыхательных путей. Ренгалин не вызывал побочных реакций, характерных для противокашлевых препаратов центрального действия (седативного и снотворного эффектов, угнетения дыхания, нарушения моторики желудочно-кишечного тракта, привыкания и лекарственной зависимости), хорошо переносился больными и сочетался с другими лекарственными средствами для лечения ОРИ и сопутствующих заболеваний. По оценкам врачей-исследователей, лечение кашля на фоне острой респираторной инфекции безопасно и более эффективно по сравнению плацебо-терапией.


