С момента описания синдрома обструктивного апноэ сна (СОАС) и первых попыток его лечения хирургическими и консервативными методами существует некий антагонизм между двумя основными подходами к лечению СОАС, связанный с менталитетом врачей-оториноларингологов и врачей-сомнологов. Радикальный подход противостоит неинвазивным способам коррекции дыхательных нарушений во время сна. Зачастую это связано с непониманием патофизиологических механизмов, приводящих к развитию СОАС, с одной стороны, и отрицанием структурных особенностей верхних дыхательных путей (ВДП) и возможностей их коррекции хирургическим путем, со стороны апологетов консервативного лечения. Безусловно, некий компромисс должен быть найден. Однако поиск решения необходимо вести с учетом доказательной базы знаний и клинического опыта. Не менее важными являются и предпочтения самого пациента, которому должна быть предоставлена полноценная информация обо всех способах коррекции СОАС, преимуществах и потенциальных осложнениях того или иного метода в каждом конкретном случае, а также спрогнозирована стойкость эффекта лечения.
Одним из ключевых моментов в выборе терапии является полноценная диагностика, которая должна проводиться по международным стандартам и включать как консультации оториноларинголога, сомнолога, а при необходимости и врачей других специальностей, так и различные лабораторно-инструментальные методы.
МАТЕРИАЛЫ И МЕТОДЫ
За период с февраля 2011 г. по июль 2015 г. было выполнено полиграфическое обследование 728 пациентов (530 мужчин и 198 женщин) с жалобами на храп. Средний возраст больных, вошедших в исследование, составил 45,6 (стандартное отклонение [SD] 11,5) года, медиана возрастного распределения – 45 лет, разброс значений в возрастном ряду составил 64 года, находился в пределах от минимального значения 14 лет до максимального 78 лет. Среди мужчин средний возраст составил 43,4 (SD 11,6) года, медиана – 45 лет, разброс – 59 лет (от 15 до 74 лет). Средний возраст женщин – 51,5 (SD 11,8) года, медиана – 45 лет, разброс – 64 года (от 14 до 78 лет). Наибольший удельный вес (более 95%) обследованных пришелся на лиц трудоспособного возраста, что указывает на серьезное социальное значение СОАС.
Обследование проводилось в соответствии со стандартами, опубликованными Американской академией медицины сна (American Academy of Sleep Medicine, AASM) [1]. Для установления диагноза и степени тяжести СОАС всем пациентам в ночное время выполнялся полиграфический мониторинг. Для этого использовали прибор «SomnoCheck2» с программным обеспечением «SomnoLab» производства Weinmann (Германия). Полисомнографическое исследование проводилось на полисомнографе «Embla N7000» (Natus, Embla, США), программное обеспечение «RemLogic». В результате ночного полиграфического мониторинга выявлялось наличие клинически значимых остановок дыхания, определялась их продолжительность, частота и тип. Каждый из эпизодов апноэ/гипопноэ сна классифицировался как обструктивный, центральный либо смешанный тип. В соответствии с современной классификацией, апноэ – это прекращение назофарингеального потока воздуха продолжительностью 10 с и более, гипопноэ – снижение воздушного потока на 50–80% от базального значения в течение 10 с и более с последующей десатурацией на 3% и более от текущего значения. При наличии полисомнографического оборудования эпизоды гипопноэ оценивались также с использованием критерия, учитывающего наличие микропробуждения.
 Индекс апноэ/гипопноэ (ИАГ) соответствует среднему числу эпизодов апноэ и гипопноэ, зарегистрированных во время диагностической ночи/сна за 1 ч, и характеризует степень тяжести СОАС. Согласно рекомендациям AASM, СОАС подразделяют на три степени тяжести в зависимости от значения ИАГ. Норму составляет ИАГ < 5; легкая степень СОАС характерна при 5 ≤ ИАГ < 15; средняя – 15 ≤ ИАГ < 30; тяжелая степень СОАС отмечается при ИАГ ≥ 30.
Индекс апноэ/гипопноэ (ИАГ) соответствует среднему числу эпизодов апноэ и гипопноэ, зарегистрированных во время диагностической ночи/сна за 1 ч, и характеризует степень тяжести СОАС. Согласно рекомендациям AASM, СОАС подразделяют на три степени тяжести в зависимости от значения ИАГ. Норму составляет ИАГ < 5; легкая степень СОАС характерна при 5 ≤ ИАГ < 15; средняя – 15 ≤ ИАГ < 30; тяжелая степень СОАС отмечается при ИАГ ≥ 30.
Выраженность артериальной гипоксемии оценивали по величине индекса десатураций (количество эпизодов понижения насыщения гемоглобина крови кислородом на 3% и более от текущего значения) и минимальному уровню сатурации. Продолжительность периодов апноэ, гипопноэ, десатурации измерялась в секундах. При проведении полиграфического исследования для каждого пациента определялась продолжительность времени корректного положения датчиков назального потока и пульсоксиметрического сенсора. На основании полученных данных осуществлялся расчет ИАГ и индекса десатураций (среднее количество эпизодов снижения насыщения гемоглобина крови кислородом за 1 ч исследования). После завершения анализа кривых назального потока в сочетании с данными пульсоксиметрии и торакоабдоминальных движений выполнялась оценка влияния положения тела на частоту дыхательных нарушений.
По окончании ночного полиграфического мониторинга автоматический программный анализ дополнялся визуальным анализом полиграфической записи ночного мониторинга. Это позволило избежать ошибок либо искажения результатов, связанных с некорректной автоматической интерпретацией записи. Полученные данные использовались для определения диагноза в соответствии с действующей Международной классификацией нарушений сна (3-й пересмотр). При формулировке диагноза указывалось следующее:
- основная нозологическая форма (СОАС, дыхание Чейн–Стокса, синдром альвеолярной гиповентиляции/гипоксемии и др.);
- степень тяжести, если в качестве нозологической формы был определен СОАС (легкая, средняя, тяжелая);
- наличие позиционной зависимости нарушений дыхания, зависимости от REM, NREM фаз сна;
- наличие признаков хронической артериальной гипоксемии.
У каждого из пациентов осуществлялся расчет индекса массы тела (ИМТ) для определения влияния избытка веса на тяжесть дыхательных нарушений во время сна. Выявление большого количества дыхательных нарушений центрального происхождения, преобладающих над частотой обструктивных, рассматривалось как повод для подробного диагностического поиска в отношении неврологической и сердечно-сосудистой патологии. При сборе анамнеза внимание уделялось наличию артериальной гипертензии (количество препаратов, используемых для коррекции повышенного артериального давления), симптомов ишемической болезни сердца, хронических обструктивных болезней легких, сахарного диабета и других сопутствующих заболеваний.
Определение уровня дневной сонливости выполнялось с помощью шкалы сонливости Эпворта. Суммарное количество баллов 10 и более расценивалось как повышенная дневная сонливость. Интенсивность храпа определяли в соответствии с визуальной аналоговой шкалой от 0 до 10 баллов (0 баллов − отсутствие храпа; 10 баллов − максимально выраженный храп). При стандартном оториноларингологическом осмотре оценивали:
- выраженность гипертрофии небного язычка;
- состояние небных дужек (широкие, провисшие, парусообразно натянутые задние небные дужки);
- степень гипертрофии небных и язычной миндалин;
- положение языка по Фридману;
- размер и форму надгортанника;
- сужение просвета глотки (за счет гипертрофии мышц боковых стенок, отложений жировой ткани);
- соотношение языка и неба по шкале Маллампати в баллах:
- 1 балл: свободный край мягкого неба имеет форму свода, хорошо обозримы небные дужки, мягкое небо, язычок;
- 2 балла: свободный конец небного язычка расположен ниже корня языка, визуализируется верхняя треть язычка;
- 3 балла: свободный край мягкого неба находится на уровне корня языка;
- 4 балла: расположение свободного края мягкого неба ниже корня языка, фарингоскопически обозримо только твердое небо.
С целью визуализации уровня обструкции выполняли эндоскопическое исследование ВДП (проба Мюллера или DISE).
Характер и степень сужения дыхательных путей на различных уровнях отражали в соответствии с классификацией NOHL, где:
- N (nasopharyngeal) – назофарингеальный уровень;
- О (oropharyngeal) – орофарингеальный уровень;
- H (hypopharyngeal) – гипофарингеальный уровень;
- L (laryngeal) – ларингеальный уровень.
Для обозначения степени обструкции после каждого уровня указывается числовое значение от 0 до 4, где:
- 0 – обструкция отсутствует;
- 1 – смыкание просвета дыхательных путей на 25%;
- 2 – сужение ВДП на 50%;
- 3 – субтотальная обструкция (≥75%);
- 4 – тотальная обструкция (100%).
Указывают направление: передне-задняя (AP), боковая (B), концентрическая (C).
Статистический анализ данных проводился с помощью программного комплекса Statistica 8,0. Статистически значимое различие определялось при p<0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
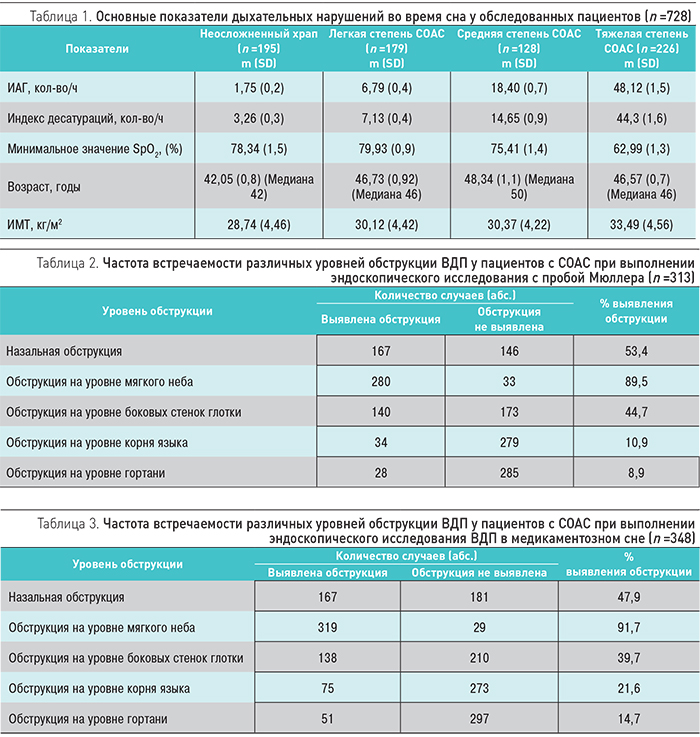
Среди обследованных пациентов с жалобами на храп в 195 случаях (26,14%) не было выявлено значимых нарушений дыхания, периодический храп наблюдался у всех обратившихся больных. В 179 случаях (23,99%) была констатирована легкая, в 128 случаях (17,16%) средняя степень СОАС. Из числа обследованных у 226 (30,29%) человек была выявлена тяжелая форма СОАС. В табл. 1 приведены средние показатели ИАГ, индекса десатураций (среднее количество эпизодов снижения насыщения гемоглобина крови кислородом за 1 ч исследования), возраста и ИМТ у пациентов в зависимости от степени тяжести выявленного СОАС.
 Помимо отличий, обусловленных непосредственно СОАС (ИАГ, выраженность гипоксемических нарушений), пациенты с тяжелой степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом, легкой и средней степенью по показателю ИМТ (p<0,001); пациенты со средней степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом (p<0,025); пациенты с легкой степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом (p<0,05).
Помимо отличий, обусловленных непосредственно СОАС (ИАГ, выраженность гипоксемических нарушений), пациенты с тяжелой степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом, легкой и средней степенью по показателю ИМТ (p<0,001); пациенты со средней степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом (p<0,025); пациенты с легкой степенью СОАС статистически значимо отличались от пациентов с неосложненным храпом (p<0,05).
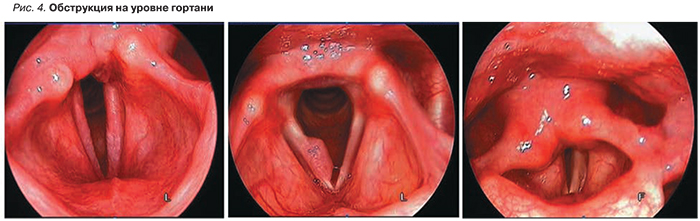
У пациентов с СОАС к обструкции предрасполагает ряд изменений ВДП: гипертрофия мягкого неба, небного язычка, небных миндалин, провисание задних небных дужек, гипертрофия небных миндалин и т.д. При анализе результатов эндоскопических исследований наиболее часто выявлялась назальная обструкция, а также обструкция на уровне мягкого неба и боковых стенок глотки. Реже встречалась обструкция на уровне корня языка и гортани. Совокупные данные по различным видам обструкции ВДП представлены в табл. 2, 3.
На рис. 1–4 представлены примеры различных видов обструкции ВДП. Назофарингеальный и орофарингеальный уровни обструкции выявлялись с одинаковой частотой при эндоскопическом исследовании ВДП как с седацией, так и без нее. Обструкция на уровне корня языка и на уровне гортани выявляется чаще при выполнении эндоскопического исследования ВДП в медикаментозном сне. При выполнении эндоскопического исследования ВДП с пробой Мюллера среди пациентов с СОАС тяжелой степени не выявлено ни одного случая одноуровневой обструкции. Частота встречаемости СОАС тяжелой степени возрастает при увеличении числа уровней обструкции: 12,9% – при 2-х, 47,1% – при 3-х и 53,6% – при 4-х уровнях обструкции. Сходная динамика выявления частоты СОАС тяжелой степени в группах с различными видами обструкции прослеживалась и при эндоскопическом исследовании ВДП в медикаментозном сне: при одноуровневой обструкции случаев тяжелого СОАС не выявлено, тогда как среди пациентов с 2-, 3- и 4-уровневой обструкцией частота встречаемости СОАС тяжелой степени соответствовала значениям 11,3, 34,1 и 79,2% соответственно.
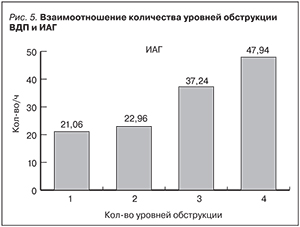
На рис. 5 представлена зависимость между количеством уровней обструкции и ИАГ.
Установлено, что оценка мягкого неба в 1–2 балла по шкале Маллампати встречалась при СОАС легкой степени у 53,79%, СОАС средней степени – у 44,44%, СОАС тяжелой степени– у 19,21% пациентов. Оценка в 3–4 балла отмечалась при СОАС легкой степени у 44,30%, СОАС средней степени – у 50,37% пациентов, СОАС тяжелой степени – у 77,29% пациентов. Таким образом, при СОАС средней и тяжелой степени у большинства пациентов наблюдались изменения соотношения свободного края мягкого неба и корня языка, что затрудняло движение воздушного потока.
Гипертрофия небных миндалин была выявлена у 19,62% пациентов с СОАС легкой степени, у 22,96% пациентов с СОАС средней степени и у 36,24% пациентов, страдавших тяжелой формой СОАС.
Провисшие, широкие и парусообразно натянутые задние небные дужки выявлялись значительно чаще у пациентов с СОАС средней и тяжелой степени: в 82,22 и 92,57% соответственно. Данный признак был диагностирован у 74,68% пациентов с легкой формой СОАС. Вовлечение боковых стенок глотки за счет отложения жировых масс в парафарингеальной области приводило к увеличению частоты встречаемости пациентов с СОАС тяжелой степени. 85% исследуемых пациентов с данным признаком имели тяжелую форму СОАС.
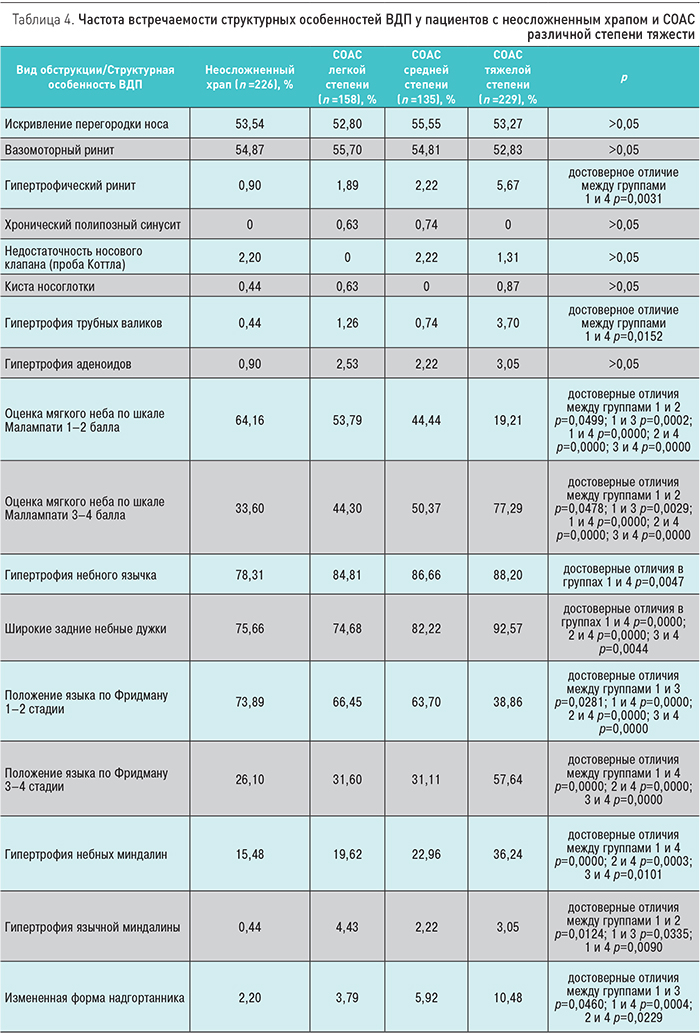
В табл. 4 представлена частота встречаемости различных видов обструкции и структурных особенностей ВДП у пациентов с неосложненным храпом и СОАС различной степени тяжести.
Большое значение с точки зрения патогенеза СОАС имеет избыточный вес. При увеличении веса возрастает вероятность многоуровневой обструкции. Результаты исследования позволяют предположить с высокой степенью вероятности, что повышение ИАГ в связи с увеличением количества уровней обструкции, прежде всего, объясняется повышением массы тела и избыточным отложением жира в тканях ВДП. Однако такой вывод можно сделать для обследованной группы пациентов – среднего возраста, патофизиология дыхательных нарушений во время сна у лиц пожилого возраста более комплексная.
Хирургические методы лечения СОАС выполняются уже на протяжении десятилетий. Однако до настоящего момента доказательная база эффективности хирургического лечения СОАС остается недостаточной [2]. Выводы большинства исследований были сделаны по результатам лечения достаточно малочисленных и отобранных групп, к тому же применялись различные хирургические методики. Методическое обеспечение объективного контроля сна зачастую не нормировалось. Хотя ИАГ как критерий эффективности лечения является на данный момент основным, существует ряд существенных ограничений в его использовании. В то же время приходиться признать, что, несмотря на все несовершенство ИАГ как критерия эффективности лечения, в настоящее время не существует более объективных параметров оценки лечебного воздействия.
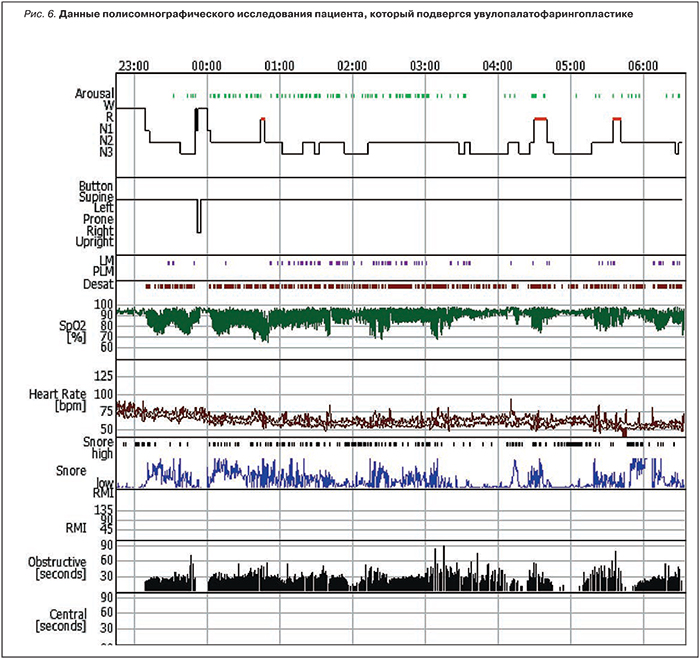
В качестве примера приводим данные полисомнографического исследования пациента, который подвергся увулопалатофарингопластике (рис. 6). Несмотря на проведенное оперативное вмешательство, остается крайне высоким значение ИАГ=85,6/час (N<5), отмечается наличие альвеолярной гиповентиляции. Общее количество эпизодов дыхательных нарушений 618, из них 575 обструктивных апноэ, 43 обструктивных гипопноэ, 0 центральных апноэ. Максимальная продолжительность обструктивного апноэ 89,4 с. Минимальное значение SpO2 65,0% (N>90%). Изменена и структура сна. Отмечается значительное уменьшение общей продолжительности REM фазы сна – 4,7% (норма 20–25%). Индекс ЭЭГ-активаций 36,2 (N<21). Подавляющее число ЭЭГ-активаций ассоциировано с эпизодами обструктивного апноэ.
Среди хирургических методов лечения наиболее эффективными являются многоуровневые оперативные вмешательства, а также выполнение ортогнатических операций (верхне-нижнечелюстное выдвижение), предусматривающих увеличение пространства ВДП за счет смещения вперед мягкого неба, корня языка. Снижение ИАГ при данной методике составило 87% (95% ДИ 80–92), что является очень хорошим результатом. Однако сложность выполнения данного хирургического вмешательства не позволяет сделать однозначный вывод в пользу данного вида лечения, и поэтому в настоящее время средством первой линии лечения СОАС является «сипап»-терапия. Данная рекомендация основана на высоком уровне доказательств эффективности «сипап»-терапии в предотвращении коллапса ВДП и уменьшении степени выраженности симптомов, таких, например, как сонливость в дневное время [3]. В последующих публикациях мы представим результаты собственных исследований различных видов хирургических вмешательств, а также «сипап»-терапии в лечении больных СОАС.
ВЫВОДЫ
- Анатомические особенности ВДП влияют на степень тяжести СОАС.
- При увеличении количества уровней обструкций ВДП увеличивается степень тяжести СОАС.
- При увеличении ИМТ увеличивается как количество обструкций ВДП на различных уровнях, так и степень тяжести СОАС.
- Выбор метода лечения СОАС должен осуществляться по результатам полиграфического/полисомнографического исследования и данных объективного контроля состояния ВДП.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Лечение пациента с СОАС должно осуществляться при непосредственном взаимодействии сомнолога и оториноларинголога.
- Каждому пациенту с СОАС должно быть проведено полиграфическое/полисомнографическое исследование и осмотр оториноларингологом.
- «Сипап»-терапия должна быть рекомендована пациентам со средней/тяжелой степенью апноэ в качестве первой линии лечения с целью уменьшения периоперативного риска даже при наличии изменений ВДП, приводящих к обструкции и требующих хирургической коррекции.


