ВВЕДЕНИЕ
По данным исследования Всемирной организации здравоохранения (ВОЗ), хронические неинфекционные заболевания (ХНИЗ), такие как сердечно-сосудистые, бронхолегочные, сахарный диабет (СД) и злокачественные новообразования, признаны наиболее распространенной причиной смертности во всем мире: на их совокупную долю приходится до 74% всех летальных случаев [1, 2]. Ежегодно от ХНИЗ умирают около 41 млн человек, при этом почти 75% из них приходится на страны с низким и средним уровнем дохода. Более того, 86% таких пациентов умирают, не дожив до 70-летия [3].
Впервые опубликованное в 2022 г. Национальное руководство, посвященное актуальному вопросу профилактики ХНИЗ в России, в основном акцентирует внимание специалистов на проблеме старческой астении или хрупкости [4], при этом частым следствием какого-либо специфического соматического заболевания выступает хроническая усталость, которая может наблюдаться у лиц различного возраста [5]. Астения – довольно распространенный и вместе с тем тревожный симптом многих хронических соматических заболеваний. Так, на нее жалуются до 40% больных при СД, до 50% – при заболеваниях сердечно-сосудистой и респираторной систем, до 60% – при цереброваскулярной патологии и злокачественных новообразованиях [5–8]. По своей распространенности астения не уступает тревожно-депрессивным расстройствам [9].
Больные могут описывать различные качественные компоненты астении: эмоциональные (потеря интереса и мотивации), когнитивные (снижение умственной активности и работоспособности), поведенческие (уменьшение производительности) и физические (например, мышечная слабость) [5]. Наличие астении негативно сказывается на способности выполнять повседневную деятельность, такую как уход за собой, домашние дела, работа и общение, и способствует ухудшению качества жизни [10].
Этиология синдрома астении сложна, противоречива и до конца не изучена. Существует множество теорий, рассматривающих участие инфекций, иммунной системы, эндокринной дисфункции и генетики в этой сложной коммуникации [5, 11]. В целом было признано, что возникновение астенического синдрома лучше всего можно объяснить взаимодействием биологических, психологических и социальных факторов [6, 12].
На сегодняшний день используется несколько стратегий борьбы с астенией, включая когнитивно-поведенческую терапию, лечебную физкультуру, рекомендации по здоровому образу жизни или прием медикаментов [7]. В частности, изменение образа жизни заключается в выделении большего времени на отдых и сон, а также уменьшении или устранении потенциальных источников чрезмерного стресса. Вместе с тем данные об эффективности предлагающихся вмешательств достаточно противоречивы, что создает проблемы для амбулаторных врачей при назначении лечения пациентам с астенией [13].
Цель исследования – оценить эффективность медикаментозного лечения синдрома астении препаратом Энерион (сульбутиамин) у пациентов с ХНИЗ в условиях амбулаторной клинической практики.
МАТЕРИАЛ И МЕТОДЫ
Проведено открытое проспективное клиническое исследование. Диагностика астении была выполнена у 2373 пациентов с ХНИЗ в возрасте от 18 до 95 лет (1337 женщин и 1036 мужчин), обращавшихся за плановой консультативной помощью к участковым врачам-терапевтам поликлиник г. Красноярска. Средний возраст пациентов составил 56,4 ± 14,9 года. Исследование проводилось в июле – августе 2023 г. и было одобрено локальным этическим комитетом ФГБОУ ВО «Красноярский государственный медицинский университет им. профессора В.Ф. Войно-Ясенецкого» Минздрава России (протокол № 119 от 07.07.2023).
Критериями включения в исследование: наличие ХНИЗ, возраст старше 18 лет, подписание информированного согласия.
Критерии невключения: отказ пациента отвечать на вопросы анкеты, отсутствие ХНИЗ, беременность, возраст младше 18 лет, отказ от подписания информированного согласия.
Выполнялись опрос пациентов, сбор жалоб и анамнеза, физикальное обследование, анализ материалов амбулаторной карты. Согласно полученным результатам с опорой на современные клинические рекомендации, пациентам был установлен диагноз ХНИЗ [3]. В нашей работе мы относили к ХНИЗ 4 основные группы болезней: сердечно-сосудистые заболевания, рак, хронические респираторные заболевания и СД 2-го типа.
Диагностика астении проводилась субъективно с помощью шкал оценки астении Multidimensional Fatigue Inventory (MFI-20) и тяжести астении Fatigue Severity Scale (FSS) [14]. Опросник MFI-20 первоначально был предложен к использованию у пациентов с раком в 1995 г.: он включает 20 пунктов и характеризует показатели общей и физической астении, снижения активности и мотивации, а также психическую астению [15]. С тех пор он переведен на несколько языков и имеет довольно высокие коэффициенты достоверности (коэффициент альфа в диапазоне от 0,80 до 0,90) полученных с его помощью результатов [16–18]. В норме суммарный балл по каждой из субшкал не должен превышать 12, а общий – 20–30.
Опросник FSS содержит 9 пунктов и первоначально был валидирован у пациентов с рассеянным склерозом и системной красной волчанкой [19]. В последующем он использовался для оценки астении у больных на поздних стадиях рака и у пациентов с разными локализациями злокачественных опухолей. При этом FSS также имеет высокие уровни достоверности полученных результатов тестирования (коэффициент альфа от 0,94 до 0,96) [16]. В норме суммарное количество баллов по этому опроснику не должно превышать 36.
В ходе скрининга астения была выявлена нами у 847 пациентов с ХНИЗ (средний возраст 60,6 ± 14,1 года) – у 326 мужчин (38,5%) и 521 женщины (61,5%). В зависимости от проводимого лечения все пациенты с астенией были разделены на 3 группы:
- 1-я – 446 больных (52,7%) с ХНИЗ и астенией, не получавших противоастеническую терапию и не изменявших привычный образ жизни;
- 2-я – 71 пациент (8,3%) с ХНИЗ и астенией, изменивший только образ жизни;
- 3-я – 330 человек (39,0%) с ХНИЗ и астенией, получавших препарат Энерион (сульбутиамин) в дозе 600 мг/сут. в течение 4 нед. Кроме того, участники 3-й группы могли при желании модифицировать образ жизни. Соответствующие рекомендации включали оптимизацию режима труда и отдыха (рекомендовалось за 30–60 мин. до сна не пользоваться электронными устройствами, по возможности максимально ограничивать время за экраном в течение дня), полноценный сон, регулярную физическую активность, лечебную гимнастику, сбалансированное питание, планирование дня и недели заранее, контроль активности и уровня энергии (не пытаться продолжать деятельность, если появилось ощущение усталости, чередовать небольшие периоды физической и умственной активности, делать перерывы для отдыха и релаксации в течение рабочего дня).
Статистический анализ данных осуществлялся с помощью пакета прикладных программ STATISTICA 12.0 (StatSoft Inc., США). Проверка нормальности распределения проводилась с использованием критерия Шапиро – Уилка. Количественные показатели представлены в виде медианы (Me) и интерквартильного размаха в виде 25 и 75 процентилей (Q0,25–Q0,75). Данные частот приведены в абсолютных значениях и процентах (n (%)). Все количественные данные в нашем исследовании были распределены ненормально, в связи с чем для сравнения двух независимых групп применялся непараметрический критерий Манна – Уитни. Анализ различия частот в 2 независимых группах выполнялся при помощи критерия Пирсона χ2 с поправкой Йетса на непрерывность. При сравнении зависимых групп использовался непараметрический U-критерий Вилкоксона. Различия считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Среди 2373 обследованных пациентов с ХНИЗ критериям астении соответствовало 35,7% (847 человек). В таблице 1 представлена сравнительная характеристика испытуемых, на рисунке 1 – частотное соотношение ХНИЗ в исследуемых группах.
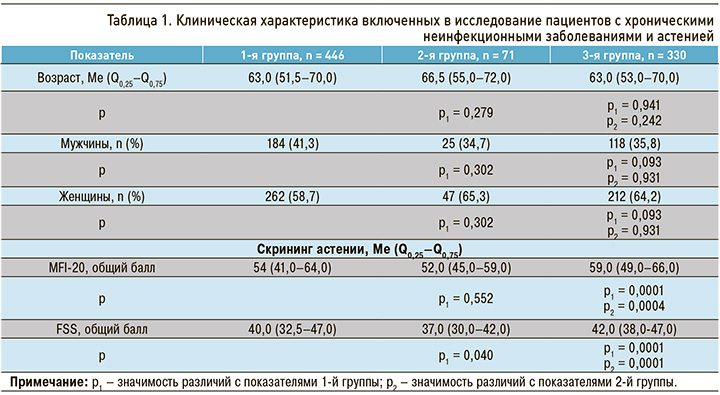
Как видно из таблицы 1 и рисунка 1, между участниками исследования не было достоверных различий по половозрастной структуре и ведущим нозологическим патологиям. Вместе с тем обнаружено, что пациенты 2-й группы в соответствии со шкалой FSS имели достоверно меньшую степень выраженности астенического синдрома в сравнении с пациентами 1-й и 3-й групп, а участники 3-й группы на 1-м скрининге астении продемонстрировали большую степень ее тяжести по обеим шкалам в сравнении с лицами 1-й и 2-й групп.
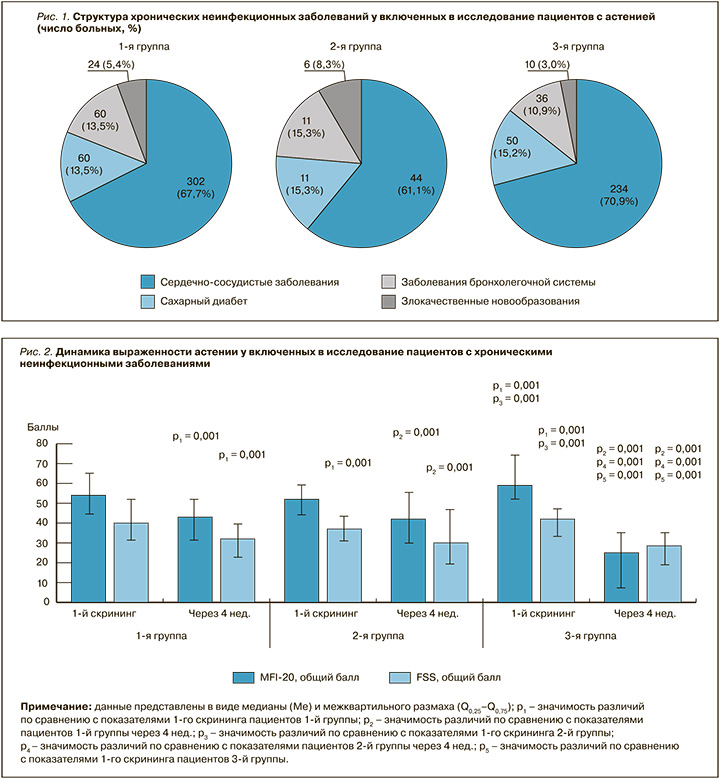
В ходе динамического наблюдения за исследуемыми обнаружено, что у пациентов 1-й группы, не предпринимавших никаких попыток изменить образ жизни и не получавших противоастенической терапии, все же отмечалось достоверное снижение общего балла по опроснику MFI-20 и шкале FSS, при этом во 2-й группе через 4 нед. модифицированного образа жизни степень выраженности астении была достоверно меньше в сравнении с больными 1-й группы. Вместе с тем, несмотря на наблюдавшееся снижение, показатели выраженности астении в 1-й и 2-й группах не достигали нормы при оценке по шкале MFI-20. В связи с этим обращают на себя внимание результаты, полученные у пациентов 3-й группы, в которой исходные значения по данным скрининга астении были хуже, чем в 1-й и 2-й группах. У участников этой выборки на фоне приема сульбутиамина установлена достоверная и полная нормализация общего балла по опросникам MFI-20 и FSS (рис. 2).
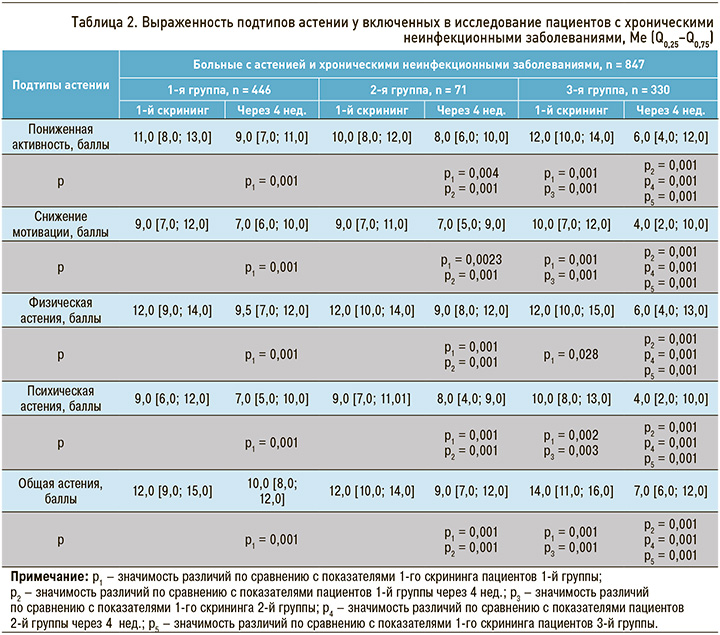
При анализе подтипов астении у пациентов как 1-й, так и 2-й группы через 4 нед. наблюдения отмечалось уменьшение таких проявлений астенического синдрома, как пониженная активность, снижение мотивации, физическая и психическая усталость, а также общей астении (табл. 2). При этом у пациентов 3-й группы в 1-е сутки скрининга регистрировалась достоверно более выраженная степень тяжести перечисленных подтипов в сравнении как с 1-й, так и 2-й группой, за исключением показателя физической астении (не отличавшегося в 1-е сутки скрининга от значений 2-й группы). Тем не менее у пациентов, получавших сульбутиамин в течение 4 нед., была достигнута полная нормализация показателей по всем подтипам астении, причем через месяц наблюдения суммарный балл по каждой из подшкал оказался достоверно ниже в сравнении с пациентами как 1-й, так и 2-й групп. Кроме того, ни у одного из участников исследования не наблюдалось побочных эффектов, связанных с приемом сульбутиамина.
ОБСУЖДЕНИЕ
Единого общепринятого определения астении не существует; одна из предложенных дефиниций описывается ее как симптом, который не может быть облегчен обычными методиками восстановления энергии и при этом в различной степени ухудшает способность человека выполнять обычную повседневную деятельность [5]. Пациенты описывают усталость как вялость, недостаток энергии, утомляемость, сонливость или физическую слабость [10]. При этом астению следует отличать от мышечной слабости, например, вследствие миопатии или неврологического расстройства, а также от дневной сонливости, которая приводит к наступлению сна уже во время обычной повседневной деятельности. Астения, продолжающаяся более 6 мес., называется хронической.
Сульбутиамин является производным тиамина, который был разработан в Японии в середине 1960-х гг. как препарат для лечения бери-бери – болезни, возникающей вследствие недостатка витамина В1 в организме [20]. С тех пор были описаны различные потенциальные сферы применения этого препарата. Например, есть ряд доказательств того, что сульбутиамин может оказывать противоастеническое, ноотропное и антиоксидантное действие, что способствовало его использованию в качестве спортивной добавки. Более того, эта молекула была предложена в качестве возможного средства лечения микроспоридиоза и даже некоторых видов рака [21, 22]. Несмотря на эти потенциальные эффекты, сульбутиамин все еще остается относительно неизвестной субстанцией, что определяет актуальность настоящей работы.
Модификация двух молекул тиамина в сульбутиамин повышает липофильные характеристики последнего. Эксперименты in vivo показали, что сульбутиамин может трансформироваться в производные тиамина после восстановления дисульфидной связи и регенерации замкнутых тиазолиевых колец, давая на выходе в основном две молекулы изобутирилтиамина [20]. После инъекции сульбутиамина его поведение в плазме крови оказалось точно таким же, как и у «настоящего» тиамина. Еще один важный момент заключается в том, что сульбутиамин повышает уровень тиамина и эфиров фосфата тиамина в мозге; это может иметь потенциальное положительное влияние на хроническую астению.
Наиболее изученным производным тиамина является тиаминдифосат. Ранние исследования продемонстрировали роль данного соединения в качестве кофактора митохондриальной пируват- и альфа-кетоглутаратдегидрогеназы, а также цитозольной транскетолазы – ферментов, участвующих в окислительном метаболизме и через это воздействующих на многие функциональные системы. С учетом этого к дефициту тиамина особенно чувствительна центральная нервная система [23]. Нейропротективное действие сульбутиамина может быть объяснено главным образом содержанием в нем тиола, который обладает антиоксидантными эффектами, предотвращая окислительный стресс в клетках головного мозга [24].
Еще одно производное тиамина – тиаминтрифосфат. Он, по-видимому, преимущественно связан с плазматическими, митохондриальными и ядерными мембранами нейронов и вовлечен в модуляцию их проницаемости. Кроме того, тиаминтрифосфат синтезируется цитозольной аденилаткиназой в скелетных мышцах и тканях организма [20].
После сделанного в работе Micheau J. et al. вывода о том, что частичное улучшение памяти у мышей может быть обусловлено способностью сульбутиамина вызывать холинергическую модуляцию гиппокампа, этот препарат начали назначать для лечения астенических состояний [25, 26]. По результатам исследования Shah S.N., где сульбутиамин применялся у пациентов, имевших одновременно инфекцию и усталость, было высказано предположение, что увеличение передачи ацетилхолина и, следовательно, активации восходящего уровня ретикулярной формации (потенциально вызываемого сульбутиамином или каким-либо его производным) может быть ассоциировано с патогенезом астении и наблюдаемым улучшением состояния пациентов [27]. Вместе с тем постинфекционная астения обязательно уменьшается в 1-й месяц даже у пациентов, не принимавших сульбутиамин.
В открытом рандомизированном контролируемом исследовании Kiew K.K. et al. у пациентов с СД 2-го типа, страдающих полинейропатиями, после применения сульбутиамина в дозе 400 мг/сут. в течение 42 дней отмечалось улучшение параметров нервных сигналов [28]. В работе С.В. Гурак и соавт., включившей 44 человека после перенесенного инфаркта миокарда и 39 больных с постишемическим инсультом, было зафиксировано очевидное улучшение показателей астении по шкале MFI-20 на фоне терапии сульбутиамином в дозе 400 мг/сут. при хорошей переносимости препарата [29]. Другое исследование подтвердило эффективность и благоприятный профиль безопасности Энериона при его применении у пациентов с постинсультной астенией (n = 30) в дозе 200 мг 2 р./сут. в течение 4 нед. [30].
В исследовании пациентов с рассеянным склерозом (n = 26), выполненном в 2017 г. Sevim S. et al., использование сульбутиамина 400 мг/сут. на протяжении 2 мес. при хорошей переносимости сопровождалось снижением общего балла по шкале влияния усталости (Fatigue Impact Scale, FIS), а также другим подшкалам, оценивающим физическое, когнитивное и психосоциальное функционирование у лиц, которые проходили какое-либо лечение, модифицирующее заболевание. Тем не менее у пациентов, которые не получали никакого лечения, прием 400 мг сульбутиамина в день не вызывал существенного улучшения [26]. Исследователи предположили, что развитие астении при рассеянном склерозе может быть ассоциировано с дисбалансом дофамина, а сульбутиамин оказывает регулирующее влияние на метаболизм этого нейромедиатора у соответствующих пациентов.
В нашей работе сульбутиамин получала группа пациентов с достоверно более высокими показателями степени тяжести астении, выявленными на 1-м скрининге. Назначение Энериона больным с ХНИЗ в дозе 600 мг в течение 4 нед. привело к достоверному снижению и полной нормализации проявлений астении по уровню общего балла, определенного в соответствии с опросниками MFI-20 и FSS, а также к уменьшению выраженности всех подтипов астенического синдрома. При этом прием сульбутиамина не был связан с развитием каких-либо серьезных побочных эффектов.
Одним из интересных результатов настоящего исследования стало уменьшение выраженности различных подтипов астении у пациентов, которые не принимали сульбутиамин, но изменили образ жизни, а также у тех, кто не придерживался никаких рекомендаций в течение 4 нед. наблюдения. В этих группах значения общего балла по шкале FSS снизились до нормы, а по шкале MFI-20 уменьшились, но все же не достигли нормальных значений. Возможно, это обусловлено тем, что наше наблюдательное исследование не было рандомизированным, его участники имели неоднородную соматическую патологию, не была выделена группа плацебо-контроля, и не осуществлялся скрининг тревожно-депрессивных расстройств. Приведенные ограничения настоящей работы необходимо учитывать при планировании будущих исследований.
Тем не менее наше исследование является первым, в котором продемонстрирована эффективность сульбутиамина у относительно большой группы пациентов с ХНИЗ и астенией. Принимая во внимание отрицательное влияние астении на качество жизни пациентов, полученные нами данные крайне важно дополнительно подтвердить в долгосрочных плацебо-контролируемых и многоцентровых исследованиях.
ЗАКЛЮЧЕНИЕ
Изучение эффектов сульбутиамина началось 50 лет назад, но за это время было выполнено лишь ограниченное количество исследований, посвященных влиянию этого лекарственного средства на пациентов с хронической соматической патологией и астенией. Экспериментальные данные, наблюдательные исследования и клинические испытания свидетельствуют, что сульбутиамин обладает многоплановым влиянием на физиологию человека благодаря улучшению доставки тиамина в различные ткани, например в мозг, повышая антиоксидантную способность и модулируя действие белков [20].
По нашему мнению, сульбутиамин обладает большим терапевтическим потенциалом, и, возможно, представленная работа послужит отправной точкой для будущих исследований, посвященных изучению безопасности и эффективности этого препарата у пациентов с различными соматическими заболеваниями.


